Evaluating the Anticancer Potential of Ornithogalum saundersiae Saponins on Hepatocellular Carcinoma: A Transcriptome Sequencing Method
-
摘要: 目的:基于转录组测序发掘虎眼万年青皂苷(Ornithogalum saundersiae Saponins,OSW-1)作用于肝癌细胞(HEP3B)后的关键通路及差异表达基因。方法:利用转录组测序技术检测OSW-1处理HEP3B的基因表达数据,通过测定的序列信息精确地分析转录本,筛选与细胞存活相关的表达差异基因,得到核心基因,并通过实验验证OSW-1是否通过调控核心靶点治疗肝细胞癌。结果:MTT结果表明,经OSW-1给药后HEP3B细胞活性明显降低,且呈浓度依赖性。通过转录组测序检测,共获得1381个存在明显表达差异的基因,并且多数基因富集在TNF信号通路。进一步通过免疫荧光及Western blot表明,OSW-1干预HEP3B细胞后,p-PI3K、p-AKT、p-NF-κB蛋白水平表达降低。结论:OSW-1可能通过调控炎症信号通路降低炎症反应,抑制HEP3B细胞活性,可作为潜在的治疗肝癌的药物,以及为保肝护肝的保健食品研发提供实验依据。Abstract: To investigate the crucial pathways and differentially expressed genes following the action of Ornithogalum saundersiae Saponins (OSW-1) on liver cancer cells (HEP3B), this study utilized transcriptome sequencing technology to examine the gene expression data of HEP3B cells treated with OSW-1. By precisely analyzing the transcripts from the measured sequence information, differentially expressed genes related to cell survival were screened to identify core genes. Furthermore, experiments were conducted to verify whether OSW-1 could treat hepatocellular carcinoma by regulating the core targets. Results showed that the MTT assay revealed a significant reduction in HEP3B cell activity following OSW-1 treatment, which was dependent on the concentration. A total of 1381 genes showed significant differences in expression as a result of transcriptome sequencing, with a majority being involved in the TNF signaling pathway. Additionally, immunofluorescence and Western blot analysis indicated that the levels of p-PI3K, p-AKT, and p-NF-κB proteins were reduced in HEP3B cells after treatment with OSW-1. In conclusion, OSW-1 may suppress inflammation and reduce HEP3B cell activity by modulating inflammatory signaling pathways, suggesting its potential as a drug for liver cancer treatment and providing an experimental foundation for the development of healthy foods aimed at liver protection.
-
肝细胞癌(HCC)是世界范围内癌症相关疾病致死的第四大诱因[1]。其核心危险因素在于乙型肝炎疾病、嗜酒和非酒精性的脂肪性肝病[2−3]。目前,HCC的死亡率仍逐年升高[4]。临床阶段,HCC的干预策略包括了局部的消融、手术等。大部分病患在确诊的情况下已然处于晚期以及转移阶段,丧失了彻底根除的机会[5−7]。目前的研究表明,针对HCC存在潜在的治疗靶点,但多数药物实际应用时均临床疗效不佳,只是把生存期延长了数月。所以,急需寻找新的药物可以更有效地治疗HCC。HEP3B细胞系是Aden等人从一名8岁的美国男性黑人肝癌患者的活体标本分离出来的肝癌细胞系,是研究原发性肝癌的重要的细胞系模型。故选取HEP3B细胞系作为实验材料[8]。
转录组为特殊的物种、细胞类型等于特殊的阶段及环境下转录全部的RNA集合,涵盖了mRNA、非编码RNA。借助高通量测序的方式能够很好地确定已知基因表达的有关数据,此外基于测定序列数据能够精准地研究转录本cSNP/InDel、可变剪接、融合基因等序列及结构变异,这可为后续相关研究提供指引方向[9−11]。
虎眼万年青为典型的百合科虎眼万年青属的多年生常绿草本植株之一,产自南非,上世纪九十年代初期,日本研究人员首次提出其在抗肿瘤方面的功效[12−13]。虎眼万年青是一种常见的中药材和食材,同时也是一种天然的保健品,含有多种营养成分,如蛋白质、脂肪、碳水化合物、维生素、矿物质等,可以促进人体的生长发育,促进细胞的新陈代谢,增强人体的抵抗力[14]。其有效成分OSW-1是从虎眼万年青球茎中分离得到的一种酰化甾体皂苷,分子式为C47H68O15,分子量为873.0 g/mol,根据国际纯粹与应用化学联合会命名法命名为:[(2S,3R,4S,5R)-2 [(2S,3R,4S,5S)-3-acetyloxy-2-[[(3S,8R,9S,10R,13S,14S,16S,17S)-3,17-dihydroxy 10,13-dimethyl-17-[(2S)-6-methyl-3-oxoheptan-2-yl]-1,2,3,4,7,8,9,11,12,14,15,16 dodecahydrocyclopenta[a]phenanthren-16-yl]oxy]-5-hydroxyoxan-4-yl]oxy-4,5 dihydroxyoxan-3-yl] 4-methoxy benzoate][15]。该植株也是国内较为认可的调节肝癌以及肝病的有效药物,近几年更是在其他疾病的治疗方面也进行了深入研究[16−19]。现有的研究显示,OSW-1抗肿瘤功效为目前较为普遍的抗肿瘤药剂(如依托泊若、MTX等)的十倍甚至百倍,并且对正常细胞没有毒性,因此被认为可能逐渐取代具有严重化疗副作用的药物[20−21]。尽管OSW-1对治疗HCC有效,但其机制尚不清楚。因此,本研究基于转录组测序的方式,确定了差异表达基因同时实行基因本体学以及信号通路的富集处理,旨在阐明OSW-1处理HEP3B细胞转录组水平的变化,并进行实验验证,以阐明OSW-1治疗HCC的机制。
1. 材料与方法
1.1 材料与仪器
人肝癌细胞(HEP3B) 上海富衡生物科技有限公司,HEP3B使用EMEM(含20% FBS以及1% PS)培养基于培养箱(37 ℃、5% CO2)中进行培养;OSW-1(纯度>98%) 上海医恩医疗系统研发有限公司;EMEM培养基、胎牛血清、青霉素、链霉素、0.25% Trypsin-EDTA 上海达特希尔生物科技有限公司;二甲基亚砜、10xPBS、细胞裂解液RIPA、PMSF、Tween-20、彩虹蛋白上样Marker、10% SDS溶液、1.5 mol/L Tris-HCL缓冲液、1 mol/L Tris-HCl 缓冲液、5×蛋白上样Buffer、BD脱脂牛奶 美国BD公司;TEMED 美国Thermo scientific;硝酸聚酯纤维膜 美国Merck Millipore;无水乙醇、无水甲醇 上海阿拉丁公司;30%聚丙烯酰胺 南京碧云天科技有限公司;荧光二抗 美国Licor;p-PI3K、p-AKT、p-NF-κB、PI3K、AKT、NF-κB、β-Actin 江苏亲科生物研究中心有限公司。
LDF0200超净工作台 意大利Euroclone Bioair公司;371 CO2培养箱 美国Thermo Fisher Scientific有限公司;OLYMPUS CKX53光学显微镜、M491EON1微孔板酶标仪 美国伯腾仪器有限公司;细胞计数板 德国Marienfeld公司;VWB-9恒温水浴箱 天津泰斯特仪器有限公司;ALLEGRAX-15R超高速离心机 美国贝克曼库尔特有限公司;MX-S涡旋振荡器 德国Janke & Kunkel公司;FMB50制冰机 日本Sanyo有限公司;REVOLVE正倒置一体显微镜 美国ECHO公司;CLX-2464凝胶成像仪 美国Protein Simple公司;Mini-p4双垂直平板电泳仪、Mini-p4双垂直平板转模仪 美国BIO-RAD公司;DHG-9053A恒温干燥箱 天冠仪器仪表有限公司;2100生物分析仪 Agilent。
1.2 实验方法
1.2.1 细胞培养和处理
将HEP3B在37 ℃水浴锅中解冻,于37 ℃、5% CO2培养箱内培育,至细胞的融合度达到百分之九十进行铺板。分为对照组(空白培养液,CY)及给药组(含有50 ng/mL OSW-1的培养液,ZC),当细胞密度达到60%~70%时,给予药物处理24 h后,每孔加入1 mL TRNzol并在冰上提取细胞总RNA。提取的RNA样品送至上海天昊生物科技有限公司进行质量检测,包括双链cDNA的合成、转录组文库的构建以及样本的上机测序分析。
1.2.2 总RNA质量检测
共计2组细胞样品,分别为OSW-1给药组,空白对照组,各个组三个重复样本处理,规定RNA试样的含量不低于100 ng/µL,总量高于2 μg,OD260/280控制于1.8~2.2以内,而OD260/230保持不低于2,另外生物分析仪检测的RIN≥6.5,以保证下游高质量mRNA-seq文库的构建。
1.2.3 分选纯化mRNA及片段化
取适量总RNA分选mRNA,选择oligo-dT的磁珠特异性结合带有poly(A)结构的mRNA,给予两轮纯化处理,最大限度降低rRNA等与分选磁珠的非特异性结合,达到从总RNA中富集,纯化mRNA的效果[22]。
1.2.4 PCR扩增DNA文库
选择高保真聚合酶扩大文库,确保其总量。PCR扩增循环数控制在12~15之间。在保证产物足够的前提下,减少因扩增循环数过大而引入的bias。扩容后的文库在磁珠纯化下便成为可以上机的文库。
1.2.5 文库的质量检测
选择Qubit以及生物分析仪依次确定文库含量以及片段长度散布。规定其含量高于5 ng/μL,同时各个片段长度保持在300~400 bp范围内。
1.2.6 上机测序
选择Illumina高通量测序平台,按照2×150 bp双端测序的方式开展文库的高通量检测,继而得到FastQ结果[23]。
1.2.7 mRNA参考基因组比对
使用STAR软件将过滤后的reads与参照数据库进行比对,分析碱基的占比,在一定程度上能反映测序水平的高低、参选基因的好坏和后续分析结果的可靠性。采用Picard对STAR比对的结果进行统计,得到各个样本序列于编码区、非翻译区、内含子和基因间隔区域的分布情况,用于评估实验建库异常情况;正常情况下,外显子的测序序列定位占比最大,定位至内含子区域的测序序列或许因为不成熟的mRNA污染所致,而定位到注释不完全导致的,而定位到基因间隔区域的序列,可能是因为基因组注释不充分和背景噪音导致。
1.2.8 mRNA文库质量评估
表达情况有着明显不同的转录本,在有效检测时对数据量的需求不一样。高表达量基因测序期间得到很少的数据时即趋向饱和,低表达基因要求更大的数据量方可确保测得的结果精确。饱和度曲线能够反馈各个测序量情况下的基因表达检测的准确性。选择RSeQC应用就全部获得的参照基因予以随机抽样,基于抽样的read对转录本予以表达定量,对于丰度存在差异的转录本,按照RPKM结果得到六个层次,使抽样与最终的RPKM值小于15%。
1.2.9 MTT法检测细胞存活率
待HEP3B细胞培养生长至80%~90%,将其均匀铺至96孔板,各个孔的细胞数保持1×105个;设置对照组与给药组,每组设三个复孔。铺板24 h后,加入OSW-1(0、1、10、25、50、75、100 ng/mL)作用24 h,遮光下加入2.5 mg/mL MTT干预2 h,吸弃培养基,每孔加入100 μL DMSO,转移到酶标仪之中,490 nm波长条件下分析OD值结果。
1.2.10 细胞免疫荧光
细胞铺板给药处理结束后,4%多聚甲醛固定15 min,0.5%曲拉通透化10 min,5% BSA封闭60 min,孵育一抗4 ℃过夜,避光孵育荧光二抗1 h,加入DAPI及抗荧光淬灭封片液,用荧光显微镜观察拍照即可。
1.2.11 总蛋白提取及Western blot实验
细胞培养24 h后给予50 ng/mL OSW-1进行干预,药物处理结束后,制备蛋白质样品。采用BCA试剂盒检测蛋白浓度,筛选适度的蛋白样品予以聚丙酰胺凝胶电泳处理,恒压90 min,再转印到NC膜之中,恒流80 min,5%脱脂牛奶或5% BSA封闭1.5 h,PBST清洗三次,将膜在4 ℃条件摇床上缓慢孵育一抗过夜。取出后PBST清洗三次,清洗完毕后,将其浸入二抗工作液中1.5 h。再次PBST进行清洗,清洗3次后显像。
1.3 数据处理
利用 GraphPad Prism 8软件进行数据处理和图片制作,利用Student t检验和单因素方差分析对各处理组进行统计分析。
2. 结果与分析
2.1 OSW-1对HEP3B的抗肿瘤作用
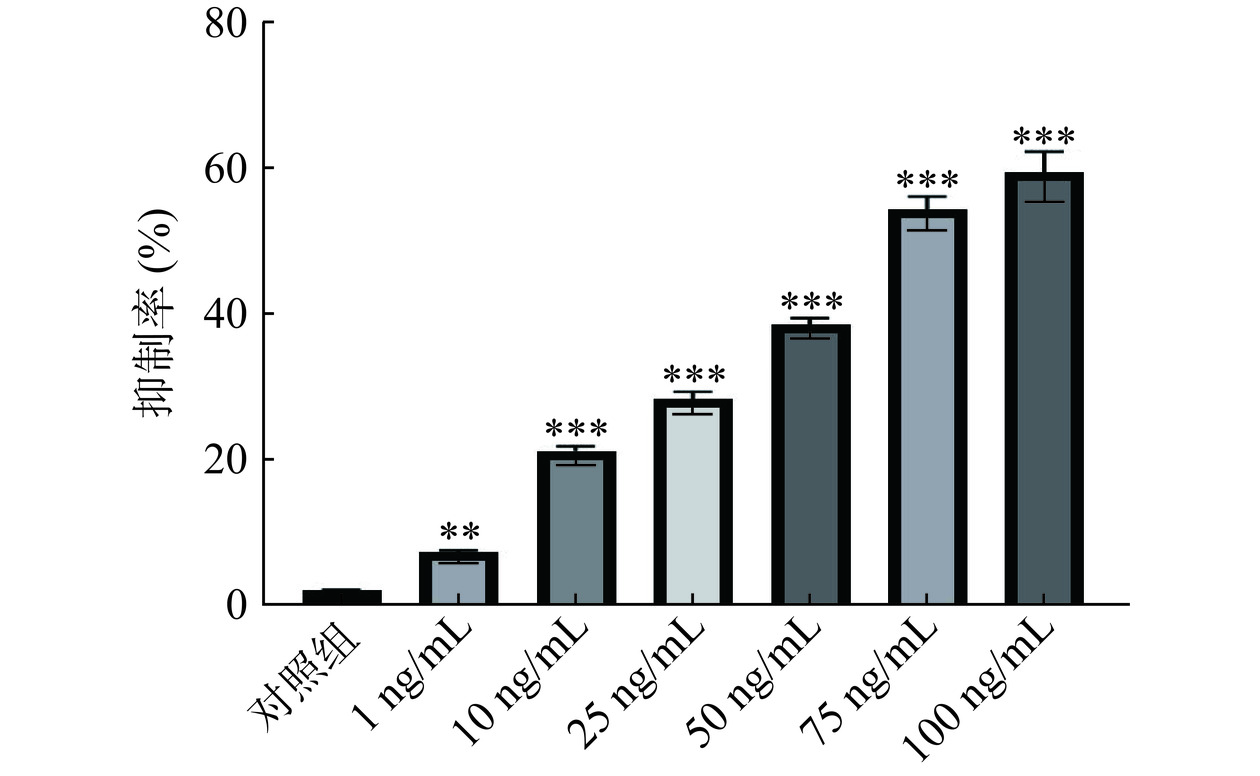
OSW-1是虎眼万年青中天然的有效抗肿瘤成分,前期研究发现OSW-1可用于治疗肝细胞癌,但具体的调控机制尚不明确[16],本研究采用MTT法检测OSW-1作用于HEP3B后的细胞存活率。MTT结果如图1所示,OSW-1对HEP3B细胞具有较强的抗增殖作用,与对照组比较,1、10、25、50、75、100 ng/mL的OSW-1给药组HEP3B细胞抑制率显著增加(P<0.001),得到IC50值为69.41 ng/mL,后续实验OSW-1给药浓度选择50 ng/mL。
2.2 原始测序数据质量评估
图2A结果表明送检样品的Clean reads rate均大于98%。图2B可以看出所有样本测序质量Q30值均大于95%;图2C显示测序数据在基因组各个区域的分布:使用STAR软件将过滤后的reads与参照数据库进行比对,采用Picard对STAR比对的结果进行统计,结果示匹配到外显子区域的测序序列定位的百分比含量最高,表明本次测序送检样品质检合格,可以进行后续转录组测序及分析实验。
2.3 基因表达分析
满足P<0.05且|log2(Fold change)|>1为差异基因,其中log2(Fold change)>1为上调基因(Up);log2(Fold change)<−1为下调基因(Down),本次测序获得的1381个差异表达基因中(图3A~图3B),上、下调基因分别为844个和537个。基于全部基因的FPKM分布情况就不同分组样品基因表达情况予以对比。而同一条件下的重复样本,最后的FPKM则是全部重复样本均数的均值(图3C)。
2.4 差异表达基因GO功能分析
将本研究中CY组、ZC组的1381个差异表达基因比对。发现相关的GO条目共1034个(P<0.05)(图4),结果发现OSW-1作用于HEP3B细胞的生物学过程主要与受体配体活性、细胞因子活性、有机阴离子跨膜转运活性等有关;分子功能主要与细胞外基质、含胶原蛋白的细胞外基质、内质网管腔等有关;分子组成主要与轴突发展、有机阴离子运输、轴突生成等有关。
2.5 差异表达基因KEGG Pathway显著性富集分析
持续性炎症通常为疾病发展过程中对肝损伤的适应性反应,进而导致肝纤维化、肝硬化,最终导致HCC[24−25]。慢性炎症是已知的并影响致癌的所有阶段,靶向炎症在肿瘤微环境中已被证明可显着降低恶性肿瘤的发展、生长和扩散[26−27]。依据KEGG分析得出,差异表达基因大部分集中于人体免疫、炎症发生和代谢等相关通路(图5),如补体和凝血级联、TNF信号通路、视黄醇新陈代谢、药物代谢细胞色素P450等信号通路。因此针对TNF信号通路展开后续实验研究。
2.6 HEP3B中p-PI3K、p-AKT、p-NF-κB的免疫荧光染色
通过本次转录组测序结果,本研究选取了炎症相关通路(TNF信号通路),同时从基因组层面筛选出OSW-1抑制HEP3B细胞系增殖的关键候选基因p-PI3K、p-AKT、p-NF-κB,并对上述选择的TNF信号通路中核心基因进行MTT法、免疫荧光及Western Blot等实验进行验证。
通过免疫荧光检测蛋白的表达,经OSW-1给药处理HEP3B细胞后,细胞中的p-PI3K、p-AKT、p-NF-κB荧光强度较对照组显著减弱。如图6结果表明,给药后PI3K、AKT、NF-κB磷酸化水平显著降低。
2.7 检测HEP3B中p-PI3K、p-AKT、p-NF-κB蛋白表达水平
NF-κB信号通路的异常激活已在包括HCC在内的多种癌症中得到证实[28−30]。NF-κB为典型的转录调节因子,在细胞增殖以及免疫应答方面有着关键作用[31]。研究表明,NF-κB信号级联持续活跃,可以引起持续的炎症以促进癌变[32]。通过Western blot结果显示,给药组p-PI3K、p-AKT、p-NF-κB蛋白表达相较于对照组显著降低;PI3K、AKT、NF-κB蛋白表达水平未见明显变化(图7)。表明OWS-1可能通过减少p-PI3K、p-AKT、p-NF-κB蛋白表达,进而促进HEP3B细胞的死亡。这与已有研究OSW-1可以抑制肝癌细胞生长[33]的结果一致。
3. 结论
本研究基于转录组测序分析,探讨OSW-1对肝细胞癌的治疗作用。经Illumina高通量测序平台分析,表明OSW-1作用于HEP3B细胞后主要与TNF和NF-κB等炎症信号通路有关,而NF-κB作为炎症信号的核心靶点,在介导炎症反应中发挥重要作用。通过MTT实验,发现OSW-1可以明显抑制肝癌细胞的存活。进一步研究表明,OSW-1可通过下调炎症反应核心蛋白p-PI3K、p-AKT、p-NF-κB蛋白的表达,减少炎症的发生。表明OSW-1可能通过抑制肝细胞癌中p-NF-κB的表达,从而抑制肝细胞癌的增值,本项实验结果均证明OSW-1具有较强的抗HCC作用,有望成为有效治疗肝细胞癌的潜在药物。
本次研究只在细胞层面上验证了OSW-1的抗癌作用,未在体内进一步证明OSW-1对实体瘤的有效性,在后续的研究中仍需进行体内实验验证OSW-1的抗肿瘤作用。
-
-
[1] DENG S, SOLINAS A, CALVISI D F. Cabozantinib for HCC treatment, from clinical back to experimental models[J]. Front Oncol,2021,13(11):756672.
[2] BANG A, DAWSON L A. Radiotherapy for HCC:Ready for prime time?[J]. JHEP Rep,2019,1(2):131−137. doi: 10.1016/j.jhepr.2019.05.004
[3] YOU M J, GAO Y N, FU J L, et al. Epigenetic regulation of HBV-specific tumor-infiltrating T cells in HBV-related HCC[J]. Hepatology,2023,78(3):943−958. doi: 10.1097/HEP.0000000000000369
[4] WANG W Y, WEI C. Advances in the early diagnosis of hepatocellular carcinoma[J]. Genes Dis,2020,7(3):308−319. doi: 10.1016/j.gendis.2020.01.014
[5] HU B, XU Y, LI Y C, et al. CD13 promotes hepatocellular carcinogenesis and sorafenib resistance by activating HDAC5-LSD1-NF-κB oncogenic signaling[J]. Clin Transl Med,2020,10(8):e233. doi: 10.1002/ctm2.233
[6] SHI R, LIU Z R. RPL15 promotes hepatocellular carcinoma progression via regulation of RPs-MDM2-p53 signaling pathway[J]. Cancer Cell Int,2022,22(1):150. doi: 10.1186/s12935-022-02555-5
[7] ZHANG X, HU B, SUN Y F, et al. Arsenic trioxide induces differentiation of cancer stem cells in hepatocellular carcinoma through inhibition of LIF/JAK1/STAT3 and NF-κB signaling pathways synergistically[J]. Clin Transl Med,2021,11(2):e335. doi: 10.1002/ctm2.335
[8] 齐英姿, 邓晨, 苏纳, 等. 肝癌细胞系Hep3B的泛素化蛋白质组学[J]. 生物工程学报,2016,32(10):1443−1454. [QI Y Z, DENG C, SU N, et al. Ubiquitination proteomics of hepatocellular carcinoma cell line Hep3B[J]. Chinese Journal of Biological Engineering,2016,32(10):1443−1454.] QI Y Z, DENG C, SU N, et al. Ubiquitination proteomics of hepatocellular carcinoma cell line Hep3B[J]. Chinese Journal of Biological Engineering, 2016, 32(10): 1443−1454.
[9] ZHENG G, XIE Z Y, WANG P, et al. Recent advances of single-cell RNA sequencing technology in mesenchymal stem cell research[J]. World J Stem Cells,2020,12(6):438−447. doi: 10.4252/wjsc.v12.i6.438
[10] LAWSON D A, KESSENBROCK K, DAVIS R T, et al. Tumour heterogeneity and metastasis at single-cell resolution[J]. Nat Cell Biol,2018,20(12):1349−1360. doi: 10.1038/s41556-018-0236-7
[11] LOWE R, SHIRLEY N, BLEACKLEY M, et al. Transcriptomics technologies[J]. PLoS Comput Biol,2017,13(5):e1005457. doi: 10.1371/journal.pcbi.1005457
[12] 王瑜. 虎眼万年青对人非小细胞肺癌H1299细胞增殖与凋亡的影响及机制研究[D]. 延吉:延边大学, 2018. [WANG Y. Effect and mechanism of tigereye Dieffonia on proliferation and apoptosis of human non-small cell lung cancer H1299 cells[D]. Yanji:Yanbian University, 2018.] WANG Y. Effect and mechanism of tigereye Dieffonia on proliferation and apoptosis of human non-small cell lung cancer H1299 cells[D]. Yanji: Yanbian University, 2018.
[13] ZHAN Z X, LIU Z Q, LAI J C, et al. Anticancer effects and mechanisms of OSW-1 isolated from Ornithogalum saundersiae:A review[J]. Front Oncol,2021,11:747718. doi: 10.3389/fonc.2021.747718
[14] 郭小宇. 长白多点发力推动县域经济发展[N]. 吉林农村报, 2022. [GUO X Y. Changbai makes more efforts to promote county economy[N]. Jilin Rural News, 2022.] GUO X Y. Changbai makes more efforts to promote county economy[N]. Jilin Rural News, 2022.
[15] 詹志鑫. OSW-1抗胶质瘤作用及其机制的研究:基于网络药理学分析和实验验证[D]. 长春:吉林大学, 2023. [ZHAN Z X. Effect of OSW-1 on glioma and its mechanism:Based on network pharmacological analysis and experimental verification[D]. Changchun:Jilin University, 2023.] ZHAN Z X. Effect of OSW-1 on glioma and its mechanism: Based on network pharmacological analysis and experimental verification[D]. Changchun: Jilin University, 2023.
[16] 刘哲. 虎眼万年青总皂苷对结肠癌细胞自噬及凋亡的影响及相关机制研究[D]. 大连:大连医科大学, 2019. [LIU Z. Effects of total saponins of Diaenopsis Tigris on autophagy and apoptosis of colon cancer cells and related mechanisms[D]. Dalian:Dalian Medical University, 2019.] LIU Z. Effects of total saponins of Diaenopsis Tigris on autophagy and apoptosis of colon cancer cells and related mechanisms[D]. Dalian: Dalian Medical University, 2019.
[17] ZHOU Y, GARCIA-PRIETO C, CARNEY D A, et al. OSW-1:A natural compound with potent anticancer activity and a novel mechanism of action[J]. J Natl Cancer Inst,2005,97(23):1781−1785. doi: 10.1093/jnci/dji404
[18] JIN J C, JIN X L, QINA C S, et al. Signaling network of OSW-1-induced apoptosis and necroptosis in hepatocellular carcinoma[J]. Mol Med Rep,2013,7(5):1646−1650. doi: 10.3892/mmr.2013.1366
[19] ZHANG Y H, FANG F Q, FAN K, et al. Effective cytotoxic activity of OSW-1 on colon cancer by inducing apoptosis in vitro and in vivo[J]. Oncol Rep,2017,37(6):3509−3519. doi: 10.3892/or.2017.5582
[20] 千昌石. 虎眼万年青总皂苷防治肝癌作用的初步实验研究[D]. 延吉:延边大学, 2011. [QIAN C S. Preliminary experimental study on the prevention and treatment of hepatocellular carcinoma by total saponins of Dirhizoba tigerum[D]. Yanji:Yanbian University, 2011.] QIAN C S. Preliminary experimental study on the prevention and treatment of hepatocellular carcinoma by total saponins of Dirhizoba tigerum[D]. Yanji: Yanbian University, 2011.
[21] DING X R, LI Y M, LI J, et al. OSW-1 inhibits tumor growth and metastasis by NFATc2 on triple-negative breast cancer[J]. Cancer Med,2020,9(15):5558−5569. doi: 10.1002/cam4.3196
[22] DU G Z, YU M M, XU Q Q, et al. Hypomethylation of PRDM1 is associated with recurrent pregnancy loss[J]. J Cell Mol Med,2020,24(12):7072−7077. doi: 10.1111/jcmm.15335
[23] HUANG Z Y, DU G Z, HUANG X M, et al. The enhancer RNA lnc-SLC4A1-1 epigenetically regulates unexplained recurrent pregnancy loss (URPL) by activating CXCL8 and NF-κB pathway[J]. E Bio Medicine,2018,38:162−170.
[24] SRIVASTAVA A, SHARMA H, KHANNA S, et al. Interleukin-6 induced proliferation is attenuated by transforming growth Factor-β-Induced signaling in human hepatocellular carcinoma cells[J]. Front Oncol,2022,11:811941. doi: 10.3389/fonc.2021.811941
[25] CHAKRABORTY E, SARKAR D. Emerging therapies for hepatocellular carcinoma (HCC)[J]. Cancers (Basel),2022,14(11):2798. doi: 10.3390/cancers14112798
[26] ANNAND J R, HENDERSON A R, COLE K S, et al. Gibberellin JRA-003:A selective inhibitor of nuclear translocation of IKKα[J]. ACS Med Chem Lett,2020,11(10):1913−1918. doi: 10.1021/acsmedchemlett.9b00613
[27] CHEN C, WANG Z H, DING Y, et al. Tumor microenvironment-mediated immune evasion in hepatocellular carcinoma[J]. Front Immunol,2023,14:1133308. doi: 10.3389/fimmu.2023.1133308
[28] HAN H X, LIN T, WANG Z Y, et al. RNA-binding motif 4 promotes angiogenesis in HCC by selectively activating VEGF-A expression[J]. Pharmacol Res,2023,187:106593. doi: 10.1016/j.phrs.2022.106593
[29] YU H, LIN L B, ZHANG Z Q, et al. Targeting NF-κB pathway for the therapy of diseases:mechanism and clinical study[J]. Signal Transduct Target Ther,2020,5(1):209. doi: 10.1038/s41392-020-00312-6
[30] LI X H, SHANG D H, SHEN H L, et al. ZSCAN16 promotes proliferation, migration and invasion of bladder cancer via regulating NF-κB, AKT, mTOR, P38 and other genes[J]. Biomed Pharmacother,2020,126:110066. doi: 10.1016/j.biopha.2020.110066
[31] JOMEN W, OHTAKE T, AKITA T, et al. Iron chelator deferasirox inhibits NF-κB activity in hepatoma cells and changes sorafenib-induced programmed cell deaths[J]. Biomed Pharmacother,2022,153:113363. doi: 10.1016/j.biopha.2022.113363
[32] ELBAKRY M M M, ELBAKARY N M, HAGAG S A, et al. Pomegranate peel extract sensitizes hepatocellular carcinoma cells to ionizing radiation, induces apoptosis and inhibits MAPK, JAK/STAT3, β-catenin/NOTCH, and SOCS3 signaling[J]. Integr Cancer Ther, 2023, 22:15347354221151021.
[33] 张晓威, 李娜, 金吉春, 等. OSW-1与线粒体DNA缺失对肝癌细胞PI3K信号通路的影响[J]. 吉林医学,2016,37(8):1849−1852. [ZHANG X W, LI N, JIN J C, et al. Effects of OSW-1 and mitochondrial DNA deletion on PI3K signaling pathway of hepatocellular carcinoma cells[J]. Jilin Medical Science,2016,37(8):1849−1852.] ZHANG X W, LI N, JIN J C, et al. Effects of OSW-1 and mitochondrial DNA deletion on PI3K signaling pathway of hepatocellular carcinoma cells[J]. Jilin Medical Science, 2016, 37(8): 1849−1852.





 下载:
下载:






 下载:
下载:
