Enhanced Fatty Acid Production by Addition of Exogenous Oil in Mucor circinelloides
-
摘要: 卷枝毛霉(Mucor circinelloides)可利用多种碳源实现脂质积累,不同的碳源对其脂质积累的影响不同。在不改变其它发酵培养条件和碳氮比的情况下,以100%葡萄糖为对照,添加不同比例的外源油脂(大豆油)作为另一种碳源,对其细胞生长和脂质生成的影响进行了研究。采用氯仿-甲醇法提取脂质,通过气相色谱技术(gas chromatography,GC)测定其脂肪酸组成及含量。同时,采用实时荧光定量PCR法检测了与脂肪酸合成相关的脱饱和酶基因在菌株中的表达情况。结果表明:碳氮比不变的情况下,最佳碳源混合比例为葡萄糖35 g/L,大豆油24.3 g/L,该培养基中生长的卷枝毛霉的生物量、脂质含量和脂质产量在发酵前期迅速增长,在发酵后期的增长趋势逐渐平缓,在发酵72 h之后略有下降,其最高生物量、脂质含量和产量分别为19.60 g/L、42.62%和8.35 g/L,而对照组(以葡萄糖为单一碳源)仅为14.72 g/L、34.41%和5.06 g/L。与对照组相比,经混合碳源培养的卷枝毛霉的生物量、脂质含量和产量分别提高了33.15%、23.8%和65.10%,且可以将大豆油中的α-亚麻酸(α-Linolenic acid,ALA)吸收并储存在细胞内,同时,其生物体内△12脱饱和酶的表达量显著(P<0.05) 上升,而△9和△6脱饱和酶的表达量显著(P<0.05)下降,这解释了脂肪酸含量的变化,并为进一步探究其他外源油脂对卷枝毛霉产脂的影响奠定了基础。Abstract: Mucor circinelloides has the ability to use a wide range of carbon sources to accumulate lipids. The different carbon sources have significantly influenced the total lipids through different metabolic pathways in oleaginous organisms. In the present study, the effects of exogenous oil (soybean oil) at different concentrations as an alternative carbon source on its fungal growth and lipid accumulation were investigated without changing fermentation culture conditions and the original C/N ratio, while using 100% glucose as a control. Total lipids and their fatty acid composition were determined by gas chromatography (GC). Moreover, the expression levels of desaturases genes involved in fatty acid biosynthesis were investigated in the studied strains using real-time fluorescence quantitative PCR. The results showed that a concentration of 35 g/L of glucose mixed with 24.3 g/L of soybean oil were the optimal carbon sources with constant carbon to nitrogen ratio. The biomass, lipid content and lipid yield of M. circinelloides grown in this medium increased rapidly in the early stage of fermentation, and the growth trend gradually slowed down in the late stage of fermentation, decreasing slightly after 72 h of fermentation. It was found that the highest biomass, total lipids, and lipid yields were significantly increased at 19.60 g/L, 42.62%, and 8.35 g/L (33.15%, 23.8%, and 65.10%), respectively. In contrast, the control group (those cultured on glucose as a single carbon source) was only 14.72 g/L, 34.41%, and 5.06 g/L, respectively. The critical step was in which α-linolenic acid (ALA) was stored from the exogenous oil in fungal cells supplying enough soybean oil with mixed substrates for fatty acids synthesis. The overexpression of the △12-desaturase gene in WJ11 significantly (P<0.05) increased, while the overexpression of △9- and △6-desaturases genes was significantly (P<0.05) decreased. This study could provide important insights for further investigation of the effect of other exogenous oils on lipid production by M. circinelloide and other oleaginous fungi.
-
某些微生物具有将外部碳源转化为脂质的能力,可用于生产必需脂肪酸和生物柴油[1-3],这些能够广泛利用各种类型碳源物质的微生物被称为产油微生物。产油微生物(Oleaginous microorganisms)在合适的培养条件(碳源丰富,N源缺乏)下,由于营养元素N源的限制,细胞生长到一定程度不再生长,将过量的碳源转化为甘油三酯(Triacylglycerol, TAG),并在细胞内储存起来,能积累超过20%的细胞油脂[4-6](w/w,细胞干重)。相应地,所产的油脂称为微生物油脂[7](Microbial oil)。微生物油脂通常被认为是一种代替动物脂肪和植物油的油脂来源,与传统动植物油脂相比,微生物油脂有众多优势:产油量高,生长周期短,不受气候影响,不占用耕地,原料来源丰富,且可以合成多种不饱和脂肪酸如GLA、ARA、EPA和DHA等。
产油微生物能够利用低廉的植物油等来生产高价值的不饱和脂肪酸[8],因此,利用产油微生物进行功能性油脂的生产越来越受到人们的关注,产油微生物生产并积累油脂的要素是高碳氮比[9-10],当微生物将葡萄糖作为碳源进行发酵时,细胞内的脂质合成主要是从头合成[11-14],即经过糖酵解途径生成丙酮酸,再进入柠檬酸循环[15-16],当氮源耗尽后,腺苷一磷酸(Adenosine 3' -mono- phosphate,AMP)含量降低[17],三羧酸循环(Tricarboxylic acid cycle,TCA cycle)受阻,导致线粒体中柠檬酸积累[16,18],此时胞内蛋白质、核酸等大分子的合成趋于停止,菌体不再生长,积累的柠檬酸被转运到细胞质中被ATP[17](Adenosine Triphosphate)依赖型柠檬酸裂解酶裂解为草酰乙酸和乙酰-CoA,再进入脂肪酸及TAG合成[19],从而引起胞内脂质大量积累。但是,当产油微生物利用其它脂类物质作为碳源发酵时,其胞内脂质合成采用非从头合成途径。至今,对产油真菌利用脂类碳源生长和积累脂质还缺乏系统的研究。
产油真菌卷枝毛霉,因能够产生人体必需脂肪酸—γ-亚麻酸(C18:3,γ-Linolenic acid,GLA)[16],其重要性受到脂类生物技术行业的广泛关注[6],是一种具有巨大潜力的油脂微生物资源,并且卷枝毛霉已经成为研究丝状真菌脂质积累机制的模式生物[19]。目前,对产油丝状真菌利用外源油作为碳源的研究相对较少。本研究利用外源油脂(大豆油)与葡萄糖作为混合碳源代替单一碳源(葡萄糖)对卷枝毛霉进行发酵优化,并分析其生长情况、脂质产量及其脂肪酸组分,旨在为后续进一步研究卷枝毛霉高效利用碳源合成高附加值多不饱和脂肪酸奠定基础,也为定向改造产油真菌卷枝毛霉合成特定脂肪酸提供了参考。
1. 材料与方法
1.1 材料与仪器
卷枝毛霉WJ11(Mucor circinelloides WJ11) 由本实验室保藏[20];大豆油 食品级,金龙鱼粮油食品股份有限公司;C15:0脂肪酸标品 色谱纯,Sigma公司;酵母浸粉、酒石酸铵等其他试剂 分析纯,国药集团化学试剂有限公司;吐温80 化学纯,国药集团化学试剂有限公司;正己烷 色谱纯,格里斯医药化学技术有限公司;Total RNA Extractor(Trizol) 生工生物工程(上海)股份有限公司;Evo M-MLV 反转录预混型试剂盒、SYBR pro Taq HS Premix试剂盒 Takara公司。
AD500S-H高速分散均质机 上海新勒机电科技有限公司;ZWYR-C211D摇床(恒温培养振荡器) 上海智城分析仪器制造有限公司;葡萄糖氧化酶电极生物传感器 山东省科学院生物研究所;LightCycler 96实时荧光定量PCR仪 上海罗氏制药有限公司;Agilent 7890B气相色谱仪 安捷伦科技有限公司;Labconco-6L真空冷冻干燥机 美国LABCONCO公司;布氏过滤器 山东雨燊生物科技有限公司。
1.2 实验方法
1.2.1 培养基
活化培养基为YPG(Yeast Extract-Peptone-Glucos)(pH4.5),参照Zhao等[16]方法配制,种子培养基为Kendrick & Ratledge(K&R)培养基[17,21],成分为:葡萄糖 30 g/L,MgSO4·7H2O 1.5 g/L,酒石酸铵 3.3 g/L,KH2PO4 7 g/L,Na2HPO4 2 g/L,酵母抽提物 1.5 g/L,CaCl2·2H2O 0.1 g/L,FeCl3·6H2O 8 mg/L,Co(NO3)2·6H2O 0.1 mg/L,ZnSO4·7H2O 1 mg/L,CuSO4·5H2O 0.1 mg/L, MnSO4·5H2O 0.1 mg/L。发酵培养基为改良K&R培养基[20]:葡萄糖,80 g/L;酒石酸铵,2 g/L;其他成分与种子培养基相同。混合发酵培养基使用大豆油作为另一碳源,使用前利用乳化剂吐温80(乳化剂的添加量为2%)进行乳化均质,均质条件为10000 r/min,持续5min,形成乳浊液,并按照表1进行配制,以单一碳源(葡萄糖)作为对照组,其他四组作为实验组进行发酵实验。培养基使用前均需对其进行高温灭菌,于121 ℃高压蒸汽下灭菌20 min。
表 1 葡萄糖-大豆油混合培养基的配方Table 1. Formulation of glucose-soybean oil mixed medium组数 葡萄糖(g/L) 大豆油(g/L) 1 80(100.00%) 0(0) 2 40(50.00%) 21.6(50.00%) 3 35(43.75%) 24.3(56.25%) 4 30(37.50%) 27.0(62.50%) 5 25(31.25%) 29.7(68.75%) 注:括号内为葡萄糖或大豆油在培养基中所占的比例。 1.2.2 培养方法
平板培养:取出保存的菌种(Mucor circinelloides WJ11),经划线接种到YPG(pH4.5)平板上,在28 ℃恒温培养箱培养3~4 d。用无菌水收集孢子并进行计数,将孢子浓度稀释到数量级为1.0×107个/mL,并置于4 ℃冰箱以备使用。种子培养:取100 µL孢子悬浮液(1.0×107个/mL)接种到装有100 mL种子培养基的1 L带挡板的玻璃瓶中,在28 ℃、130 r/min的条件下摇床培养24 h。 发酵培养:按10%(v/v)的接种量将10 mL的种子培养液接种到装有100 mL发酵培养基的1 L带挡板的锥形瓶中,在28 ℃、130 r/min条件下发酵96 h,在发酵的12、24、36、48、72、96 h取样。
1.2.3 生物量的测定
发酵液经取样点取样后通过布氏过滤器过滤至滤纸上,收集滤液和菌体,用0.9%生理盐水冲洗四遍,将滤纸放入提前称重的离心管中,随后对装有过滤菌体的离心管冷冻干燥48 h并称重,利用差重法[16,20,22]计算细胞干重。计算细胞干重和细胞干重(不包含脂质)公式如下:
(1) (2) 式中:m1为空离心管和滤纸的重量,g;m2为冻干后带有滤纸的菌体管重量,g;v为取样体积,mL;m3为脂质产量(计算公式见公式5),g/L。
1.2.4 发酵液中葡萄糖和大豆油浓度的测定
取12、24、36、48、72、96 h的发酵液进行葡萄糖和残油的测定,用葡萄糖氧化酶电极生物传感器对上清液中葡萄糖的剩余量进行测定;采用萃取法[23]将残油(包括上清液和生理盐水的洗脱液中的油)分离,然后参考Tang等[20]的方法进行脂肪酸含量的测定;根据其剩余量计算其消耗速率,公式如下:
(3) 式中:ΔC为发酵时间内消耗的葡萄糖或大豆油,g/L;t为发酵时间,h。
1.2.5 总脂肪酸的提取
采用氯仿-甲醇方法[23]对冻干菌体进行油脂提取,具体步骤如下:称取10 mg左右已冻干的菌丝体于5 mL提脂瓶中,加入2 mL 4 mol/L的盐酸;80 ℃水浴3~5 h,期间每隔30 min漩涡震荡一次;取出提脂瓶冷却降温,用微量进样器加入100 μL的十五烷酸(浓度0.2004 g/100 mL)为内标,加入体积比为2:1的氯仿(2 mL)和甲醇(1 mL)充分混匀15~20 min进行萃取;在离心机中离心5 min(3000 r/min),收集下层(氯仿层)转移至新的提脂瓶中并氮气吹干;加入1 mL 10%的硫酸甲醇溶液进行甲酯化,60 ℃水浴3~5 h,期间每隔30 min漩涡震荡一次;取出提脂瓶冷却降温后,加入2 mL正己烷和1 mL饱和食盐水,充分混匀15~20 min,在离心机中离心5 min;吸取上层正己烷层的脂肪酸甲酯溶液转移至气相瓶,随后进行GC检测。
1.2.6 总脂肪酸的含量及组成的测定
采用高效气相色谱法进行脂肪酸的测定,气相色谱条件为:不分流进样,氢离子火焰监测器,色谱柱是DB-WAXcolumn,载气为氮气,气化室温度和检测器温度均为250 ℃,进样量为1 μL。色谱柱升温程序:设定进样器初始温度80 ℃,先以8 ℃/min的升温速率升至200 ℃,再以1 ℃/min的升温速率升至205 ℃,最后以4 ℃/min的升温速率升至240 ℃,保持5 min。卷枝毛霉积累的脂肪酸种类根据气相色谱图中的出峰时间和出峰面积进行判定,之后使用内标法计算卷枝毛霉的脂肪酸含量,以十五烷酸(C15:0)为内标,每种脂肪酸的峰面积为A,总脂肪酸含量和脂质产量的计算公式如下:
(4) (5) 式中:A总为所有脂肪酸的面积总和;A内标为内标的面积;C内标为内标浓度,g/mL;V内标为内标的体积,mL;m称重为实验菌体的重量,mg。
1.2.7 卷枝毛霉脱饱和过程中相关基因转录水平的测定
本实验所用到基因信息如表2所示。总RNA的提取:用Trizol法[16]提取卷枝毛霉WJ11的基因组总RNA。反转录:使用Takara公司Evo M-MLV反转录预混型试剂盒将卷枝毛霉WJ11的RNA反转录得到cDNA,操作步骤参考试剂盒说明书。 实时荧光定量PCR:实时荧光定量PCR(RT-qPCR)使用Takara公司的SYBR pro Taq HS Premix试剂盒进行荧光定量,步骤参考试剂盒说明书。将卷枝毛霉的β-actin rRNA作为内参基因,以单一碳源(葡萄糖)培养菌株的脱饱和酶基因的mRNA表达量作为1,根据2−ΔΔCt法分析以最佳混合碳源培养基上生长的卷枝毛霉的脱饱和酶基因的相对表达水平。所用到的引物序列如表3所示,由上海生工生物工程股份有限公司合成。
表 2 卷枝毛霉WJ11中Δ9、Δ12和Δ6脱饱和酶基因信息Table 2. Gene information of Δ9-, Δ12- and Δ6-desaturases in M. circinelloides WJ11基因名称 染色体上的位置 基因大小 脱饱和
酶基因scaffold00005.3 scaffold00005: 15315- 16821(+) 1506 Δ9-1 scaffold00126.19 scaffold00126: 56635- 58330(+) 1696 Δ9-2 scaffold00248.11 scaffold00248: 28862-30077(−) 1215 Δ12 scaffold00003.2 scaffold00003: 11655-13376(−) 1722 Δ6-1 scaffold00010.52 scaffold00010: 159563-161134(+) 1572 Δ6-2 表 3 实时荧光定量 PCR 所用的特异性引物Table 3. Details of specific primer pairs used in RT-qPCR引物名称 序列5'-3' rt-D9-1-F ATGCTCCTTATTACCTGCGCCGAC rt-D9-1-R CAATAAGCTTTAAGCCTAGAGTTTAA rt-D9-2-F ATGTCAACTACAACGACAACTA rt-D9-2-R AACCTGAGAAGAACAAGACCAAGTAA rt-D6-1-F CCTTGTCATGGTGGAAGAACAAGC rt-D6-1-R CGGCAATGAAACGGGATAACATGG rt-D6-2-F GCAGAGACGCTACAGATGTCTTTC rt-D6-2-R CGAATTTCTTGAGCAAAAGCAGCAG rt-D12-F CAGGTCTTTGTCCCCTCTACTCG rt-D12-R ATCTTGACCAGAGACATTGGTG β-actin-F GATGAAGCCCAATCCAAGA β-actin-R TTCTCACGGTTGGACTTGG 1.3 数据处理
采用SPSS 21.0软件进行统计分析。所有实验分为三个独立重复。数据以Mean±SD表示。采用Student's t检验来评价均值之间的差异,P<0.05为显著差异。
2. 结果与分析
2.1 不同比例的葡萄糖-大豆油混合培养基对卷枝毛霉WJ11细胞生长的影响
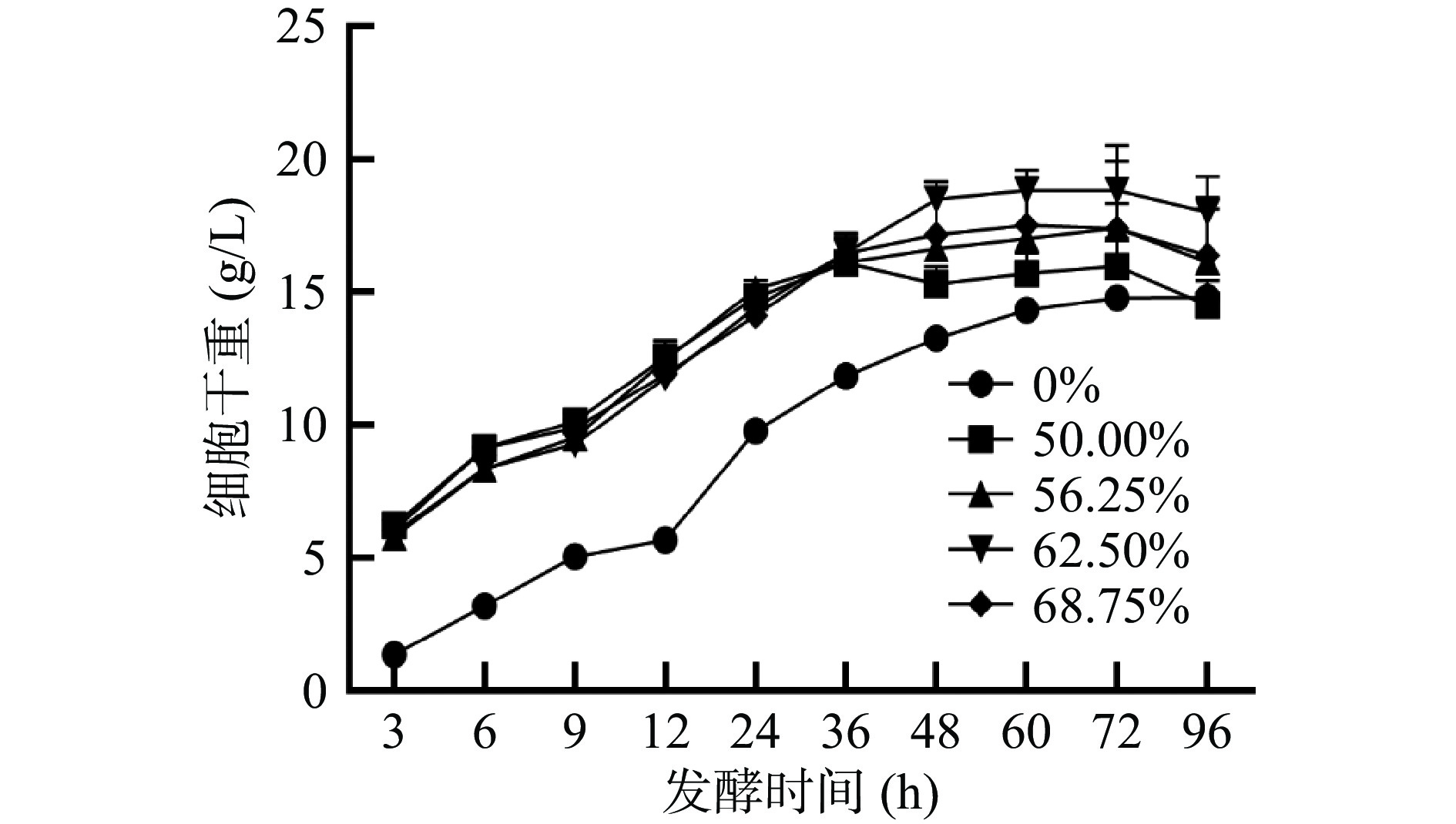
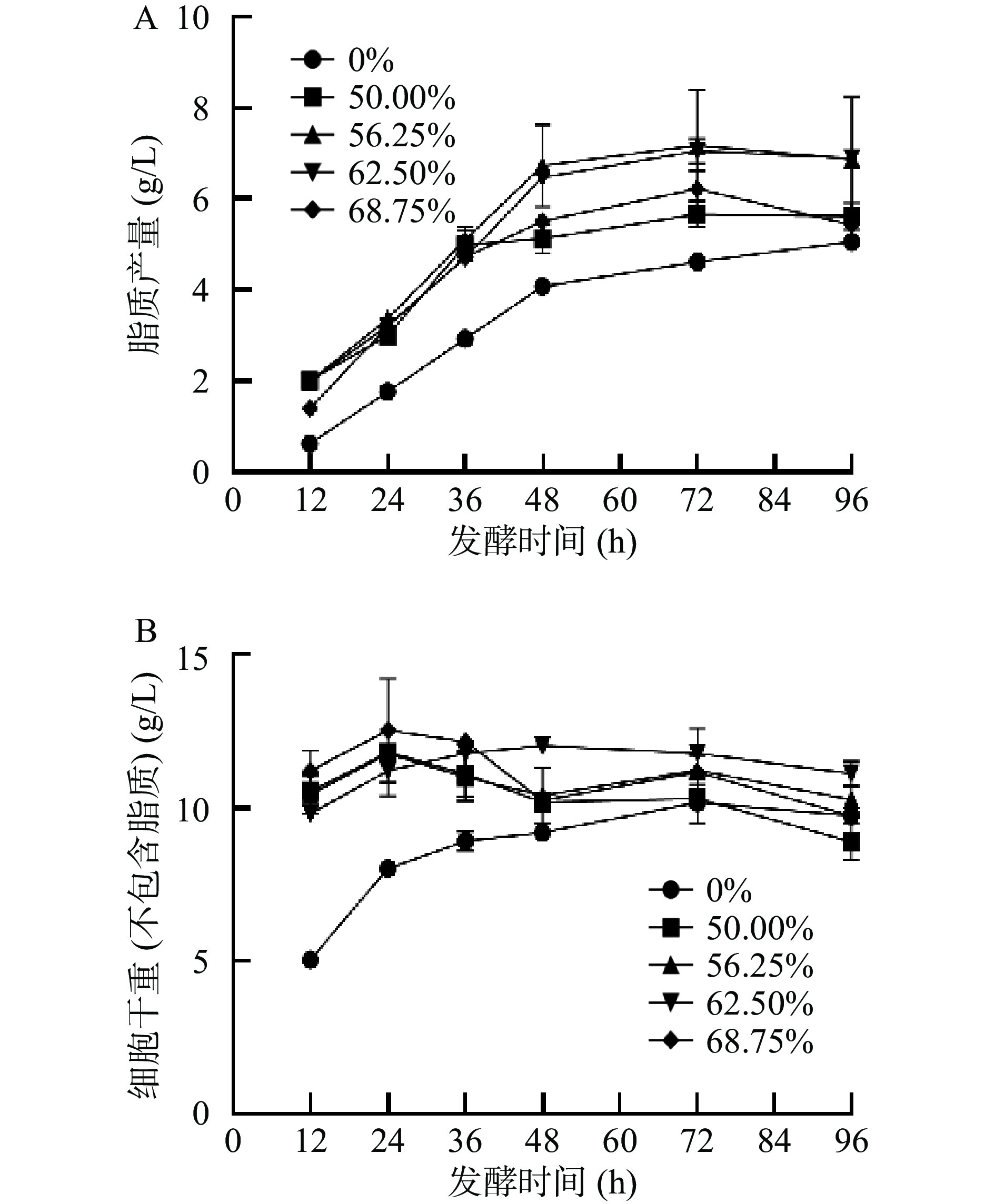
产油真菌可以从培养基中吸收碳源,通过脂质合成[11]等途径将其转化成脂肪酸,并在细胞体内积累油脂。早期研究表明,当培养基中含有外源油脂时,产油真菌可以直接吸收培养基中的油脂在胞内进行储存[24-25],一方面是因为产油真菌能够分泌胞外脂肪酶[26],另一方面是因为细胞膜上存在脂肪酸转运体[27-28]。因此本实验以不同的葡萄糖和大豆油的比例作为混合碳源,与以葡萄糖作为单一碳源的培养基做对比,对卷枝毛霉WJ11的细胞生长情况进行研究。如图1所示,卷枝毛霉WJ11细胞在单一碳源(葡萄糖)与在混合碳源上的生长趋势相似,在培养的前36 h,卷枝毛霉WJ11细胞大量生长,然后,生物量的增长趋势逐渐降低并趋于平缓,在72 h达到最大值,在发酵72 h后,细胞生物量及其脂质产量略有降低,这是因为细胞消耗能量(分解油脂)维持自身生命活动。由于0~12 h生物量比较低,其脂质产量很少且不稳定,故实验数据从12 h开始分析,在发酵12~72 h时,脂质产量逐渐积累,在72 h达到最大值(如图2)。由图2B可知,在发酵前期(12~36 h)细胞迅速增长,细胞干重随之增加,脂质逐渐积累,在发酵后期即细胞生长后期,菌体细胞缓慢生长,此时生物量(细胞干重)的增加是因为脂质的逐渐积累引起的。在混合碳源上生长的卷枝毛霉WJ11的生物量及脂质产量均高于单一碳源(葡萄糖)上生长的菌体。发酵培养96 h的过程中,对照组中WJ11的细胞干重最大达到14.72 g/L,脂质产量高达5.03 g/L,而在实验组中,当大豆油占比为56.25%(即葡萄糖为35 g/L,大豆油为24.3 g/L)时,WJ11的细胞干重高达19.60 g/L,脂质产量高达8.35 g/L,与对照组相比,该实验组的生物量和脂质产量分别提高了33.15%和65.1%。
与对照组相比,卷枝毛霉WJ11在混合碳源培养基上生长的更旺盛,这与早期实验结果一致[19,24]。脂肪酸氧化分解为二氧化碳和水,并释放出大量的能量,如通过β-氧化可将一分子软脂酸(C16:0)氧化,并释放129个ATP,进而为机体供能。而在混合培养基中培养时,在真菌细胞外,这些脂肪和油脂被胞外脂肪酶催化水解分解为游离脂肪酸[29],当游离脂肪酸吸收到细胞中以后,一方面为生命机体提供所需能量,促进细胞生长繁殖,另一方面,外源脂肪酸进入细胞中可直接参与脂质的非从头合成[29],这一过程大大促进了胞内脂质的合成效率。因此,外源油脂的添加可以引起卷枝毛霉WJ11生物量的增加。
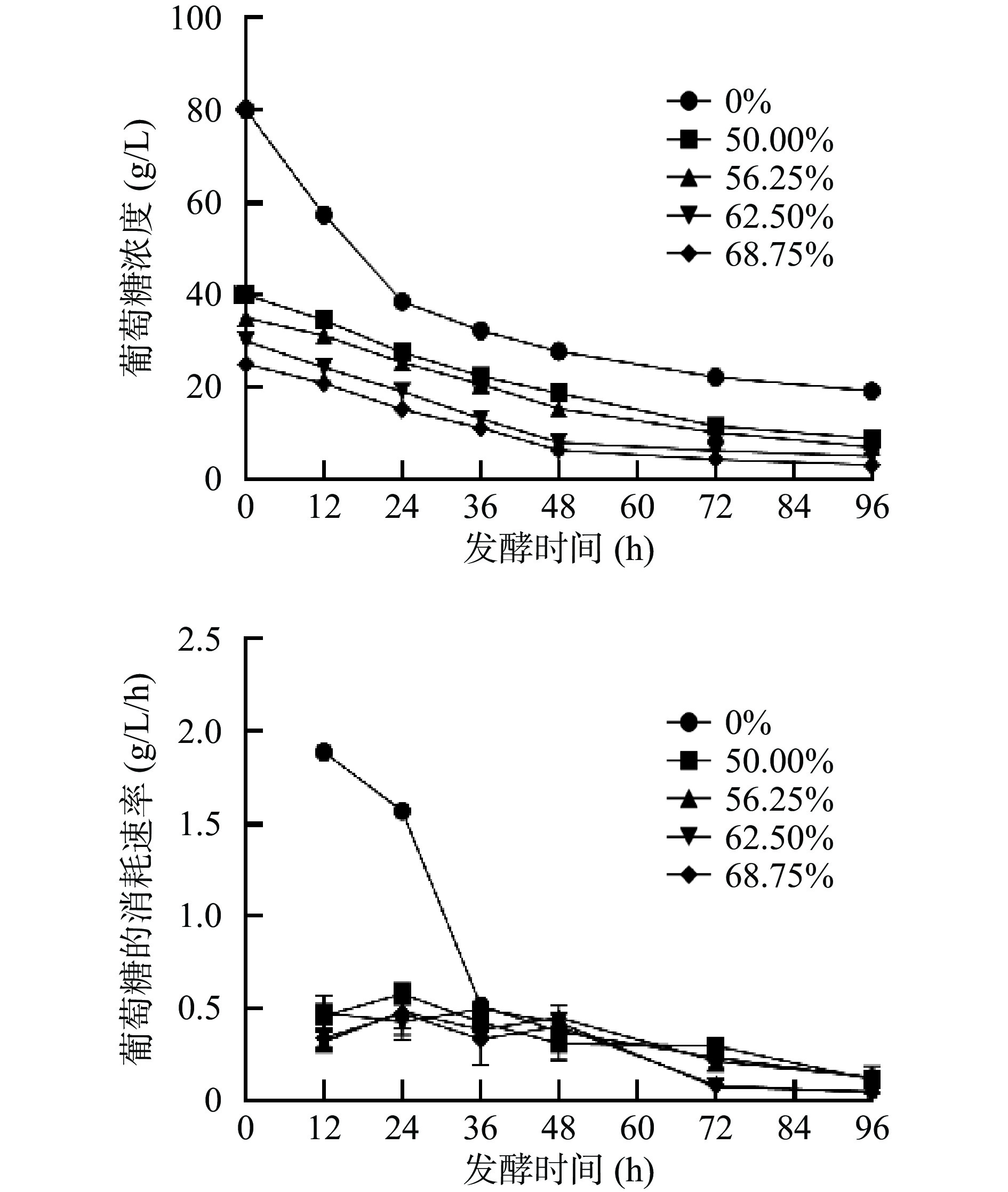
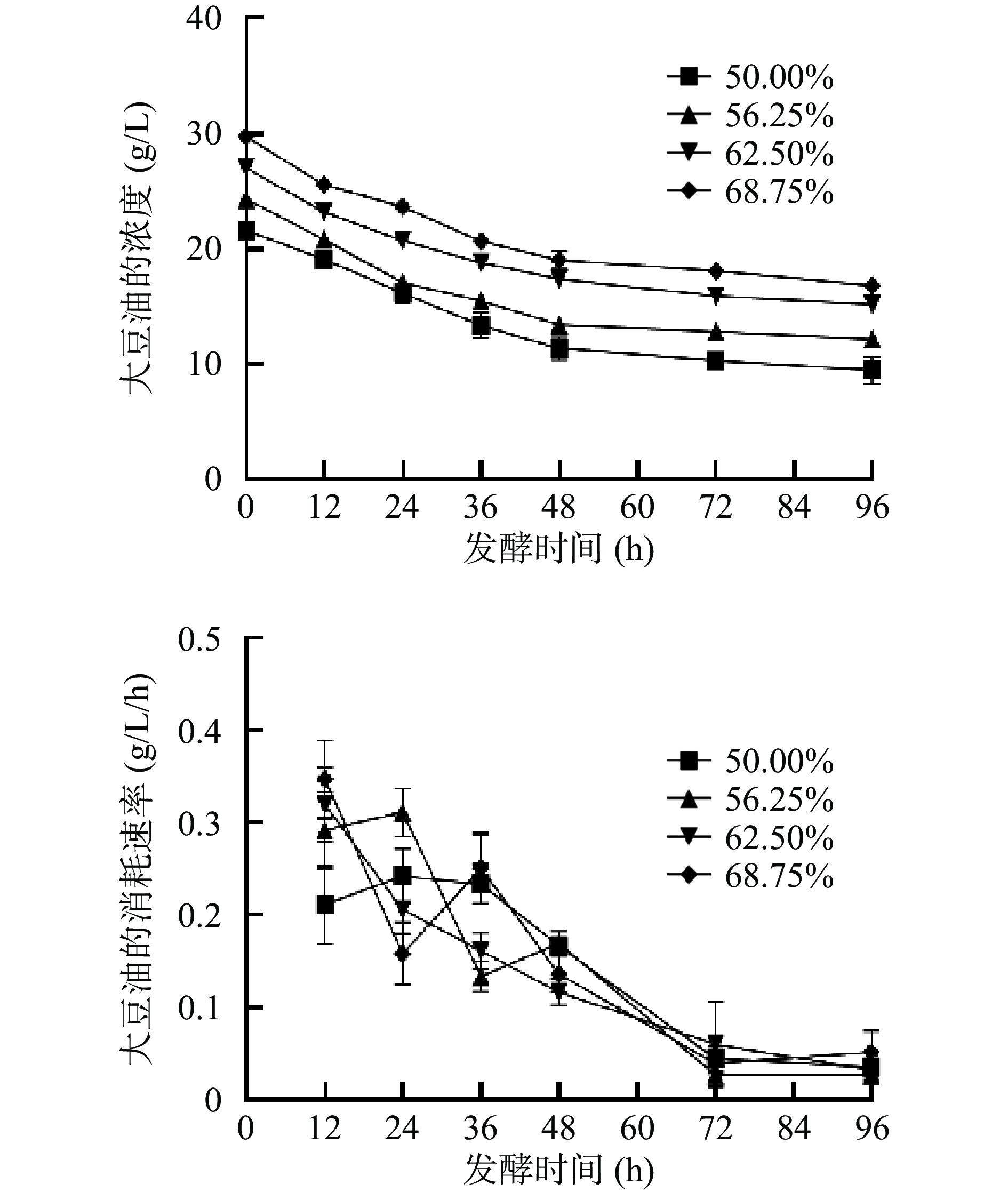
为了探究卷枝毛霉WJ11生长过程中对碳源的利用情况,测定上清液中的葡萄糖和大豆油含量并计算其消耗速率。如图3所示,当卷枝毛霉WJ11在混合培养基中生长时,葡萄糖的消耗速率基本相同,但在单一碳源(葡萄糖)培养基上生长的卷枝毛霉WJ11的葡萄糖消耗速率较快,并且在0~24 h内消耗速率达到1.5~1.9 g/L/h,原因可能为外源油脂(大豆油)的添加,使卷枝毛霉WJ11所能利用的碳源增加,故对葡萄糖的利用减少,大量游离在大豆油中的脂肪酸进入细胞后,通过分解后产生大量能量,供其进行生命活动[29]。在混合培养基中大豆油的消耗速率较低且相差不大(如图4),随发酵时间的延长其消耗速率逐渐降低,这可能是因为在葡萄糖没有被消耗尽的情况下,卷枝毛霉WJ11对大豆油的利用效率是一定的。
2.2 不同比例葡萄糖-大豆油混合培养基对WJ11脂质积累的影响
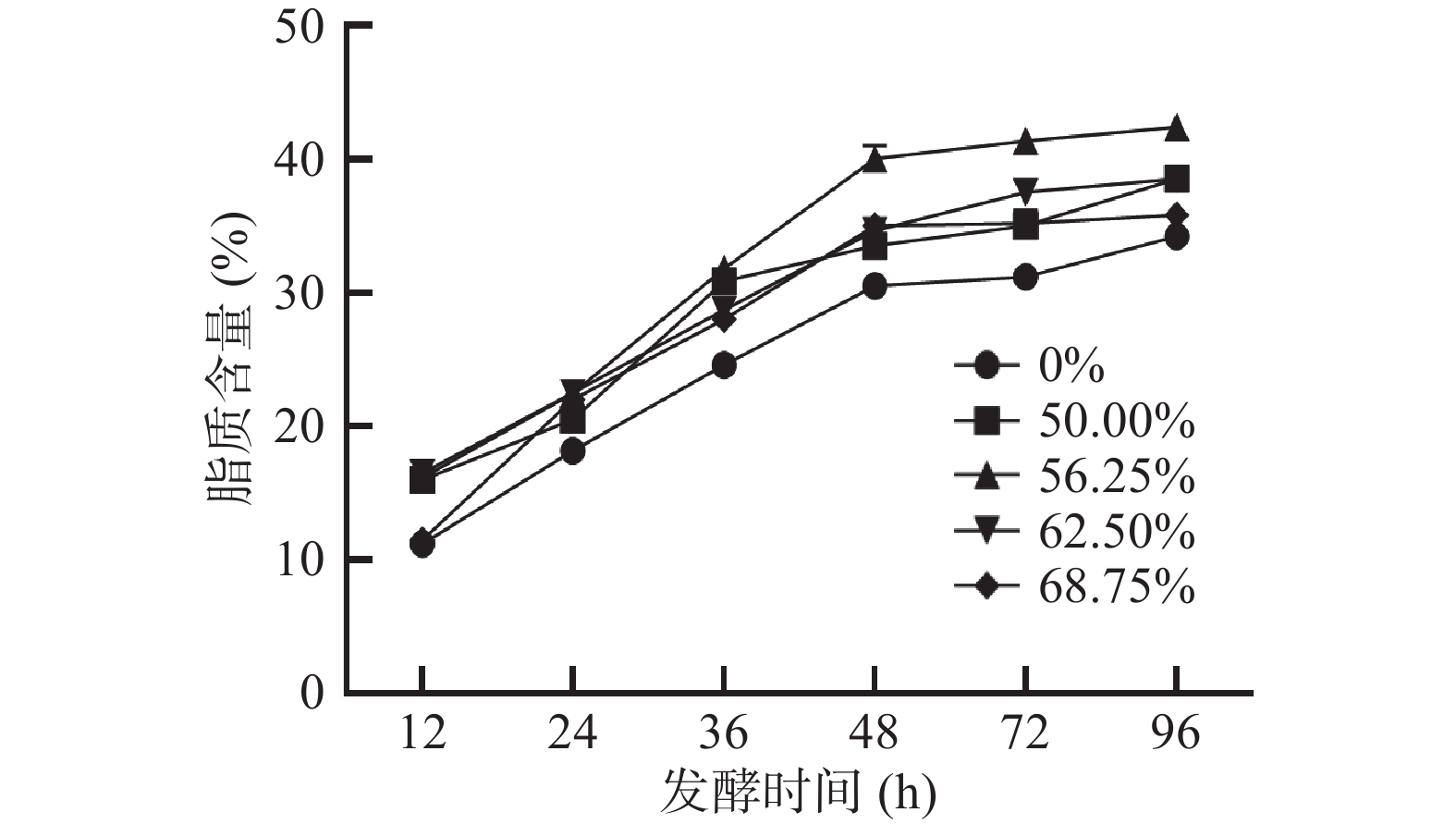
卷枝毛霉WJ11在不同培养基上的脂质含量如图5所示,在混合培养基上生长的脂质含量远高于单一碳源(葡萄糖)培养基上生长的脂质含量,同时在混合培养基上生长的卷枝毛霉WJ11的脂质积累明显大于单一碳源(葡萄糖)上生长的卷枝毛霉的脂质积累。培养96 h后,脂质积累达到最大值,而其中最佳的葡萄糖和大豆油的混合比例仍为大豆油占比56.25%(葡萄糖为35 g/L,大豆油为24.3 g/L),此时卷枝毛霉WJ11所积累的脂质含量最高可达42.62%,其脂质产量达到8.35 g/L,而对照组中卷枝毛霉WJ11的脂质积累含量为34.41%,其脂质产量达到5.06 g/L。与对照组相比,实验组的卷枝毛霉WJ11的脂质含量和产量分别提高了23.86%和65.10%。这可能是因为培养基中的外源油脂被分解成了小分子脂肪酸后进入细胞,并储存在细胞中,此外,游离脂肪酸进入细胞后,可以直接与甘油发生酯化反应生成甘油酯[28-30],从而提高了卷枝毛霉细胞内脂质的含量。因此,在混合碳源培养时,细胞内脂质的合成可以通过两个途径实现:一方面,以葡萄糖为碳源从头合成脂肪酸(C12~C16),另一方面,外源油中大量游离脂肪酸直接进入细胞参与脂质合成[29],从而提高了卷枝毛霉WJ11细胞内脂肪酸的积累。
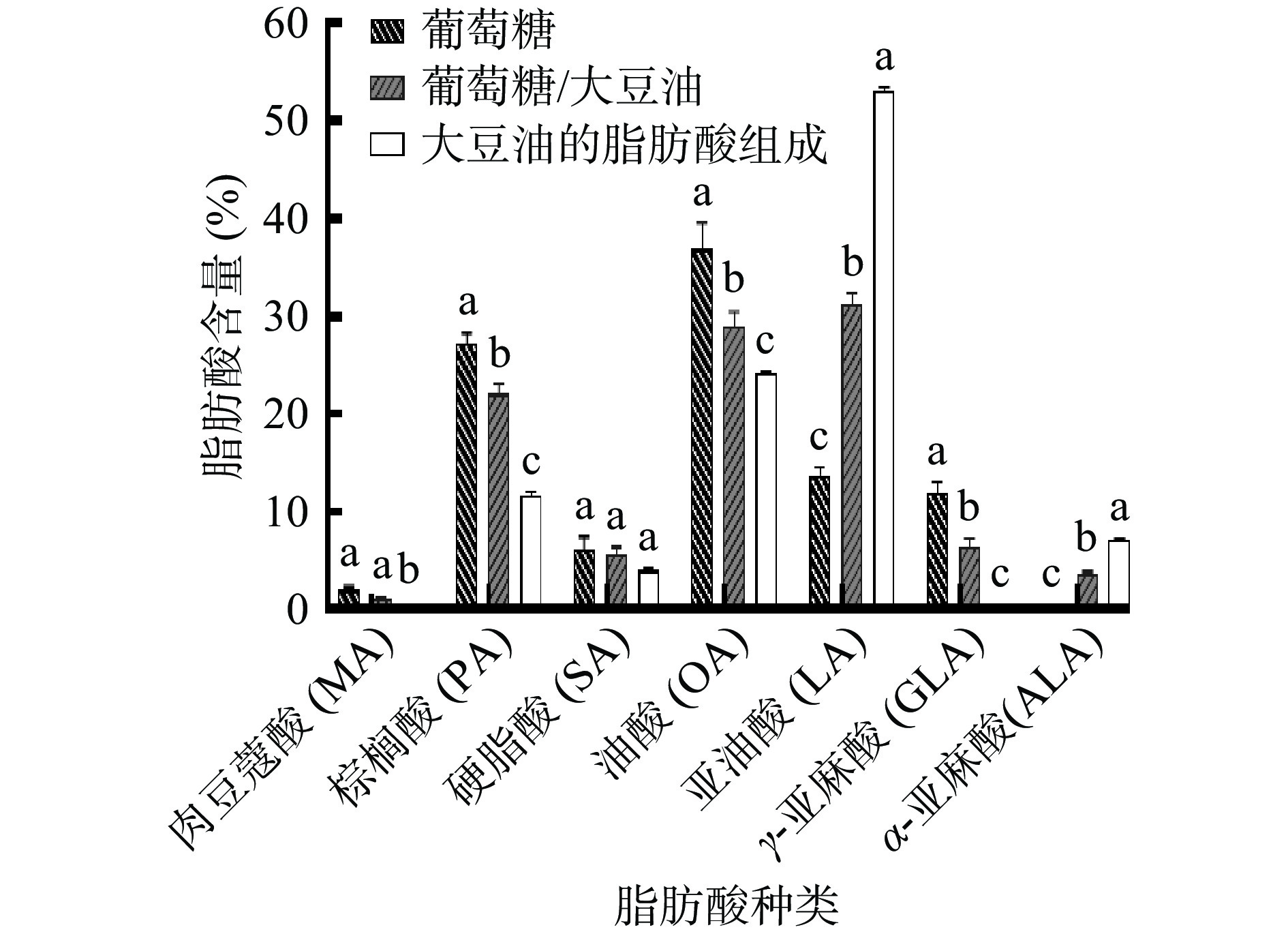
对大豆油的脂肪酸组成和在单一碳源(葡萄糖)以及最佳混合碳源培养基上生长的菌体脂肪酸组成进行分析,如图6所示,大豆油的脂肪酸组成主要包括棕榈酸(C16:0,Palmitoleic acid,PA)、硬脂酸(C18:0,Stearic acid,SA)、油酸(C18:1,Oleic acid,OA)、亚油酸(C18:2,Linolenic acid,LA)和α-亚麻酸(C18:3,α-Linolenic acid,ALA),在单一碳源(葡萄糖)上培养的卷枝毛霉WJ11细胞中的主要脂肪酸组成为PA、SA、OA、LA和GLA,而在添加大豆油的混合培养基上生长的卷枝毛霉WJ11的主要脂肪酸的比例和种类发生明显变化,卷枝毛霉WJ11的细胞内的LA含量明显增加,达到了32.44%,与对照组相比增加了131.9%,且在细胞中检测到ALA,含量达到3.92%。当卷枝毛霉WJ11在含有大豆油的培养基中生长时,PA、SA、OA、LA和ALA的含量都有显著(P<0.05) 提高,分别达到1.77 g/L、501.84 mg/L、2.56 g/L、2.71 g/L和327.32 mg/L,说明卷枝毛霉WJ11可将外源油脂吸收利用,并在胞内积累储存。
![]() 图 6 在单一碳源和最佳混合碳源上发酵的卷枝毛霉WJ11的脂肪酸组成及大豆油的脂肪酸组成分析注:MA,C14:0;PA,C16:0;SA,C18:0;OA,C18:1;LA,C18:2;GLA,6,9,12-C18:3;ALA,9,12,15-C18:3;不同小写字母表示不同组之间差异显著(P<0.05)。Figure 6. Fatty acid composition of Mucor circinelloides WJ11 fermented on a single and optimally mixed carbon source and analysis of fatty acid composition of soybean oil
图 6 在单一碳源和最佳混合碳源上发酵的卷枝毛霉WJ11的脂肪酸组成及大豆油的脂肪酸组成分析注:MA,C14:0;PA,C16:0;SA,C18:0;OA,C18:1;LA,C18:2;GLA,6,9,12-C18:3;ALA,9,12,15-C18:3;不同小写字母表示不同组之间差异显著(P<0.05)。Figure 6. Fatty acid composition of Mucor circinelloides WJ11 fermented on a single and optimally mixed carbon source and analysis of fatty acid composition of soybean oil2.3 单一碳源(葡萄糖)和最佳混合碳源上培养的卷枝毛霉WJ11脱饱和酶基因表达水平分析
根据NCBI数据库,查找到卷枝毛霉WJ11中存在两个Δ9脂肪酸脱饱和酶同工酶,两个Δ6脂肪酸脱饱和酶同工酶和一个Δ12脂肪酸脱饱和酶[31],并且已明确卷枝毛霉WJ11中脂肪酸的生物合成途径[32],SA经Δ9脱饱和酶催化生成OA,再经Δ12脱饱和酶催化生成LA,最后经过Δ6脱饱和酶催化生成GLA[31]。因此,对上述五个脂肪酸去饱和酶进行基因表达量的分析。
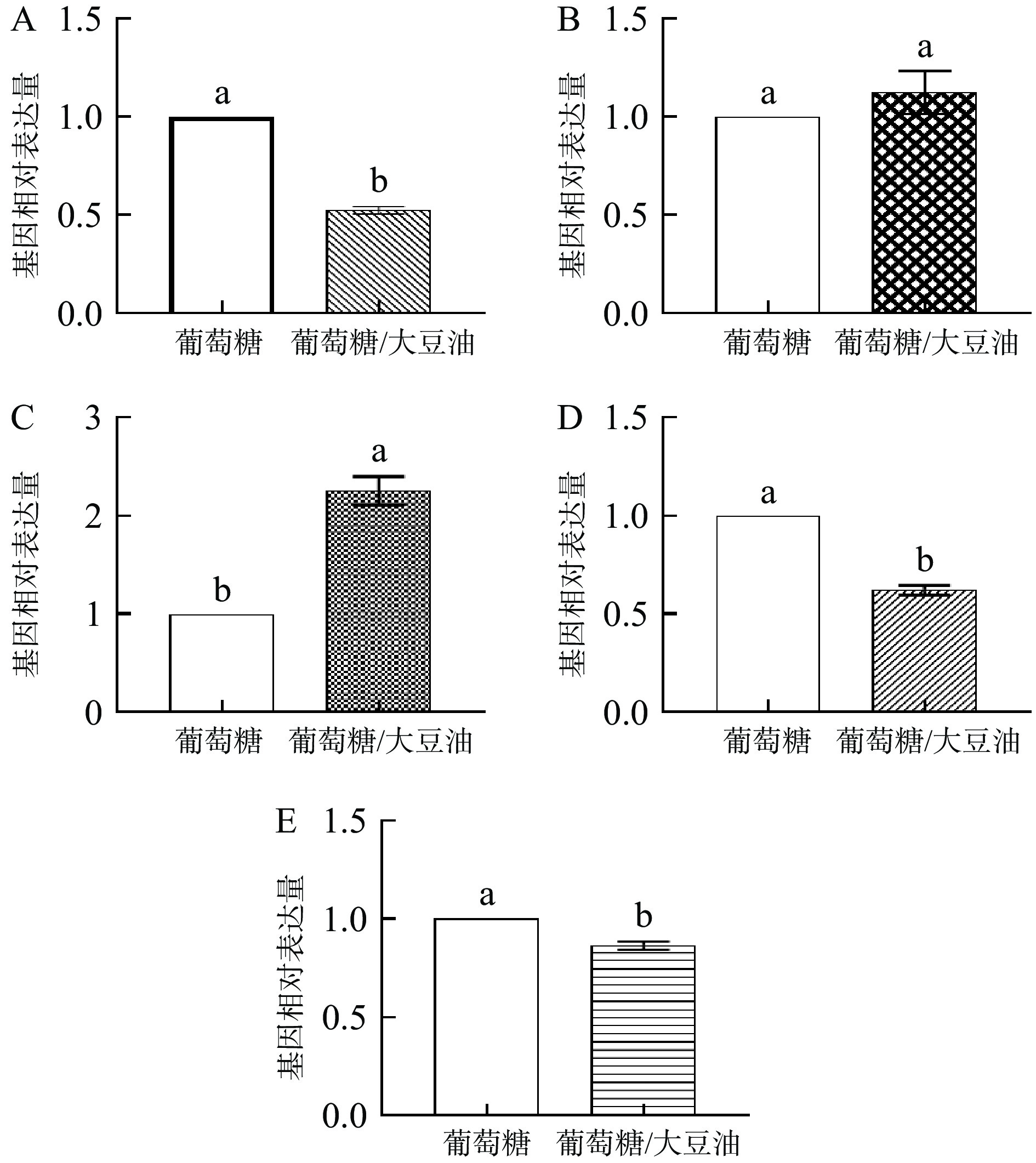
根据卷枝毛霉的生长特性,本文选取24 h(脂质合成率最高阶段)的样品,利用RT-qPCR进行各基因表达水平分析(图7)。图7A表明,在油脂迅速积累时期混合碳源上生长的WJ11生物体内△9-1脱饱和酶的表达量显著下降(P<0.05);图7B表明,△9-2脱饱和酶的表达量无显著差异;而图7C表明,在混合碳源上生长的WJ11生物体内△12脱饱和酶的表达量与对照组相比显著上升(P<0.05);图7D和图7E表明,在油脂迅速积累时期混合碳源上生长的WJ11生物体内△6-1脱饱和酶和△6-2脱饱和酶的表达量与对照组相比显著下降(P<0.05)。
综上所述,当卷枝毛霉WJ11在混合培养基中生长时,细胞中OA的含量降低了24%,这可能是由于在卷枝毛霉WJ11进行脂质合成时,即当SA经Δ9脱饱和酶催化生成OA,再经Δ12脱饱和酶催化生成LA,Δ9脱饱和酶的表达量相对下降,而Δ12脱饱和酶的表达量相对上升(见图6),因此导致OA的含量相对下降;而细胞中LA的含量增加了127%,这是因为外源OA的大量存在使卷枝毛霉WJ11细胞内的△12脱饱和酶的表达水平上调,从而使其能够利用大豆油中的OA合成LA[31];而卷枝毛霉WJ11中GLA的含量降低了46.7%,可能是由于△6脱饱和酶的表达水平降低导致的,不足以将过多的LA转化为GLA,从而使得GLA的积累量相对降低,这与之前的研究结果相符[33-34]。在混合碳源培养的卷枝毛霉WJ11细胞中检测到ALA的积累以及LA含量的增加,均可以说明卷枝毛霉WJ11可以吸收外源脂肪酸,并将其储存在细胞内,参与脂质的合成。
3. 结论
与单一碳源(葡萄糖)培养基相比,以大豆油为外源碳源添加到培养基时,不同的添加量会对卷枝毛霉WJ11细胞的生长和脂质积累造成不同的影响,均可引起卷枝毛霉WJ11细胞生物量和脂质产量的增加。在最佳糖油混合碳源培养基(葡萄糖35 g/L,大豆油24.3 g/L,即大豆油占比为56.25%)上培养时,卷枝毛霉WJ11的细胞干重可高达19.60 g/L,与在单一碳源(葡萄糖)上生长的菌体相比增加了33.15%,积累的脂质含量和产量达到42.62%和8.35 g/L,与对照组相比增加了23.8%和65.10%,并且在细胞内积累了ALA。因此,产油真菌可以利用外源油脂进行脂质积累,并且可以据此生产高附加值多不饱和脂肪酸。本研究为农业、食品工业低值油脂的综合利用、生产高附加值的多不饱和脂肪酸奠定了基础。
-
图 6 在单一碳源和最佳混合碳源上发酵的卷枝毛霉WJ11的脂肪酸组成及大豆油的脂肪酸组成分析
注:MA,C14:0;PA,C16:0;SA,C18:0;OA,C18:1;LA,C18:2;GLA,6,9,12-C18:3;ALA,9,12,15-C18:3;不同小写字母表示不同组之间差异显著(P<0.05)。
Figure 6. Fatty acid composition of Mucor circinelloides WJ11 fermented on a single and optimally mixed carbon source and analysis of fatty acid composition of soybean oil
表 1 葡萄糖-大豆油混合培养基的配方
Table 1 Formulation of glucose-soybean oil mixed medium
组数 葡萄糖(g/L) 大豆油(g/L) 1 80(100.00%) 0(0) 2 40(50.00%) 21.6(50.00%) 3 35(43.75%) 24.3(56.25%) 4 30(37.50%) 27.0(62.50%) 5 25(31.25%) 29.7(68.75%) 注:括号内为葡萄糖或大豆油在培养基中所占的比例。 表 2 卷枝毛霉WJ11中Δ9、Δ12和Δ6脱饱和酶基因信息
Table 2 Gene information of Δ9-, Δ12- and Δ6-desaturases in M. circinelloides WJ11
基因名称 染色体上的位置 基因大小 脱饱和
酶基因scaffold00005.3 scaffold00005: 15315- 16821(+) 1506 Δ9-1 scaffold00126.19 scaffold00126: 56635- 58330(+) 1696 Δ9-2 scaffold00248.11 scaffold00248: 28862-30077(−) 1215 Δ12 scaffold00003.2 scaffold00003: 11655-13376(−) 1722 Δ6-1 scaffold00010.52 scaffold00010: 159563-161134(+) 1572 Δ6-2 表 3 实时荧光定量 PCR 所用的特异性引物
Table 3 Details of specific primer pairs used in RT-qPCR
引物名称 序列5'-3' rt-D9-1-F ATGCTCCTTATTACCTGCGCCGAC rt-D9-1-R CAATAAGCTTTAAGCCTAGAGTTTAA rt-D9-2-F ATGTCAACTACAACGACAACTA rt-D9-2-R AACCTGAGAAGAACAAGACCAAGTAA rt-D6-1-F CCTTGTCATGGTGGAAGAACAAGC rt-D6-1-R CGGCAATGAAACGGGATAACATGG rt-D6-2-F GCAGAGACGCTACAGATGTCTTTC rt-D6-2-R CGAATTTCTTGAGCAAAAGCAGCAG rt-D12-F CAGGTCTTTGTCCCCTCTACTCG rt-D12-R ATCTTGACCAGAGACATTGGTG β-actin-F GATGAAGCCCAATCCAAGA β-actin-R TTCTCACGGTTGGACTTGG -
[1] PAUL S, BHAGOBATY R K, NIHALANI M C, et al. Are endophytic fungi a feasible option as biofuel nanofactories[J]. International Journal of Scientific Research,2018,7:1112−1118.
[2] KHOT M, KATRE G, ZINJARDE S, et al. Single cell oils (SCOs) of oleaginous filamentous fungi as a renewable feedstock: A biodiesel biorefinery approach[J]. Fungal Biorefinery,2018,1:145−183.
[3] JAMBULINGAM R, SHALMA M, SHANKAR V. Biodiesel production using lipase immobilised functionalized magnetic nanocatalyst from oleaginous fungal lipid[J]. Journal of Cleaner Production,2019,215(D7):245−258.
[4] JIN M, SLININGER P J, DIEN B S, et al. Microbial lipid-based lignocellulosic biorefinery: Feasibility and challenges[J]. Trends in Biotechnology,2015,33(1):43−54. doi: 10.1016/j.tibtech.2014.11.005
[5] . 孙彩丽. 卷枝毛霉利用外源油积累脂质的机制研究[D]. 淄博: 山东理工大学, 2022 SUN C L. Study on the mechanism of lipid accumulation by exogenous oil in Mucor circinelloides[D]. Zibo: Shandong University of Technology, 2022.
[6] RATLEDGE C, WYNN J P. The biochemistry and molecular biology of lipid accumulation in oleaginous microorganisms[J]. Advances in Applied Microbiology,2002,51:1−51.
[7] BJORKLUND G, DADAR M, DOSA M D, et al. Insights on dietary omega-6/omega-3 polyunsaturated fatty acid (PUFA) ratio in oxidative metabolic pathways of oncological bone disease and global health[J]. Current Medicinal Chemistry,2021,28(9):1672−1682. doi: 10.2174/0929867327666200427095331
[8] KAMAT S, KHOT M, ZINJARDE S, et al. Coupled production of single cell oil as biodiesel feedstock, xylitol and xylanase from sugarcane bagasse in a biorefinery concept using fungi from the tropical mangrove wetlands[J]. Bioresource Technology,2013,135:246−253. doi: 10.1016/j.biortech.2012.11.059
[9] MENG X, YANG J, XU X, et al. Biodiesel production using lipase immobilised functionalized magnetic nanocatalyst from oleaginous fungal lipid[J]. Renewable Energy,2009,34:1−5. doi: 10.1016/j.renene.2008.04.014
[10] ZHANG L, ZHANG H Y, SONG Y D. Identification and characterization of diacylglycerol acyltransferase from oleaginous fungus Mucor circinelloides[J]. Journal of Agricultural and Food Chemistry,2018,66(3):674−681. doi: 10.1021/acs.jafc.7b04295
[11] CARSANBA E, PAPANIKOLAOU S, ERTEN H. Production of oils and fats by oleaginous microorganisms with an emphasis given to the potential of the nonconventional yeast Yarrowia lipolytica[J]. Critical Reviews in Biotechnology,2018,38(8):1230−1243. doi: 10.1080/07388551.2018.1472065
[12] COLLA L M, PRIMAZ A, BENEDETTI S, et al. Surface response methodology for the optimization of lipase production under submerged fermentation by filamentous fungi[J]. Brazilian Journal of Microbiology,2016,47(2):461−467. doi: 10.1016/j.bjm.2016.01.028
[13] GUJJALA L K, KUMAR S J, TALUKDAR B, et al. Biodiesel from oleaginous microbes: Opportunities and challenges[J]. Biofuels,2019,10(1):45−59. doi: 10.1080/17597269.2017.1402587
[14] HUANG X, LUO H, MU T, et al. Enhancement of lipid accumulation by oleaginous yeast through phosphorus limitation under high content of ammonia[J]. Bioresource Technology,2018,262:9−14. doi: 10.1016/j.biortech.2018.04.063
[15] IACOBAZZI V, INFANTINO V. Citrate-new function for an old metabolite[J]. Journal of Biological Chemistry,2014,395:387−399. doi: 10.1515/hsz-2013-0271
[16] ZHAO L N, CANOVAS-MARQUES J T, TANG X, et al. Role of malate transporter in lipid accumulation of oleaginous fungus Mucor circinelloides[J]. Applied Microbiology and Biotechnology,2016,100(3):1297−1305. doi: 10.1007/s00253-015-7079-y
[17] YANG J, KHAN M A K, ZHANG H, et al. Mitochondrial citrate transport system in the fungus Mucor circinelloides: Identification, phylogenetic analysis, and expression profiling during growth and lipid accumulation[J]. Current Microbiology,2020,77(2):220−231. doi: 10.1007/s00284-019-01822-5
[18] . ZHANG H L, ZHANG H, CHEN Y Q, et al. Enhanced lipid accumulation in the yeast Yarrowia lipolytica by over-expression of ATP: Citrate lyase from Mus musculus[J]. Journal of Biotechnology, 2014, 192 Pt A: 78-84. .
[19] 高萌, 辛菲菲, 王瑞雪, 等. 过表达酰基蛋白硫酯酶促进产油真菌卷枝毛霉脂肪酸合成[J]. 粮食与食品工业,2021,28(3):1−5. [GAO M, XIN F F, WANG R X, et al. Overexpression of acyl-protein thioesterase enhanced fatty acid biosynthesis in oleaginous fungus Mucor circinelloides[J]. Cereal and Food Industry,2021,28(3):1−5. doi: 10.3969/j.issn.1672-5026.2021.03.001 [20] TANG X, CHEN H, CHEN Y Q, et al. Comparison of biochemical activities between high and low lipid-producing strains of Mucor circinelloides: An explanation for the high oleaginicity of strain WJ11[J]. Public Library of Science One,2015,10:1−12.
[21] HARAUMA A, SUEYASU T, TOKUDA H, et al. Changes in behavior and fatty acid composition induced by long-term reduction in murine Δ6-desaturation activity[J]. Prostaglandins Leukotrienes and Essential Fatty Acids,2020,155:102079. doi: 10.1016/j.plefa.2020.102079
[22] 唐鑫. 产油真菌卷枝毛霉WJ11高产脂质的分子机制[D]. 无锡: 江南大学, 2015 TANG X. Molecular mechanism of high lipid-production in oleaginous fungus Mucor circinelloides WJ11[D]. Wuxi: Jiangnan University, 2015.
[23] KHAN M A K, YANG J, HUSSAIN S A, et al. Construction of DGLA producing cell factory by genetic modification of Mucor circinelloides[J]. Microbial Cell Factories,2019,18(1):64. doi: 10.1186/s12934-019-1110-4
[24] SUN C L, AABID M S, YANG J H, et al. Transcriptome analysis of oleaginous fungus Mucor circinelloides WJ11 in response to exogenous soybean oil as carbon source[J]. Natural Product Communications,2021,16(6):1−7.
[25] 昝新艺. 卷枝毛霉脂肪酶及其调控脂质代谢的机制[D]. 无锡: 江南大学, 2019 ZAN X Y. Lipases and their role in regulating lipid metabolism in the oleaginous fungus Mucor circinelloides[D]. Wuxi: Jiangnan University, 2019.
[26] 王艳霞, 姜川, 李鹏程, 等. 卷枝毛霉胞外/胞内脂肪酶的发酵优化及酶学性质[J]. 食品科技,2020,45(4):12−18. [WANG Y X, JIANG C, LI P C, et al. Fermentation optimization and enzymatic properties of extracellular/intracellular lipase produced by Mucor circinelloides[J]. Food Science and Technology,2020,45(4):12−18. doi: 10.13684/j.cnki.spkj.2020.04.003 [27] 王艳霞, 王璐, 杨俊换, 等. 卷枝毛霉苹果酸转运蛋白生物信息学分析[J]. 山东理工大学学报(自然科学版),2021,35(5):44−48. [WANG Y X, WANG L, YANG J H, et al. Bioinformatics analysis of malate transporter protein in Mucor circinelloides[J]. Journal of Shandong University of Technology (Natural Science Edition),2021,35(5):44−48. [28] 王璐, 张瑶, 杨俊换, 等. 卷枝毛霉重组菌株Mc-MT-2培养条件优化及产油特性[J]. 农业工程学报,2021,37(8):251−258. [WANG L, ZHANG Y, YANG J H, et al. Optimization of the culture conditions and lipid production characteristics of Mucor circinelloides recombinant strain Mc-MT-2[J]. Transactions of the Chinese Society of Agricultural Engineering,2021,37(8):251−258. doi: 10.11975/j.issn.1002-6819.2021.08.029 [29] NAJJAR A, ROBERT S, GUÉRIN C, et al. Quantitative study of lipase secretion, extracellular lipolysis, and lipid storage in the yeast Yarrowia lipolytica grown in the presence of olive oil: Analogies with lipolysis in humans[J]. Applied Microbiology and Biotechnology,2011,89(6):1947−1962. doi: 10.1007/s00253-010-2993-5
[30] SUN C L, SHAH A M, YANG J H, et al. The effect of soybean oil on lipid metabolism in Mucor circinelloides WJ11 by metabolomic analysis[J]. American Journal of Biochemistry and Biotechnology,2021,17(2):130−139. doi: 10.3844/ajbbsp.2021.130.139
[31] ZHANG Y, LUAN X, ZHANG H, et al. Improved γ-linolenic acid production in Mucor circinelloides by homologous overexpressing of delta-12 and delta-6 desaturases[J]. Microbial Cell Factories,2017,16:113−119. doi: 10.1186/s12934-017-0723-8
[32] KHAN M, YANG J H, HUSSAIN S, et al. Genetic modification of Mucor circinelloides to construct stearidonic acid producing cell factory[J]. International Journal of Molecular Sciences,2019,20(7):1−10.
[33] ZHANG Y, WANG Y X, YANG J H, et al. Improved γ-linolenic acid production from cellulose in Mucor circinelloides via coexpression of cellobiohydrolase and delta-6 desaturase[J]. Journal of Agricultural and Food Chemistry,2022,70(14):4373−4381. doi: 10.1021/acs.jafc.2c00359
[34] ZAN X Y, TANG X, CHU L F, et al. Characteristics of cell growth and lipid accumulation of high and low lipid-producing strains of Mucor circinelloides grown on different glucose-oil mixed media[J]. Process Biochemistry,2018,72:31−40. doi: 10.1016/j.procbio.2018.06.012





 下载:
下载:





 下载:
下载:
