Antioxidant Activity and Pyrolysis Properties of Lignin Extracted from Camellia oleifera Shell by Deep Eutectic Solvents (DES)
-
摘要: 为了获得兼具分子量低、分散度低和抗氧化活力高的木质素,本研究以油茶果壳为原料,采用碱法和低共熔溶剂法分离得到四种木质素,利用紫外光谱、凝胶渗透色谱、傅里叶变换红外光谱和热重分析对其进行结构分析,并通过清除1,1-二苯基-2-三硝基苯肼(DPPH)自由基能力评价其体外抗氧化活性。结果表明:紫外光谱和红外光谱显示油茶果壳木质素主要由紫丁香基和愈创木酚基单元结构组成。凝胶渗透色谱分析表明碱木质素的重均分子量(Mw)和分散度(PDI)分别为41858 g/mol和4.53,而低共熔溶剂提取的木质素具有较小的相对分子量(Mw<11000 g/mol)和分散度(PDI<2)。热重分析可知油茶果壳木质素热稳定性依次为:氯化胆碱-草酸(ChCl-OA)>碱木质素(AL)>氯化胆碱-乙二醇-对甲苯磺酸(ChCl-EG-P)>氯化胆碱-丙三醇(ChCl-GA)。此外,抗氧化活性结果显示4种木质素均有一定的抗氧化活性,清除DPPH自由基的IC50为0.388~1.02 mg/mL。此研究结果为油茶果壳木质素分离和高值化开发利用提供了一定的参考价值。Abstract: In order to obtain lignin with low molecular weight and polydispersity, as well as high antioxidant activity, using Camellia oleifera shell as raw material, four lignin products were isolated from it by alkaline and deep eutectic solvents. The structural and pyrolysis properties of lignin were investigated with ultraviolet spectroscopy (UV), Fourier transform infrared spectroscopy (FTIR), gel permeation chromatography (GPC) and thermogravimetric analyzer (TGA). Furthermore, the antioxidant activity of the lignin samples was evaluated by 1,1-diphenyl-2-picrylhydrazyl (DPPH) radical scavenging activity assay. The UV and FTIR analyses showed that the lignin from Camellia oleifera shell was mainly composed of guaiacyl and syringyl. GPC analysis revealed that AL had a relatively higher molecular weight (Mw=41858 g/mol) and broad polydispersity index (PDI=4.53), and the DES-lignin exhibited relatively low relative molecular weight (Mw<11000 g/mol) and narrow polydispersity index (PDI<2). Thermogravimetric analysis showed that the thermal stability of lignin samples was ChCl-OA>AL>ChCl-EG-P>ChCl-GA. Furthermore, the results showed that four lignin products had good antioxidant activity in vitro, and the IC50 values of DPPH free radical scavenging ability was 0.388~1.02 mg/mL. The findings of this study would provide a novel way to fractionate lignin from Camellia oleifera shell, and provide certain reference value for the development of lignin valorization.
-
油茶是我国南方广泛种植的木本食用油料树种,种植面积约6000万亩,每年油茶加工产生的果壳副产物可达约400万吨[1]。大部分油茶果壳以焚烧或丢弃方式处理,造成资源浪费和环境污染。因此,如何将油茶果壳转化为高附加值资源成为当今的研究热点。油茶果壳组分复杂多样,其中纤维素(13.87%~20.95%)、半纤维素(35.15%~49.34%)和木质素(30.07%~36.23%)含量占比达到80%以上[2]。木质素是天然芳香族高分子聚合物,含有多种类型活性官能团,如羟基、羧基和甲氧基等,将其转化为芳香族化学品、生物燃料和生物功能材料后在化工、医药、食品和能源等领域具有较广的应用前景和科学研究意义[3]。
提取木质素常用的方法有碱法、酸法、酶法、有机溶剂法等[4-6],不同处理分离得到的木质素结构存在较大差异。崔兴凯等[7]利用五种不同方法提取甘蔗渣木质素并研究其结构及热解特性,结果发现五种木质素分子量和热解特性存在较大差异,其中乙酸木质素的酚羟基含量(3.19%)和重均分子量均高于Acetosolv木质素。Pin等[8]利用不同类型质子型离子液体提取甘蔗渣木质素对其化学结构分析,发现[Etid][Lac]型离子液体分离的木质素中β-O-4键可达48.2%,而[2He][Lac]型离子液体分离的木质素中β-O-4键仅为19.3%。Wei等[9]采用有机溶剂法和球磨法提取桉树木质素,结果表明球磨法提取磨木木质素中β-O-4、β-β、β-5和β-1的比例分别为52.19%、15.38%、5.13%和1.44%,而有机溶剂法提取木质素中四种化学键相对较少,分别为7.74%、5.71%和0.82%,且不含β-1键;此外,球磨法提取磨木木质素中甲氧基含量比有机溶剂法提取木质素含量高,但其羟基含量比有机溶剂提取木质素含量低;通过进一步的木质素抗氧化活性试验发现有机溶剂分离得到的木质素明显高于磨木木质素。综上所述,由于木质素提取方法不同,导致其结构和抗氧化活性存在较大差异。
近年来,低共熔溶剂(Deep eutectic solvents,DES)因具有良好水溶性、可降解性、生物相容性、高选择性、可回收利用、高效率和易制备等优点,已成为有机溶剂和离子液体的替代品,并已应用于提取分离木质素[10]。本研究以传统碱法提取木质素作为参考,探究羧酸型、醇型和三元体系胆碱类低共熔溶剂分离的油茶果壳木质素在分子结构、热稳定性和抗氧化活性方面存在的差异。以期为油茶加工废弃物资源高值化利用及开发木质素基抗氧化性功能材料提供依据。
1. 材料与方法
1.1 材料与仪器
油茶果壳 产自贵州省荔波县;无水乙醇、冰乙酸、氢氧化钠、浓硫酸、吡啶、醋酸酐、石油醚、1,4-二氧六环、乙醚、对甲苯磺酸、草酸、丙三醇、氯化胆碱等 均为分析纯;1,1-二苯基-2-苦基肼(DPPH,纯度96%) 上海麦克林生化科技有限公司;四氢呋喃(色谱级) 国药化学试剂有限公司。
GreatWall HWCL-3集热恒温磁力搅拌油浴锅 郑州长城科工贸有限公司;台式冷冻高速离心机 上海卢湘仪离心机有限公司;TU-1901双光束紫外可见分光光度计 北京普析仪器有限公司;Nicolet iS20傅里叶变换红外光谱仪 美国赛默飞世尔科有限公司;TDA/DSC 2热重/差热同步分析仪 瑞士梅特勒-托利多仪器公司;waters1525/waters 2414液相色谱-凝胶渗透色谱仪 美国沃世特科技公司。
1.2 实验方法
1.2.1 DES的合成
DES合成方法参考文献[10]中描述方法并做适当修改。氯化胆碱(ChCl)作为氢键受体和氢键供体(草酸、丙三醇、乙二醇和对苯甲磺酸)按不同摩尔比例混合后,置于80 ℃恒温的油浴锅中反应2 h,使其充分混合成为透明均一液体,分别得到以下三种低共熔溶剂:氯化胆碱-草酸(摩尔比1:1,ChCl-OA)、氯化胆碱-丙三醇(摩尔比1:2,ChCl-GA)和氯化胆碱-乙二醇-对甲苯磺酸(摩尔比1:1.96:0.06,ChCl-EG-P),取出冷却后密封保存,备用。
1.2.2 不同方法制备木质素
油茶果壳自然风干,粉碎后过80目标准筛,取筛下物,将一定量粉末置于索式抽提器中,加入一定体积的苯和乙醇混合溶液(2:1,v/v)抽提6 h,脱除色素、脂肪和蜡等杂质,抽提完成后过滤去除苯和乙醇溶液,剩余固体自然风干,收集备用。
碱法提取木质素工艺参考文献[7]中所述方法并适当修改。油茶果壳粉末与3% NaOH溶液在固液比(w/v,下同)为1:10条件下充分混合后,置于90 ℃油浴锅中,搅拌速度200 r/min,反应90 min,过滤得到澄清黑液,逐滴加入质量分数为4%硫酸溶液至黑液中,溶液pH调节至2.0左右,使木质素沉淀析出,在转速10000 r/min条件下离心10 min,弃上清液,固体沉淀用去离子水洗至中性后,用90%的1,4-二氧六环水溶液(V二氧六环:V水=1:9)溶解固体沉淀,转速为9000 r/min,离心10 min除去不溶物,上清液减压浓缩后,加入10倍体积的去离子水,木质素固体析出,转速为9000 r/min,离心10 min除上清液,收集固体,放置于冷冻干燥机12 h后,得到干燥碱木质素,标记为AL。
DES法提取木质素过程参考文献[10]所述方法并适当修改。油茶果壳粉末分别与氯化胆碱-草酸(ChCl-OA)、氯化胆碱-丙三醇(ChCl-GA)、氯化胆碱-乙二醇-对甲苯磺酸(ChCl-EG-P)三种DES混合均匀后(固液比1:20),置于120 ℃油浴锅中,搅拌速度200 r/min,反应6 h后,冷却后离心得到透明液体,残渣用无水乙醇洗涤3~5次,合并过滤液体,旋蒸去除无水乙醇,将浓缩液缓慢加入4 L去离子水中,使木质素固体沉淀析出,过滤收集固体沉淀。用无水乙醇多次洗涤固体沉淀,确保无DES残留后,将过滤分离得到固体沉淀进行冷冻干燥12 h,得到干燥粗木质素,氯化胆碱-草酸、氯化胆碱-丙三醇、氯化胆碱-乙二醇-对甲苯磺酸三种DES分离所得木质素分别标记为:ChCl-OA、ChCl-GA和ChCl-EG-P。
以上粗木质素纯化按照崔兴凯等[7]描述方法,将粗木质素溶于90%乙酸水溶液,然后加入10倍体积的去离子水,析出木质素沉淀,过滤,木质素水洗至中性后冷冻干燥。再将干燥的木质素溶于1,4-二氧六环-乙醇溶液(V1,4-二氧六环:V乙醇=8:2),转速为9000 r/min,离心10 min去除不溶物,澄清液中滴加5倍体积的乙醚-石油醚溶液(V乙醚:V石油醚=1:1),使木质素沉淀析出,所得木质素采用乙醚-石油醚溶液洗涤两次后,冷冻干燥。
1.2.3 木质素结构表征
1.2.3.1 紫外光谱分析
将2 mg木质素分别溶解于20 mL氢氧化钠溶液(pH12)和20 mL 1,4-二氧六环水溶液(V1,4-二氧六环:V水=1:9)后,利用紫外分光光度计在波长范围为200~400 nm内,进行光谱扫描。
1.2.3.2 傅里叶变换红外光谱(FTIR)分析
取1 mg干燥纯化的木质素与100 mg光谱纯溴化钾在玛瑙研钵中充分研磨至粒径小于2 μm左右,利用压片机进行制样,获得厚度均匀透明的薄片,采用傅里叶变换红外光谱仪进行图谱扫描,范围为500~4000 cm−1,分辨率4 cm−1。
1.2.3.3 凝胶渗透色谱分析
按照刘金科等[11]描述的方法对木质素进行乙酰化。取50 mg木质素溶于4 mL吡啶/醋酸酐(体积比为1:1)混合液,在避光条件下常温搅拌24 h后,将木质素溶液逐滴加入乙醚溶液中,沉淀出乙酰化木质素,过滤得到木质素沉淀,用乙醚洗涤沉淀直至无吡啶残留后,置于40 ℃真空干燥箱中干燥。取2 mg乙酰化木质素完全溶于1 mL四氢呋喃(THF)后,用有机系滤头过滤木质素溶液,取10 μL木质素溶液进样,采用凝渗透色谱仪测定木质素相对分子量。色谱条件:色谱柱Agilent PLgel 5 μm MIXED-C,柱温35 ℃,流动相四氢呋喃,流速1 mL/min,以不同分子量聚苯乙烯作为标准品测得其相对分子量后,绘制标准曲线。
1.2.3.4 热重分析
木质素热解特性采用热重/差热同步分析仪进行测试,测定温度范围:30~1000 ℃,升温速率:20 ℃/min。以高纯氮气(99.999%)为载气,气体流速:10 mL/min。
1.2.4 木质素清除DPPH自由基能力测定
将不同质量木质素溶于1,4-二氧六环/水(体积比为9:1)溶液中,制得0.2~1.0 mg/mL的木质素溶液,取0.1 mL的木质素溶液置于10 mL棕色离心管中,加入3.9 mL DPPH的乙醇溶液(浓度为25 mg/L),摇匀后,放置于25 ℃的水浴锅中,静置30 min后,利用紫外分光光度计在波长517 nm处测量溶液吸光度。根据以下公式计算DPPH自由基清除率:
DPPH自由基清除率(%)=A0−AiA0×100 式中:A0为空白实验组吸光度;Ai为待测样品吸光度。
1.3 数据处理
所有实验均进行三次重复,实验数据采用平均值±标准差表示,并采用Origin 2021软件进行数据分析和作图。
2. 结果与分析
2.1 紫外吸收光谱分析
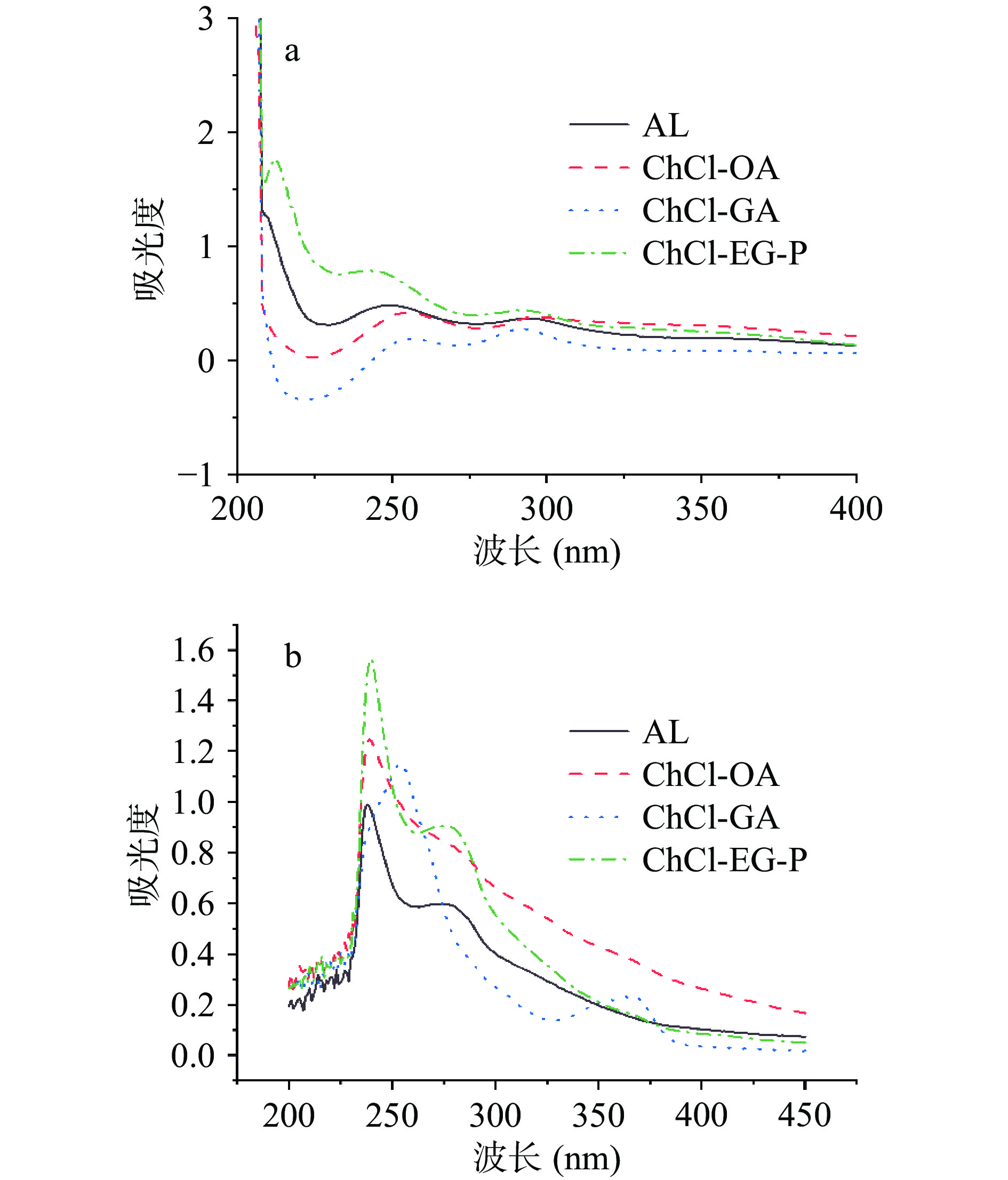
木质素具有苯环结构和共轭羰基等基团,因此会有明显的紫外吸收性能。图1为四种木质素分别在氢氧化钠溶液(pH12)和90% 1,4-二氧六环溶液中的紫外吸收光谱图。在氢氧化钠溶液中,四种木质素在210 nm(共轭烯键)、250 nm(共轭双键的π-π*跃迁产生的K吸收带)、和290 nm附近有明显的吸收峰[12]。在1,4-二氧六环溶液中,AL、ChCl-EG-P和ChCl-OA仅在240和280 nm处出现吸收峰,而210 nm处未出现吸收峰。通常木质素特征峰在280 nm处(苯环的吸收带),但油茶果壳木质素在氢氧化钠溶液中290 nm处出现吸收峰,可能是由于苯环的取代基不同,导致苯环上的π电子云密度降低,并且碱性溶液会使木质素中的酚羟基解离,从而导致最大吸收波长发生一定程度的位移[13]。此外,ChCl-GA在240~330 nm之间存在较宽吸收峰,可能是由于木质素中官能团互相导致出现特征吸收峰叠加现象,此峰型与曾诚等[14]已报道的甘蔗渣磨木木质素类似。
2.2 油茶果壳木质素相对分子量
油茶果壳木质素分子量大小受限于提取工艺,且会直接影响木质素物化性质。为了解四种油茶果壳木质素的相对分子量和分布均匀性,采用凝胶渗透色谱测量木质素样品的数均分子量(Mn)、重均分子量(Mw)和分散度(PDI),结果如表1所示。四种木质素分子量存在较大差异,AL的Mw为41858 g/mol,可能是氢氧化钠溶液提取的木质素结构中保留了大量的芳醚键(β-O-4),使AL具有较高的相对分子量。Pin等[15]利用[Etid][Lac]和[Etid][Ac]两种离子液体提取甘蔗渣的木质素分子量分别可达50010和31447 g/mol。然而,利用低共熔溶剂分离的三种木质素分别为10870、3451和2418 g/mol,这是由于低共熔溶剂可以解聚木质素分子结构中的芳醚键等化学键[16],使其降解为小分子物质溶出。此外,碱木质素的分散度较大(PDI:4.53),表明其分子量分布较广,而低共熔溶剂提取木质素的分散度均小于2,表明此类方法得到的木质素结构的均一性更高,其中利用三元低共熔溶剂体系(ChCl-乙二醇-对甲苯磺酸)提取的木质素分散度最小(PDI:1.37)。在木质素高值化精炼过程中,低分散度的木质素具有更好的生物化学稳定性。
表 1 油茶果壳木质素重均分子量(Mw)及其分散度(PDI:Mw/Mn)Table 1. Average molecular weights (Mw) and polydispersity indexes (PDI: Mw/Mn) of lignin isolated from Camellia oleifera shell木质素 Mn(g/mol) Mw(g/mol) PDI AL 9233 41858 4.53 ChCl-GA 7164 10870 1.51 ChCl-OA 1869 3451 1.84 ChCl-EG-P 1753 2418 1.37 2.3 油茶果壳木质素红外光谱分析
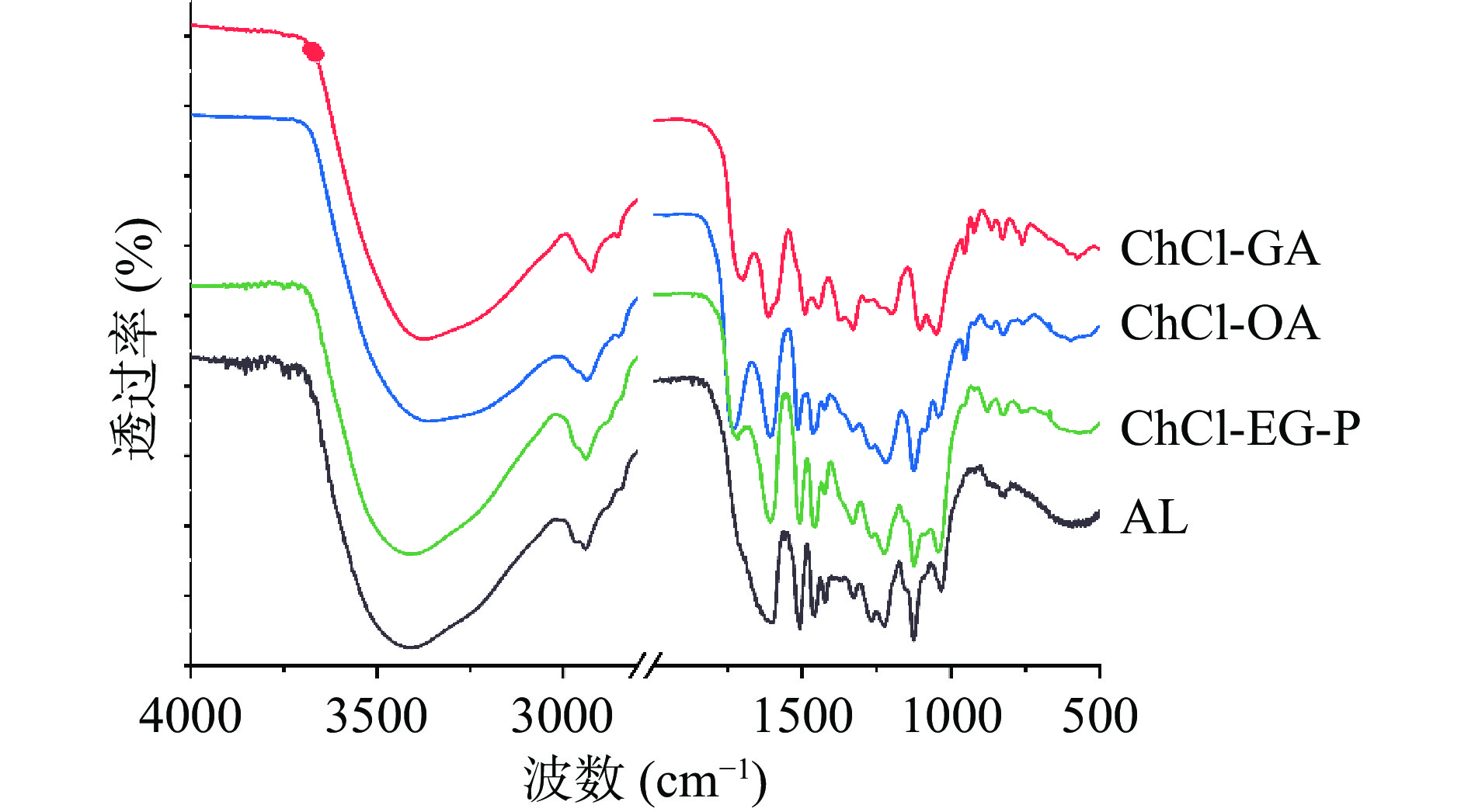
FTIR光谱图能够直观反应木质素的特征化学结构和功能基团,图2为4种木质素的红外吸收光谱图,参考已报道文献[17-19]列出了木质素分子结构的特征基团对应红外光谱吸收峰归属,见表2。四种木质素光谱图相似度较高,表明它们的化学结构和官能团组成较相似,由于官能团含量存在差异,导致特征吸收峰的强度差别较大。为比较不同方法提取木质素官能团的相对含量,以1518~1505 cm−1处的吸收峰(木质素的特征吸收峰,归属于芳香族苯环骨架振动)作为参比[13]。四种木质素均在3400、2950和2845 cm−1附近存在吸收峰,表明木质素结构中存在羟基、甲基、亚甲基和甲氧基。木质素中代表羟基特征峰(约3400 cm−1附近)与木质素特征峰(1518~1505 cm−1处的吸收峰)的吸收强度比值(I3400/I1518-1505),可以反映其羟基相对含量。AL、ChCl-GA、ChCl-OA和ChCl-EG-P的特征峰强度比值分别为0.76、0.83、1.08和0.75,ChCl-OA吸收峰强度比值较高,表明其含有羟基含量高于其他三种木质素。
表 2 油茶果壳木质素红外光谱吸收峰归属Table 2. Assigment of FTIR spectra of lignin isolated from Camellia oleifera shell波数(cm−1) 特征峰归属 3410~3360 羟基中O–H伸缩振动 2960~2940 苯环上甲氧基的C–H反对称振动 2850~2840 CH2和CH3 中C–H对称伸缩 1730~1700 非共轭的酮、羰基和酯基的C=O伸缩振动 1610~1590 苯环骨架振动与C=O伸缩振动; S>G: 缩合G>酯化G 1518~1505 苯环骨架振动(G>S) 1450~1440 CH3和CH2中的C–H不对称弯曲振动 1430~1420 苯环骨架振动结合C–H在平面变形 1370~1360 脂肪族CH3中的C–H拉伸 1330~1320 紫丁香基,缩合的S和G型(G型5位缩合) 1280~1260 愈创木酚基环和C=O伸缩振动 1230~1215 C–C、C–O和C=O伸缩振动(缩合G>醚化G) 1125 紫丁香环中C–H面内弯曲 1040~1030 芳香族 C–H 面内弯曲振动,伯醇中的C–O弯曲,C=O振动 955~950 –HC=CH平面外变形 920~915 C–H面内弯曲(芳香环) 880~860 C–H变形振动 830~820 芳香环2,6位C–H弯曲振动 低共熔溶剂提取的三种木质素在1730~1700 cm−1之间存在吸收峰,其归属于非共轭的酮、羰基或酯基的C=O伸缩振动,而碱木质素中不存在此吸收峰,表明低共熔溶剂在提取木质素过程中破坏了部分苯环结构并生成醌型结构[13]。四种木质素均在1610~1590、1518~1505和1430~1420 cm−1处存在较强吸收峰(归属于苯环骨架特征),这是木质素结构的特征峰,说明木质素提取过程中苯环骨架结构保留完好。此外,在1330~1320、1230~1215和1125 cm−1附近存在吸收峰归属于紫丁香基单元结构(S型),1280~1260 cm−1处吸收峰为愈创木酚基环(G型)和C=O伸缩振动,表明油茶果壳木质素属于典型的G-S型木质素。不同溶剂提取的油茶木质素中G/S相对含量,可以通过I1280-1260/I1330-1320比值大小来反映。AL、ChCl-GA、ChCl-OA和ChCl-EG-P中G/S相对比值分别为0.79、1.16、0.81和0.89,仅有ChCl-GA木质素比值大于1,说明此类木质素中愈创木酚基结构的相对含量比紫丁香基结构多[20]。综上所述,四种油茶果壳木质素主要由愈创木酚基和紫丁香基单元结构组成,在红外指纹区(1800~800 cm−1)出现的吸收峰均为木质素典型的红外吸收峰,证实了碱法和DES法能够较好保留油茶果壳木质素的完整性,但四种木质素中羟基含量、愈创木酚基和紫丁香基单元结构的含量存在明显差异。
2.4 油茶果壳木质素热稳定性评价
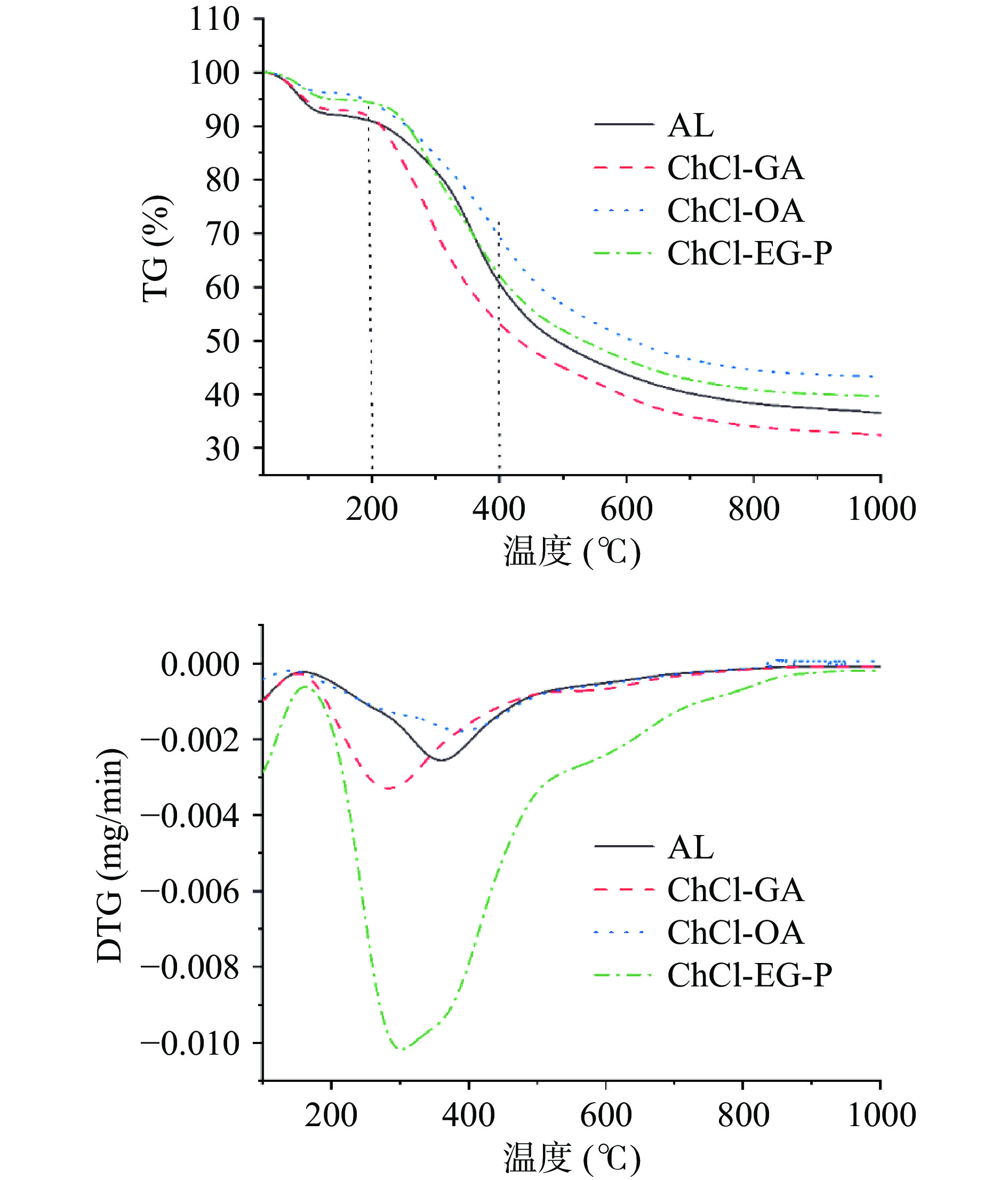
木质素是以苯丙烷单元结构为主体,由多种化学键连接而成的高分子有机化合物,化学键和官能团的类型及数量会直接影响其热解特性,可以通过该热解特性来评价不同方法提取的木质素化学结构中存在的差异。在升温速率为20 ℃/min,油茶果壳木质素从室温至1000 ℃的热失重曲线大致可分为三个阶段,如图3所示,四种木质素的热失重曲线存在较大差异。第一阶段为30~120 ℃之间,主要为木质素中的自由水和结合水的挥发,四种木质素失重率均未超过10%。第二阶段为200~400 ℃,四种木质素分解速率加速,失重率在24%~40%之间;此阶段木质素的热降解主要涉及化学键断裂,如C-O键和C-C键,以及侧链氧化,如羰基化、羧基化或脱氢反应等[21]。四种木质素在失重率和热分解速率上存在较大差异,表明木质素含有的β-O-4键、C-C键的含量及化学官能团类型和数量不同,其中ChCl-GA的失重最明显,说明其热稳定性较差。第三阶段为400 ℃以上,此阶段主要是木质素骨架结构苯环的C-C键裂解和脱甲氧基[22],所有木质素均呈现缓慢失重现象,700 ℃以后,木质素失重速率呈缓慢下降趋势,逐渐趋于平缓。温度升至1000 ℃时,ChCl-OA、ChCl-EG-P、AL和ChCl-GA的碳残渣分别为43.23%、39.67%、36.53%和32.43%。
此外,由DTG曲线可知,四种木质素的最大失重温度和失重峰峰型存在较大不同,ChCl-OA、AL、ChCl-EG-P和ChCl-GA的失重速率达到最大时的温度分别为391、362、304和283.3 ℃,最大失重速率依次为ChCl-EG-P>ChCl-GA>AL>ChCl-OA。综上所述,四种木质素的最大失重温度、热解失重速率和碳残渣存在明显差异,是由于四种木质素结构中化学键、官能团的种类和含量不同所导致。油茶果壳木质素的热稳定性依次为:ChCl-OA>AL>ChCl-EG-P>ChCl-GA,由于四种木质素的热稳定性存在差异,导致其后期研究应用也不同,比如ChCl-OA因其较好的热稳定性,更适合制备生物碳基高分子聚合材料。
2.5 油茶果壳木质素抗氧化活性
木质素中含有大量酚羟基,具备作为天然抗氧化剂的潜力。由图4可知,随着木质素浓度增加,四种木质素的DPPH自由基清除能力均逐渐增加,呈现出明显的浓度依赖关系。不同溶剂提取的木质素对DPPH自由基的清除能力存在较大差别,可能是由于木质素结构中酚羟基含量不同所导致的[23]。此外,当木质素浓度超过1.0 mg/mL时,AL、ChCl-OA和ChCl-EG-P的DPPH自由基清除率增长趋势放缓,维持在80%~87%之间,而ChCl-OA的DPPH自由基清除率呈现明显增加趋势。当木质素浓度为1.5 mg/mL时,AL、ChCl-OA、ChCl-EG-P和ChCl-GA的DPPH自由基清除率分别可达86.64%、83.87、86.67%和77.19%。IC50是自由基清除率达到50%时所需样品的质量浓度,其倒数为自由基清除指数(radical scavenging index,RSI),常作为抗氧化能力的评价,该值越大表明抗氧化活性越强[24]。经数据拟合计算得出AL、ChCl-OA、ChCl-EG-P和ChCl-GA的IC50分别为0.388、0.641、0.475和1.02 mg/mL,RSI依次分别为2.57、1.56、2.1和0.98,此结果表明碱木质素对DPPH自由基的清除能力大于低共熔溶剂法分离的木质素。李晗等[25]提取的油茶果壳乙酸木质素和碱木质素对DPPH自由基清除清除率分别为81.06%和73.36%。朱梦妮等[26]分析了碱法提取核桃壳、稻壳、玉米秸秆和芦苇木质素的抗氧化活性,当木质素浓度为0.4 mg/mL时,DPPH自由基的清除率在14.9%~53.5%之间。与已报道的研究相比,油茶果壳木质素表现出较好的DPPH自由基清除能力,表明油茶果壳木质素在食品、医药、包装等生物活性材料领域具有较好应用潜力。
3. 结论
本研究以油茶果壳为原料分别利用碱法和低共熔溶剂法提取分离得到四种木质素,并对其化学结构和潜在生物活性进行了评价。紫外和红外光谱图表明碱法和低共熔溶剂法提取分离木质素较完整保留了油茶果壳中原始木质素结构,属于典型G/S型木质素,由红外光谱特征吸收峰强度比值可知,ChCl-OA中羟基含量较多,ChCl-GA中愈创木酚基单元结构的相对含量高于紫丁香基单元结构。碱法提取油茶果壳木质素的相对分子量和分散度较大,而低共熔溶剂提取木质素分子量和分散度相对较低,表明低共熔溶剂分离的木质素结构均一性更好。从热重分析可知,与其他三种木质素相比,ChCl-GA热分解温度较低和热失重速率较高,表明其热稳定性较差;四种木质素热稳定性依次为:ChCl-OA>AL>ChCl-EG-P>ChCl-GA。此外,由DPPH自由基清除能力评价可知,当木质素浓度高于0.8 mg/mL后,AL、ChCl-EG-P和ChCl-OA对DPPH自由基清除率较相近,表现出具有较好抗氧化活性的潜力。
本研究利用低共熔溶剂高选择性木质素溶解体系,分离提取油茶果壳木质素,得到的木质素分子量分布较窄且生物活性较好,解决了传统化学试剂(如碱法)提取的木质素存在的匀质性差的问题,为开发清洁的木质素分离技术提供借鉴。本研究尚未完全阐明不同低共熔溶剂提取的木质素分子结构中存在的显著差异,如木质素中β-O-4、β-β、β-5、β-1等化学键和官能团(甲基、甲氧基和酚羟基等)所占比例等方面存在的差异。未来研究应着重以下两方面:a.对分离所得木质素结构进行全面解析,如利用核磁共振技术深入研究分离过程中木质素结构(主要化学键和官能团)的变化与潜在的抗氧化活性之间的关系;b.开发新颖低共熔溶剂体系,在分离过程中尽可能保护木质素的原始结构,尤其是β-O-4的保护。
-
表 1 油茶果壳木质素重均分子量(Mw)及其分散度(PDI:Mw/Mn)
Table 1 Average molecular weights (Mw) and polydispersity indexes (PDI: Mw/Mn) of lignin isolated from Camellia oleifera shell
木质素 Mn(g/mol) Mw(g/mol) PDI AL 9233 41858 4.53 ChCl-GA 7164 10870 1.51 ChCl-OA 1869 3451 1.84 ChCl-EG-P 1753 2418 1.37 表 2 油茶果壳木质素红外光谱吸收峰归属
Table 2 Assigment of FTIR spectra of lignin isolated from Camellia oleifera shell
波数(cm−1) 特征峰归属 3410~3360 羟基中O–H伸缩振动 2960~2940 苯环上甲氧基的C–H反对称振动 2850~2840 CH2和CH3 中C–H对称伸缩 1730~1700 非共轭的酮、羰基和酯基的C=O伸缩振动 1610~1590 苯环骨架振动与C=O伸缩振动; S>G: 缩合G>酯化G 1518~1505 苯环骨架振动(G>S) 1450~1440 CH3和CH2中的C–H不对称弯曲振动 1430~1420 苯环骨架振动结合C–H在平面变形 1370~1360 脂肪族CH3中的C–H拉伸 1330~1320 紫丁香基,缩合的S和G型(G型5位缩合) 1280~1260 愈创木酚基环和C=O伸缩振动 1230~1215 C–C、C–O和C=O伸缩振动(缩合G>醚化G) 1125 紫丁香环中C–H面内弯曲 1040~1030 芳香族 C–H 面内弯曲振动,伯醇中的C–O弯曲,C=O振动 955~950 –HC=CH平面外变形 920~915 C–H面内弯曲(芳香环) 880~860 C–H变形振动 830~820 芳香环2,6位C–H弯曲振动 -
[1] 夏美玲, 王允圃, 张淑梅, 等. 油茶壳综合利用研究进展[J]. 生物质化学工程,2021,55(6):26−38. [XIA M L, WANG Y P, ZHANNG S M, et al. Research progress on comprehensive utilization of Camellia oleifera Abel shell[J]. Biomass Chemical Engineering,2021,55(6):26−38. doi: 10.3969/j.issn.1673-5854.2021.06.004 [2] 陈沛均, 胡传双, 涂登云, 等. 油茶果壳综合利用进展与展望[J]. 林产工业,2021,58(5):60−64. [CHEN P J, HU C S, TU D Y, et al. Progress and prospect of comprehensive utilization of Camellia oleifera shells[J]. China Forest Products Industry,2021,58(5):60−64. doi: 10.19531/j.issn1001-5299.202105013 [3] AHMAD U M, JI N, LI H, et al. Can lignin be transformed into agrochemicals? Recent advances in the agricultural applications of lignin[J]. Industrial Crops and Products,2021,170:113646. doi: 10.1016/j.indcrop.2021.113646
[4] DE FRANCA SERPA J, DE SOUSA SILVA J, REIS C L B, et al. Extraction and characterization of lignins from cashew apple bagasse obtained by different treatments[J]. Biomass and Bioenergy,2020,141:105728. doi: 10.1016/j.biombioe.2020.105728
[5] LIU X, LI T, WU S, et al. Structural characterization and comparison of enzymatic and deep eutectic solvents isolated lignin from various green processes: Toward lignin valorization[J]. Bioresource Technology,2020,310:123460. doi: 10.1016/j.biortech.2020.123460
[6] MAGALHAES S, FILIPE A, MELRO E, et al. Lignin extraction from waste pine sawdust using a biomass derived binary solvent system[J]. Polymers,2021,13(7):1090. doi: 10.3390/polym13071090
[7] 崔兴凯, 赵雪冰, 刘德华. 五种甘蔗渣分离木质素热解特性及动力学[J]. 化工进展,2017,36(8):2910−2915. [CUI X K, ZHAO X B, LIU D H. Pyrolysis characteristics and kinetics of five isolated lignins from sugarcane bagasse[J]. Chemical Industry and Engineering Progress,2017,36(8):2910−2915. [8] PIN T C, NAKASU P Y S, MATTEDI S, et al. Screening of protic ionic liquids for sugarcane bagasse pretreatment[J]. Fuel,2018,235(1):1506−1514.
[9] WEI X, LIU Y, LUO Y, et al. Effect of organosolv extraction on the structure and antioxidant activity of eucalyptus kraft lignin[J]. International Journal of Biological Macromolecules,2021,187:462−470. doi: 10.1016/j.ijbiomac.2021.07.082
[10] FERNANDES C, MELRO E, MAGALHAES S, et al. New deep eutectic solvent assisted extraction of highly pure lignin from maritime pine sawdust (Pinus pinaster Ait.)[J]. International Journal of Biological Macromolecules,2021,177:294−305. doi: 10.1016/j.ijbiomac.2021.02.088
[11] 刘金科, 杨桂花, 齐乐天, 等. 胆碱类低共熔溶剂选择性分离杨木中木质素的研究[J]. 中国造纸,2020,39(4):1−9. [LIU J K, YANG G H, QI L T, et al. Selective extraction of poplar pignin with choline-based deep eutectic solvents[J]. China Pulp & Paper,2020,39(4):1−9. [12] 金春德, 杨巍, 韩申杰, 等. 制造无胶纤维板过程中木质素的变化规律—以酸性蒸气蒸煮热磨制造方法为例[J]. 东北林业大学学报,2014,42(4):89−92. [JIN C D, YANG W, HAN S J, et al. Change rule of the lignin in the manufacture process of the binder less fiberboard used wood fiber by the acidic steam steaming hot-milling method[J]. Journal of Northeast Forestry University,2014,42(4):89−92. doi: 10.3969/j.issn.1000-5382.2014.04.020 [13] 崔兴凯, 陈可, 赵雪冰, 等. 甘蔗渣木质素的结构及其对纤维素酶解的影响[J]. 过程工程学报,2017,17(5):1002−1010. [CUI X K, CHEN K, ZHAO X B, et al. Structures of several lignins isolated from sugarcane bagasse and their effects on enzymatic hydrolysis of cellulose[J]. The Chinese Journal of Process Engineering,2017,17(5):1002−1010. doi: 10.12034/j.issn.1009-606X.216376 [14] 曾诚, 宋国杰, 孙海彦, 等. 甘油预处理蔗渣的木质素分离提取及结构表征[J]. 化工进展,2020,39(11):4418−4426. [ZENG C, SONG G J, SUN H Y, et al. Isolation and structural characterization of glycerol extracted sugarcane bagasse lignin[J]. Chemical Industry and Engineering Progress,2020,39(11):4418−4426. doi: 10.16085/j.issn.1000-6613.2020-0125 [15] PIN T C, NASCIMENTO V M, COSTA A C, et al. Structural characterization of sugarcane lignins extracted from different protic ionic liquid pretreatments[J]. Renewable Energy,2020,161:579−592. doi: 10.1016/j.renene.2020.07.078
[16] BRANDT A, CHEN L, VAN DONGEN B E, et al. Structural changes in lignins isolated using an acidic ionic liquid water mixture[J]. Green Chemistry,2015,17(11):5019−5034. doi: 10.1039/C5GC01314C
[17] POPOVA Y A, SHESTAKOV S L, BELESOV A V, et al. Comprehensive analysis of the chemical structure of lignin from raspberry stalks (Rubus idaeus L.)[J]. International Journal of Biological Macromolecules,2020,164:3814−3822. doi: 10.1016/j.ijbiomac.2020.08.240
[18] WANG L, LI X, JIANG J, et al. Revealing structural and functional specificity of lignin from tobacco stalk during deep eutectic solvents deconstruction aiming to targeted valorization[J]. Industrial Crops and Products,2022,180:114696. doi: 10.1016/j.indcrop.2022.114696
[19] RAMAKOTI B, DHANAGOPAL H, DEEPA K, et al. Solvent fractionation of organosolv lignin to improve lignin homogeneity: Structural characterization[J]. Bioresource Technology Reports,2019,7:100293. doi: 10.1016/j.biteb.2019.100293
[20] 杨增玲, 梅佳琪, 曹聪, 等. 基于红外光谱的不同农作物秸秆磨木木质素差异表征[J]. 农业工程学报,2018,34(19):219−224. [YANG Z L, MEI J Q, CAO C, et al. Traits of milled wood lignin isolated from different crop straw based on FT-IR[J]. Transactions of the Chinese Society of Agricultural Engineering,2018,34(19):219−224. doi: 10.11975/j.issn.1002-6819.2018.19.028 [21] LIN X, SUI S, TAN S, et al. Fast pyrolysis of four lignins from different isolation processes using Py-GC/MS[J]. Energies,2015,8(6):5107−5121. doi: 10.3390/en8065107
[22] 王则祥, 李航, 谢文銮, 等. 木质素基本结构、热解机理及特性研究进展[J]. 新能源进展,2020,8(1):6−14. [WANG Z X, LI H, XIE W L, et al. Progress in basic structure, pyrolysis mechanism and characteristics of lignin[J]. Advances in New and Renewable Energy,2020,8(1):6−14. doi: 10.3969/j.issn.2095-560X.2020.01.002 [23] UGARTONDO V, MITJANS M, VINARDELL M P. Comparative antioxidant and cytotoxic effects of lignins from different sources[J]. Bioresource Technology,2008,99(14):6683−6687. doi: 10.1016/j.biortech.2007.11.038
[24] 龚卫华, 冉占祥, 向卓亚, 等. 笋壳醋酸木质素的提取及抗氧化活性研究[J]. 食品与发酵工业,2016,42(11):225−229. [GONG W H, RAN Z X, XIANG Z Y, et al. Extraction and antioxidant activities of lignin from bamboo shoot shell[J]. Food and Fermentation Industries,2016,42(11):225−229. doi: 10.13995/j.cnki.11-1802/ts.201611039 [25] 李晗, 杨威岭, 杨宗玲, 等. 油茶壳木质素理化性质及表征[J]. 食品工业科技,2021,42(4):33−38. [LI H, YANG W L, YANG Z L, et al. Physicochemical properties and structural characterization of lignin from Camellia oleifera shell[J]. Science and Technology of Food Industry,2021,42(4):33−38. doi: 10.13386/j.issn1002-0306.2020050136 [26] 朱梦妮, 田维珍, 王兴, 等. 不同来源木质素抗氧化活性研究[J]. 中国造纸学报,2019,34(4):14−20. [ZHU M N, TIAN W Z, WANG X, et al. Chemical structure and antioxidant activity of different sources of lignin[J]. Transactions of China Pulp and Paper,2019,34(4):14−20. doi: 10.11981/j.issn.1000-6842.2019.04.14






 下载:
下载:

 下载:
下载:
