Optimization of Preparation of Galactooligosaccharides by β-Galactosidase Using Response Surface Methodology
-
摘要: 本文以乳糖为起始原料,在单因素实验的基础上,结合响应面分析法考察加酶量、反应温度、反应时间、反应pH等因素对低聚半乳糖总产率和低聚半乳四糖产率的影响,优化β-半乳糖苷酶法制备低聚半乳糖工艺。结果表明,β-半乳糖苷酶法制备低聚半乳糖的最佳工艺参数为起始乳糖浓度300 g/L、加酶量8.25 U/g乳糖、反应温度49 ℃、反应时间16 h、反应pH5.6。在此条件下,低聚半乳糖总产率为14.61%,低聚半乳四糖产率为3.31%。该方法针对性提高高聚合度低聚半乳糖的产率,可为低聚半乳糖的功能性应用及特医食品的研发提供参考。Abstract: In this study, lactose was used as raw material, on the basis of single factor experiment and combined with response surface methodology, enzyme addition, reaction temperature, reaction time, reaction pH and other factors were utilized to investigate the influence of the galactooligosaccharides total yield and the galactotetraose yield. The process of enzymatic preparation of galactooligosaccharides by β-galactosidase was optimized. The results showed that the optimum process parameters for the enzymatic preparation of galactooligosaccharides were as follows: The initial lactose concentration was 300 g/L, the amount of enzyme added was 8.25 U/g lactose, the reaction temperature was 49 ℃, the reaction time was 16 h, and the reaction pH was 5.6. Under these conditions, the galactooligosaccharides total yield was 14.61% and the galactotetraose yield was 3.31%. The method selectively improved the yield of galactooligosaccharides with high degree of polymerization, which would provide a certain theoretical reference for the functional application of galactooligosaccharides and the further study and development of special medical food.
-
低聚半乳糖(Galactooligosaccharides,GOS)是一种具有天然益生元属性的功能性低聚糖[1],其分子结构一般是在葡萄糖或半乳糖分子上连接1~7个半乳糖基,即Gal-(Gal)n-Glc/Gal(n为0~6)。研究表明,低聚半乳糖具有调节肠道菌群结构[2-3]、促进矿物质吸收[4-5]、提高免疫调节[6-7]、预防癌症[8-9]及改善炎症性肠病[10-11]等功能,因其具有优越的生理功能和理化性质而成为近年来国内外关注的热点。
低聚半乳糖的制备方法主要有如下几种:一是从自然界中提取,其成本高、产量低且分离困难;二是酸法水解天然多糖,但副反应较多,增大了后续纯化的难度;三是化学合成,步骤繁琐、得率低,且存在环境污染的风险,仅限于实验室研究;四是酶法合成,其操作简便、成本低,是目前生产GOS最理想的方法[12-15]。但目前GOS的商品化生产旨在生产更纯净和更高效的产品[16],多以GOS的产率及纯度作为衡量标准,对GOS的具体组成及特定健康效应没有太多关注[17-18]。本实验室前期研究表明,聚合度较高的GOS(如聚合度为4的低聚半乳四糖,Degree of Polymerization is 4,DP4),其体外抗炎活性也更强。因此,在保证GOS总产率情况下,提高高聚合度GOS产率成为本文研究的重点。
本研究以乳糖为原料,研究β-半乳糖苷酶的不同来源及酶催化反应的不同条件(底物浓度、酶添加量、反应温度、反应时间和反应pH)对GOS总产率及低聚半乳四糖(DP4)产率的影响,通过Box-Behnken响应面分析法对β-半乳糖苷酶法合成GOS工艺进行优化,以期在保证GOS总产率的前提下,选择性地提高低聚半乳四糖产率,为低聚半乳糖的功能性应用和特医食品的研究开发提供参考。
1. 材料与方法
1.1 材料与仪器
β-半乳糖苷酶(黑曲霉、大肠杆菌、米曲霉来源) 上海瑞永生物科技有限公司;乳糖、邻硝基苯β-D-半乳吡喃糖苷(ONPG)、邻硝基苯酚、碳酸钠、磷酸二氢钠、磷酸氢二钠 均为分析纯;实验用水 均为超纯水。
LC1200高效液相色谱仪 美国Agilent;DF-101S集热式恒温加热磁力搅拌器 巩义市孝义合众仪器供应站;FE28 pH计 梅特勒-托利多仪器(上海)有限公司;SHA-8水浴恒温振荡器 金坛区水北科普实验仪器厂;CR22GⅢ高速冷冻离心机 日本HITACHI。
1.2 实验方法
1.2.1 不同来源的β-半乳糖苷酶对合成GOS的影响
首先参考GB/T 33409-2016 β-半乳糖苷酶活性检测方法[19],对黑曲霉来源、大肠杆菌来源、米曲霉来源的β-半乳糖苷酶的水解活性进行测定。然后以0.1 mol/L、pH6.5的磷酸二氢钠-磷酸氢二钠缓冲液溶解乳糖,配制100 mL浓度为300 g/L乳糖底物置于250 mL酶反应容器中,以6 U/g乳糖的加酶量分别加入黑曲霉来源、大肠杆菌来源、米曲霉来源的β-半乳糖苷酶,置于50 ℃的水浴摇床120 r/min反应12 h,反应液于沸水浴灭酶20 min,8000 r/min离心10 min,取上清液过0.22 μm水相滤膜,利用高效液相色谱法分析产物中糖类物质的组成,考察不同来源的β-半乳糖苷酶对GOS产率、DP4产率的影响。
1.2.2 单因素实验
1.2.2.1 起始乳糖浓度对合成GOS的影响
以0.1 mol/L、pH6.5的磷酸二氢钠-磷酸氢二钠缓冲液溶解乳糖,分别配制成100 mL不同浓度(200、300、400、500、600 g/L)的乳糖底物置于250 mL酶反应容器中,在加酶量6 U/g乳糖的条件下,置于50 ℃的水浴摇床120 r/min反应12 h,反应液于沸水浴灭酶20 min,8000 r/min离心10 min,取上清液过0.22 μm水相滤膜,利用高效液相色谱法分析产物中糖类物质的组成,考察不同起始乳糖浓度对GOS产率、DP4产率的影响。
1.2.2.2 加酶量对合成GOS的影响
以0.1 mol/L、pH6.5的磷酸二氢钠-磷酸氢二钠缓冲液配制100 mL浓度为300 g/L乳糖底物置于250 mL酶反应容器中,分别加入2、4、6、8、10 U/g的β-半乳糖苷酶,置于50 ℃的水浴摇床120 r/min反应12 h,反应液于沸水浴灭酶20 min,8000 r/min离心10 min,取上清液过0.22 μm水相滤膜,利用高效液相色谱法分析产物中糖类物质的组成,考察不同的β-半乳糖苷酶添加量对GOS产率、DP4产率的影响。
1.2.2.3 反应温度对合成GOS的影响
以0.1 mol/L、pH6.5的磷酸二氢钠-磷酸氢二钠缓冲液配制100 mL浓度为300 g/L乳糖底物置于250 mL酶反应容器中,各加入8 U/g的β-半乳糖苷酶,置于不同反应温度(30、40、50、60、70 ℃)的水浴摇床120 r/min反应12 h,反应液于沸水浴灭酶20 min,8000 r/min离心10 min,取上清液过0.22 μm水相滤膜,利用高效液相色谱法分析产物中糖类物质的组成,考察不同的反应温度对GOS产率、DP4产率的影响。
1.2.2.4 反应时间对合成GOS的影响
以0.1 mol/L、pH6.5的磷酸二氢钠-磷酸氢二钠缓冲液配制100 mL浓度为300 g/L乳糖底物置于250 mL酶反应容器中,各加入8 U/g的β-半乳糖苷酶,置于50 ℃的水浴摇床120 r/min分别反应(4、8、12、16、20 h),反应液于沸水浴灭酶20 min,8000 r/min离心10 min,取上清液过0.22 μm水相滤膜,利用高效液相色谱法分析产物中糖类物质的组成,考察不同的反应时间对GOS产率、DP4产率的影响。
1.2.2.5 反应pH对合成GOS的影响
以0.1 mol/L、不同pH(4.5、5.5、6.5、7.5、8.5)的磷酸二氢钠-磷酸氢二钠缓冲液配制100 mL浓度为300 g/L乳糖底物置于250 mL酶反应容器中,各加入8 U/g的β-半乳糖苷酶,置于50 ℃的水浴摇床120 r/min反应16 h,反应液于沸水浴灭酶20 min,8000 r/min离心10 min,取上清液过0.22 μm水相滤膜,利用高效液相色谱法分析产物中糖类物质的组成,考察不同的反应pH对GOS产率、DP4产率的影响。
1.2.3 响应面试验
综合单因素实验的结果,以加酶量(A)、反应温度(B)、反应时间(C)、反应pH(D)为自变量,以GOS产率(Y1)、DP4产率(Y2)为响应值,采用Box-Behnken响应面设计法对合成条件在四因素三水平上进行工艺参数的优化。试验因素与水平设计见表1。
表 1 响应面试验因素水平设计Table 1. Factors and levels of response surface methodology水平 因素 A加酶量(U/g) B反应温度(℃) C反应时间(h) D反应pH −1 6 40 12 4.5 0 8 50 16 5.5 1 10 60 20 6.5 1.2.4 β-半乳糖苷酶的活性检测
参考GB/T 33409-2016 β-半乳糖苷酶活性检测方法[19]。pH7.3的磷酸缓冲液适用大肠杆菌来源的β-半乳糖苷酶,pH4.5的磷酸缓冲液适用黑曲霉、米曲霉来源的β-半乳糖苷酶。精确称取酶粉1.0 mg,用相应的反应缓冲液溶解后,定容至100 mL,利用分光光度计法测定β-半乳糖苷酶活性。以邻硝基苯酚为标准品绘制标准曲线,得到线性回归方程:YpH7.3=4.0549x+0.0085,R²pH7.3=0.9998;YpH4.5=1.8251x+0.0074,R²pH4.5=0.9992。
酶活力计算公式如下:
式中:c表示测定液中邻硝基苯酚的浓度,从对应的标准曲线中得出,mmol/L;8为反应试剂的总体积,mL;D表示稀释倍数;1表示参与反应酶液的体积,mL;10为反应时间,min;V表示溶解酶粉的液体体积,mL;m表示称取酶粉的质量,g。
1.2.5 GOS产率的测定和DP4产率的测定
测定方法采用高效液相色谱法(HPLC)。色谱条件:Agilent 1200型高效液相色谱,蒸发光散射检测器(雾化温度30 ℃,蒸发温度30 ℃,气体流速1.6 SLM),色谱柱为Agilent Hi-Plex(300 mm×7.7 mm,8 µm),柱温80 ℃,流动相为超纯水,流速0.6 mL/min,进样量10 μL。按照以上色谱条件对反应样品进行测定分析。
根据反应产物中各糖类物质在HPLC上的峰面积,用外标法对GOS与DP4产率进行绝对定量计算。其计算公式如下:
式中:cGOS表示反应产物中GOS的浓度,从标准曲线中得出,μg/mL;V表示反应终止时反应液的体积,mL;D表示稀释倍数;mLac表示乳糖初始添加的质量,mg;cDP4表示反应产物中DP4的浓度,从标准曲线中得出,μg/mL。
1.3 数据处理
实验数据为3次重复平均值,采用SPSS 21.0软件进行单因素方差分析(One-way ANOVA)和Duncan's多重差异显著分析,显著性水平P<0.05,不同字母代表组间显著性差异。采用GraphPad Prism 7软件做图,Design Expert 12.0进行响应面试验设计。
2. 结果与分析
2.1 GOS和DP4标准曲线的绘制
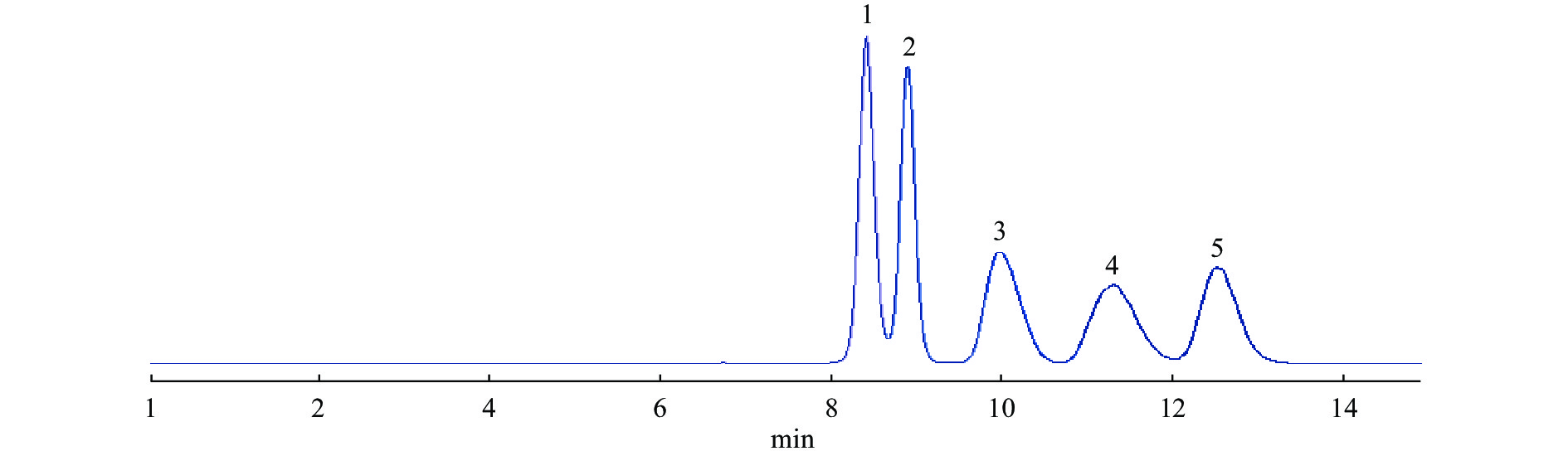
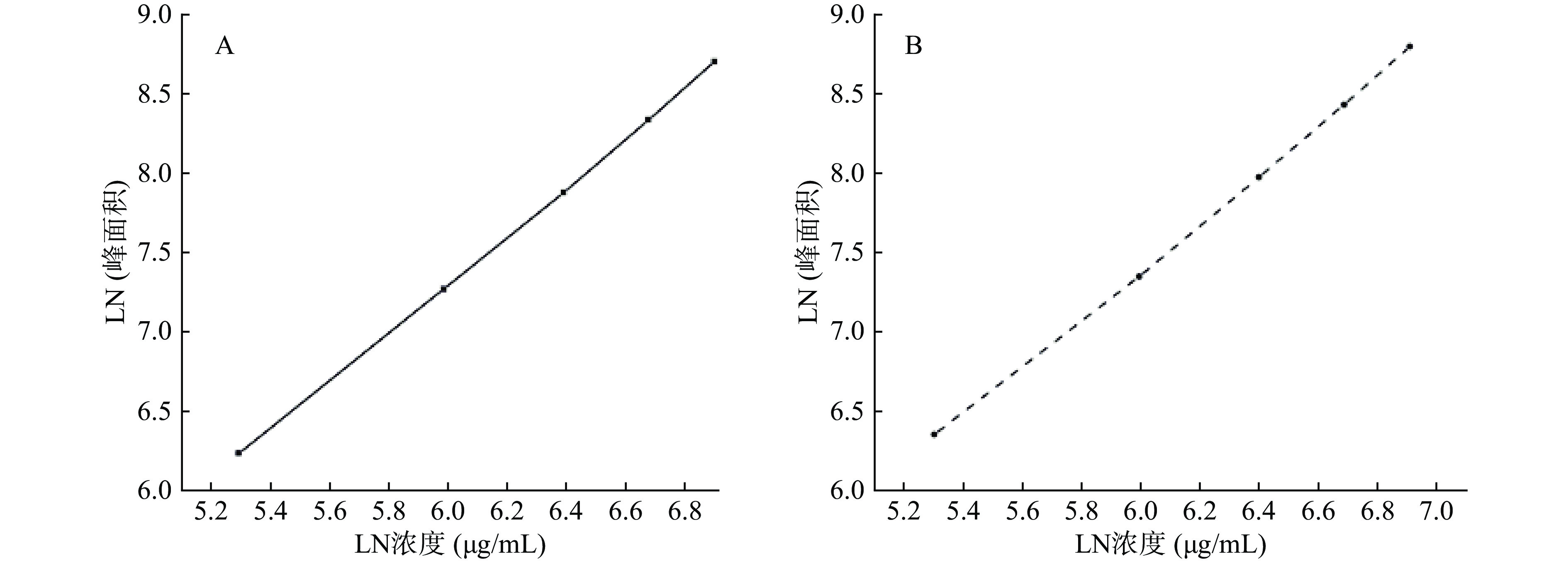
各标准品HPLC色谱图见图1,以标准品峰面积的自然对数值为纵坐标,以标准品浓度(μg/mL)的自然对数值为横坐标,进行线性回归,得到标准曲线(图2,以低聚半乳三糖和低聚半乳四糖的峰面积之和为总GOS峰面积)。经回归处理得线性回归方程:YGOS=1.523x−1.8329,R²GOS=0.9996;YDP4=1.5172x−1.7069,R²DP4=0.9993。
2.2 不同酶来源对合成GOS的影响
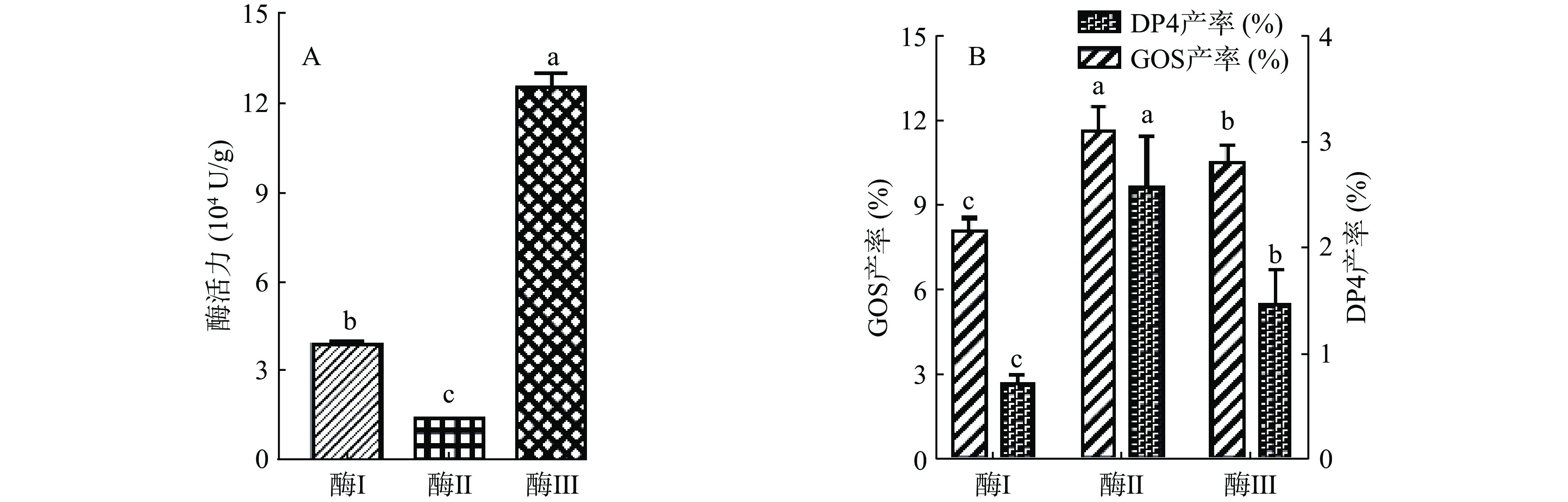
GOS的合成与β-半乳糖苷酶的反应机制密切相关,GOS合成过程中发生两类反应:一是乳糖的水解反应,二是转半乳糖基反应,而GOS正是转糖基反应的产物,因此GOS产率取决于这两种反应的平衡[18]。不同来源的酶具有不同的特性,对于水和糖具有不同的选择性,不同酶之间的结构特征或其反应机制也有所差异,从而导致GOS产率和高聚合度GOS(如DP4)的产率有所不同[20-21]。通过酶水解活力测定发现三种β-半乳糖苷酶的水解活性强弱:米曲霉来源(酶Ⅲ)>黑曲霉来源(酶Ⅰ)>大肠杆菌来源(酶Ⅱ)(图3A);在酶添加量、底物浓度、反应温度、反应pH、反应时间完全相同的条件下,测定比较GOS总产率及DP4产率,分析得出三种β-半乳糖苷酶的转糖基活性强弱:大肠杆菌来源(酶Ⅱ)>米曲霉来源(酶Ⅲ)>黑曲霉来源(酶Ⅰ)(图3B)。综上可知,相同酶添加量(U/g乳糖)的条件下,虽然大肠杆菌来源的β-半乳糖苷酶的转糖基活性更强,但因其单位质量的酶活力很低,故需消耗的酶量大,成本较高,因此兼顾到GOS产率以及经济成本,选用米曲霉来源的β-半乳糖苷酶进行接下来的实验。
2.3 不同反应条件对GOS合成的影响
2.3.1 起始乳糖浓度对合成GOS的影响
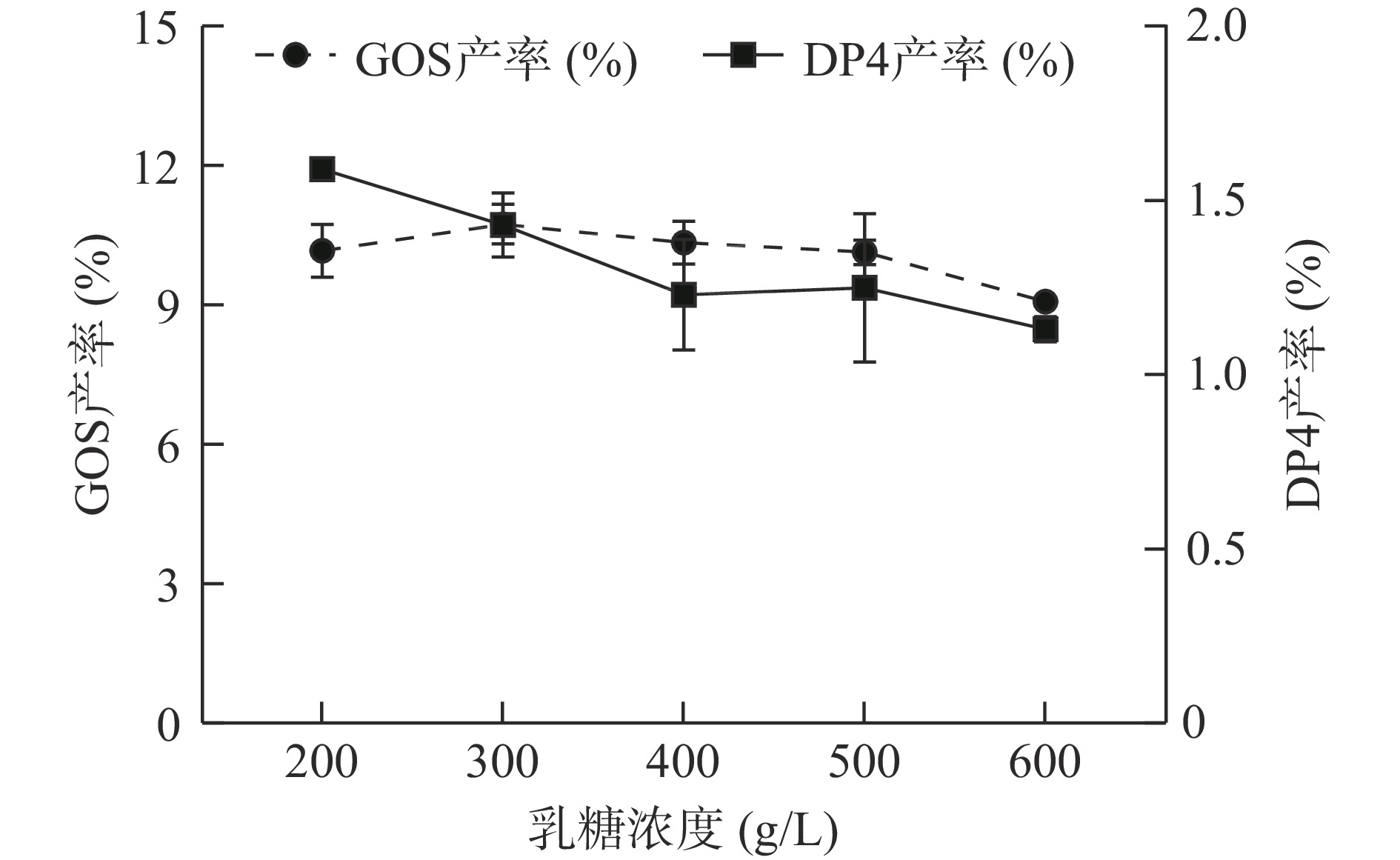
在一定的加酶量、反应温度、反应时间、反应pH条件下,以不同起始浓度的乳糖合成GOS,其结果如图4所示。随着乳糖起始浓度的增加,GOS产率逐渐增加,于300 g/L时达到最大值10.74%,这可能是随着乳糖起始浓度的提高,一方面增加了半乳糖受体的量,另一方面降低了水活度,从而更容易发生转糖基反应,生成GOS[22];当乳糖初始浓度从300 g/L继续增加到600 g/L时,其GOS产率逐渐下降,这可能是由于在高乳糖浓度下,β-半乳糖苷酶催化活性受到抑制,致使其水解和转苷作用同时降低[23]。同时,随着乳糖浓度的增加,DP4产率逐渐降低。综合考虑原料的充分利用以及GOS产率等因素,选用300 g/L的乳糖起始浓度进行后续的实验。
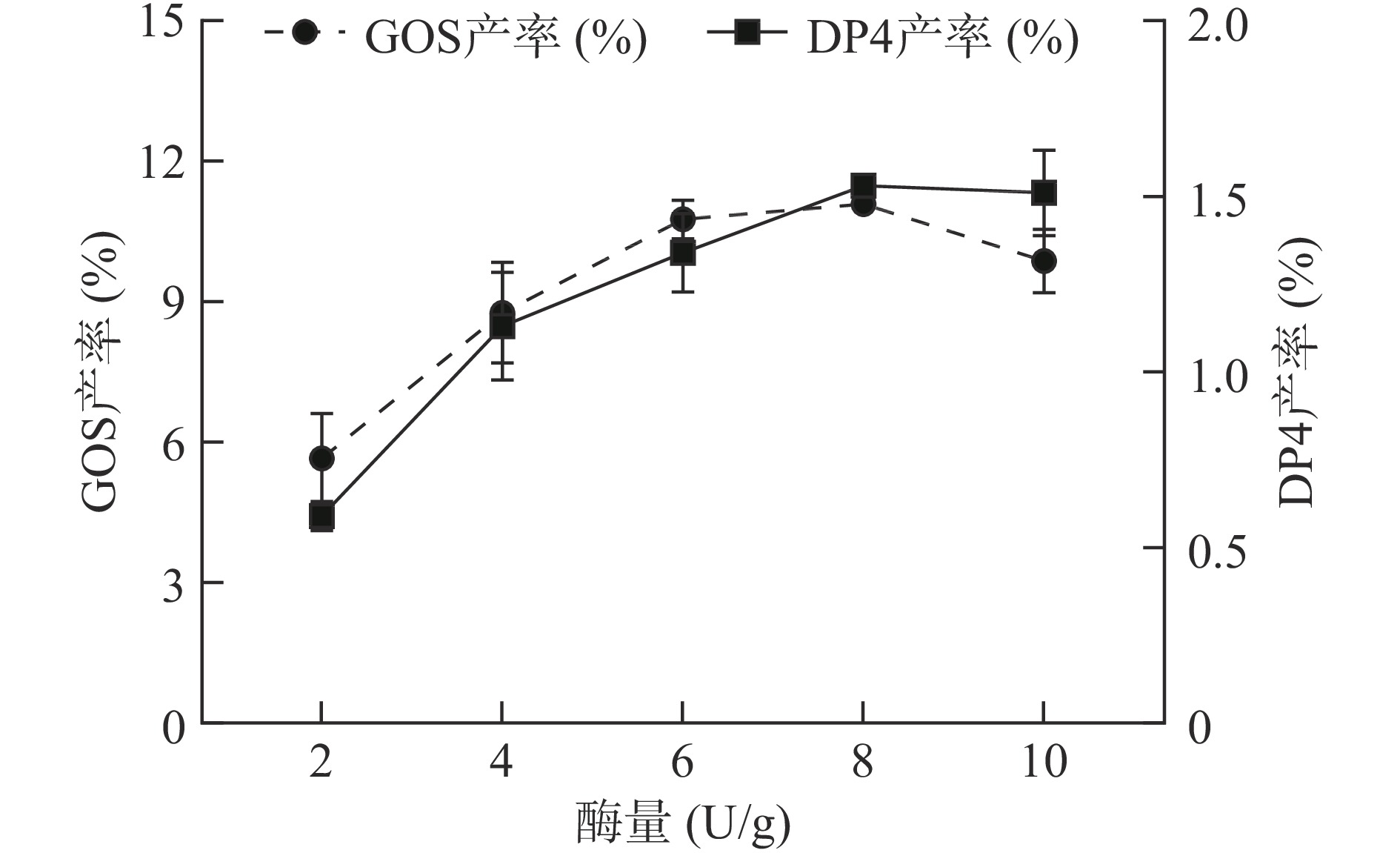
2.3.2 加酶量对合成GOS的影响
在乳糖起始浓度、反应温度、反应时间、反应pH一定的条件下,以不同加酶量合成GOS,其结果如图5所示。当加酶量为8 U/g时,GOS产率为11.09%±0.19%,DP4产率为1.53%±0.02%;继续提高酶添加量,GOS产率与DP4产率没有明显增加。总体而言,在一定的加酶量范围内,随着β-半乳糖苷酶添加量的增多,GOS产率、DP4产率也随之提高。这可能是因为在反应体系中,酶与底物络合,使得GOS产率增加;而当加酶量过高时,不能充分利用β-半乳糖苷酶,同时产生的副产物影响GOS的合成[24]。综合考虑酶的利用效率、GOS产率及DP4产率,选用加酶量8 U/g进行后续实验。
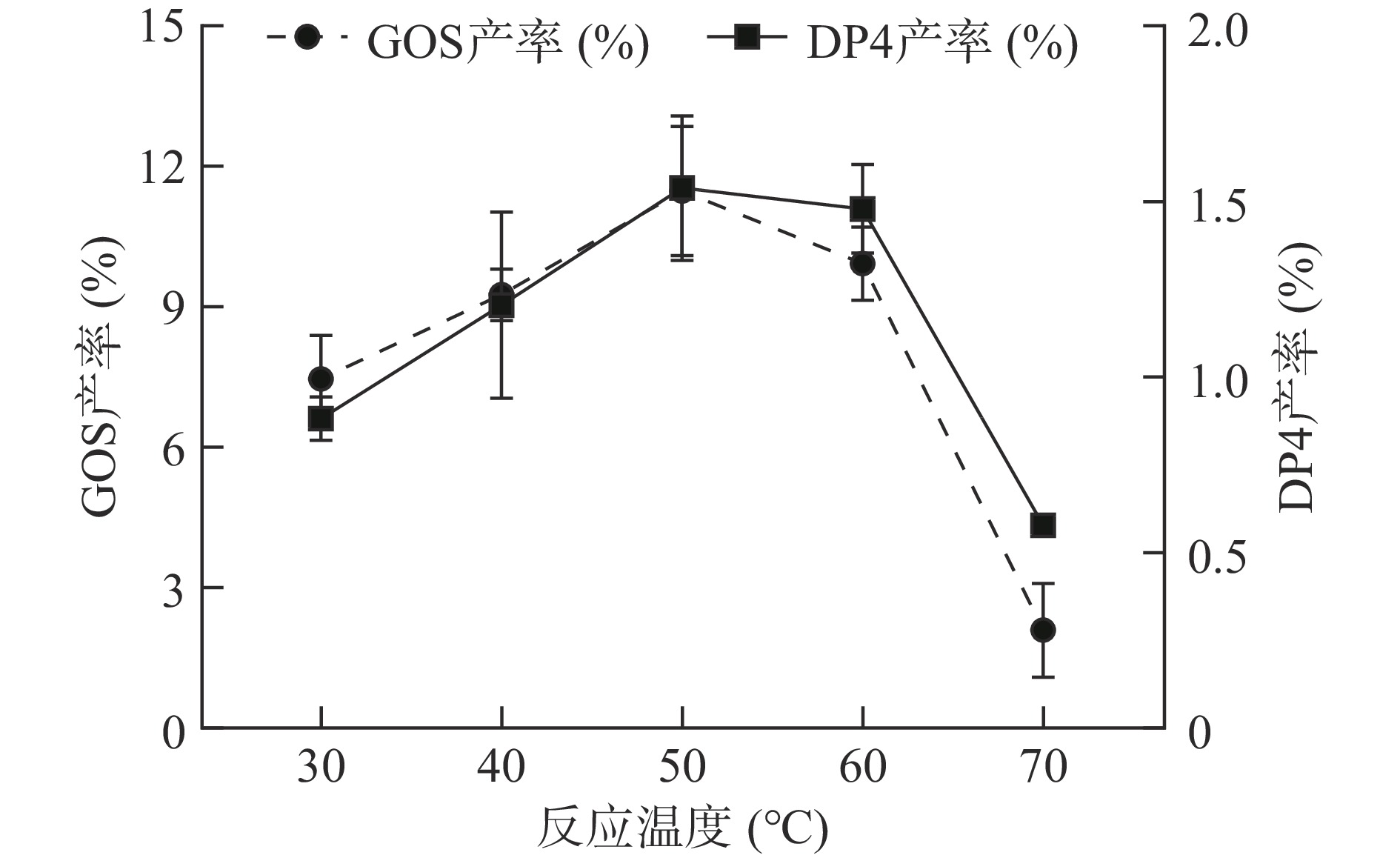
2.3.3 反应温度对合成GOS的影响
在乳糖浓度、加酶量、反应时间和反应pH固定的条件下,以不同的反应温度合成GOS,结果如图6所示。当反应温度低于50 ℃时,GOS产率及DP4产率随反应温度的升高而增加,这是因为适当升高温度不仅可以增加乳糖的溶解度,而且促进反应体系中分子间相互作用,从而促进GOS的合成,使得GOS产率及DP4产率提高。而当温度高于50 ℃时,高温使得β-半乳糖苷酶变性失活,不利于GOS合成[25]。因此,考虑到酶的热稳定性,选取最适温度为50 ℃进行后续实验。
2.3.4 反应时间对合成GOS的影响
如图7所示,在乳糖浓度、加酶量、反应温度和反应pH一定时,随着反应时间的增加,其GOS合成产率呈现出先升高后下降的趋势,这可能是反应时间过长,底物浓度降低,导致转糖苷作用减弱,而合成的GOS可能又会发生水解,最终使得GOS总产率下降[26]。随着反应时间的增加,DP4产率却逐渐升高,可能是反应时间的延长有利于高聚合度GOS的合成。综合考虑GOS产率及DP4产率,选取反应16 h进行后续实验。
2.3.5 反应pH对合成GOS的影响
由图8可知,反应pH为4.5~5.5时,GOS合成产率增加,在反应pH5.5时,GOS产率为12.03%±0.53%,达到最高;当pH高于5.5时,GOS产率随着pH的升高而下降,造成这种现象的原因可能是:米曲霉来源的β-半乳糖苷酶在酸性条件下,酶的催化活性更强,具有最适反应pH。而当反应pH提高,DP4产率逐渐下降,可能是高聚合度的GOS发生了水解的缘故。综上所述,确定该反应体系的最适pH为5.5。
2.4 响应面试验结果
在单因素实验的基础上,选定加酶量8 U/g、反应温度50 ℃、反应时间16 h、反应pH5.5为响应面Box-Behnken试验的中心点,GOS产率(Y1)与DP4产率(Y2)为响应值,对Box-Behnken试验结果进行方差分析和多元线性回归二项式拟合,响应面试验设计及结果如表2。
表 2 Box-Behnken试验设计及响应值Table 2. Design and response value of Box-Behnken experiment实验号 A B C D Y1(%) Y2(%) 1 0 0 0 0 14.78 3.15 2 0 −1 1 0 11.01 2.26 3 0 1 −1 0 10.17 2.00 4 −1 −1 0 0 9.61 1.64 5 1 0 −1 0 10.58 2.11 6 0 1 0 1 9.77 1.91 7 0 0 −1 1 11.24 2.43 8 0 0 0 0 14.85 3.30 9 0 0 0 0 14.52 3.26 10 1 0 1 0 10.25 2.09 11 −1 1 0 0 8.58 1.56 12 −1 0 −1 0 9.54 1.61 13 0 0 1 1 10.94 2.19 14 0 −1 0 −1 9.89 1.65 15 0 1 0 −1 9.98 1.94 16 1 0 0 1 10.83 2.37 17 0 0 1 −1 10.75 2.31 18 −1 0 0 1 9.41 1.41 19 0 1 1 0 8.34 1.38 20 1 1 0 0 9.92 2.20 21 0 −1 −1 0 9.85 1.67 22 1 −1 0 0 10.3 2.25 23 0 0 0 0 14.49 3.49 24 −1 0 0 −1 10.02 1.72 25 0 0 −1 −1 10.04 1.99 26 1 0 0 −1 9.57 1.60 27 0 −1 0 1 11.07 2.39 28 −1 0 1 0 9.78 1.71 2.4.1 GOS产率的回归模型及方差分析
对表2中GOS产率(Y1)相关数据进行多元二次回归拟合及方差分析,分析结果见表3。
表 3 Y1回归模型方差分析结果Table 3. Variance analysis of regression model of Y1来源 平方和 自由度 均方 F值 P值 显著性 模型 98.70 14 7.05 102.40 <0.0001 ** A 1.70 1 1.70 24.62 0.0002 ** B 2.06 1 2.06 29.90 <0.0001 ** C 0.0102 1 0.0102 0.1483 0.7060 D 0.7550 1 0.7550 10.97 0.0051 ** AB 0.1056 1 0.1056 1.53 0.2358 AC 0.0812 1 0.0812 1.18 0.2957 AD 0.8742 1 0.8742 12.70 0.0031 ** BC 2.24 1 2.24 32.46 <0.0001 ** BD 0.4830 1 0.4830 7.02 0.0191 * CD 0.2550 1 0.2550 3.70 0.0748 A2 43.52 1 43.52 632.14 <0.0001 ** B2 43.10 1 43.10 626.05 <0.0001 ** C2 28.00 1 28.00 406.74 <0.0001 ** D2 24.67 1 24.67 358.35 <0.0001 ** 失拟项 0.8648 10 0.0865 3.49 0.1198 误差 0.0991 4 0.0248 总和 99.66 28 决定系数R2 0.9903 校正决定系数R2Adj 0.9807 注:*表示差异显著,P<0.05;**表示差异极显著,P<0.01;表4同。 根据表3试验结果,得到回归方程(1)为:
Y1=14.66+0.3758A−0.4142B−0.292C+0.2508D+0.1625AB−0.1425AC+0.4675AD−0.7475BC−0.3475BD−0.2535CD−2.59A2−2.58B2−2.08C2−1.95D2 式(1)
由表3的方差分析结果可知,模型的P<0.0001,极显著;失拟项P=0.1198>0.05,不显著,说明该模型成立。模型的决定系数R2=0.9909,校正决定系数R2Adj=0.9807,变异系数为2.42%,说明拟合度较好,置信度较高,实验操作可行,可以用此模型来预测低聚半乳糖合成工艺。
该回归模型中的一次项A、B、D,二次项A2、B2、C2、D2的P值均小于0.01,具极显著性,由F值可知,四个因素对GOS产率的影响大小依次为B(反应温度)>A(加酶量)>D(反应pH)>C(反应时间)。交互项中AD、BC的P值小于0.01,BD的P值小于0.05,说明加酶量和反应pH、反应温度和反应时间及反应温度和反应pH交互作用显著。
2.4.2 GOS产率的响应面分析
利用Design-Expert 12.0软件对四个因素的交互作用进行分析,选取了AD、BC、BD这三组响应面图和等高线图,直观表示这四个因素对Y1(GOS产率)的交互作用[27-28]。其中响应面坡度越陡峭,表示该因素对于其他因素的改变越敏感,对GOS产率的影响越大。等高线可以直观地反应两因素交互作用的显著程度,其中椭圆形表示两因素之间作用显著,而接近圆形则表示不显著[27,29]。利用软件做出的响应面与等高线图如图9所示,显示四个变量中任取两个变量为0水平时,其余两个变量同时变化对GOS产率的影响。
由图9可知,当反应温度为50 ℃、反应时间16 h时,从响应面坡度可以看出,A和D的交互作用对GOS产率有显著影响;而当加酶量为8 U/g、反应pH5.5固定不变时,B小于50 ℃,C小于16 h时,等高线较密集,表明在此范围内B和C的交互作用对GOS产率的影响显著;当固定加酶量8 U/g、反应时间16 h时,B小于50 ℃,D小于5.5时,等高线较密集,表明在此范围内B和D的交互作用对GOS产率的影响显著。以上结果与方差分析的结果一致。
2.4.3 DP4产率的回归模型及方差分析
对表2中DP4产率(Y2)相关数据进行多元二次回归拟合及方差分析,分析结果见表4。
表 4 Y2回归模型方差分析结果Table 4. Variance analysis of regression model of Y2来源 平方和 自由度 均方 F值 P值 显著性 模型 9.85 14 0.7038 23.17 <0.0001 ** A 0.7351 1 0.7351 24.20 0.0002 ** B 0.0631 1 0.0631 2.08 0.1716 C 0.0014 1 0.0014 0.0464 0.8326 D 0.1850 1 0.1850 6.09 0.0271 * AB 0.0002 1 0.0002 0.0074 0.9326 AC 0.0036 1 0.0036 0.1185 0.7358 AD 0.2916 1 0.2916 9.60 0.0079 ** BC 0.3660 1 0.3660 12.05 0.0037 ** BD 0.1482 1 0.1482 4.88 0.0444 * CD 0.0784 1 0.0784 2.58 0.1305 A2 4.15 1 4.15 136.71 <0.0001 ** B2 3.43 1 3.43 113.06 <0.0001 ** C2 2.45 1 2.45 80.80 <0.0001 ** D2 2.30 1 2.30 75.63 <0.0001 ** 失拟项 0.3650 10 0.0365 2.42 0.2043 误差 0.0603 4 0.0151 总和 10.28 28 决定系数R2 0.9586 校正决定系数R2Adj 0.9172 根据表4实验结果,得到回归方程(2)为:
Y2=3.30+0.2475A−0.0725B+0.0108C+0.1242D+0.0075AB−0.0300AC+0.2700AD−0.3025BC−0.1925BD−0.1400CD−0.8002A2−0.7277B2−0.6152C2−0.5952D2 式(2)
由表4的方差分析结果可知,模型的P<0.0001,极显著;失拟项P=0.2043>0.05,不显著,说明该模型成立。模型的决定系数R2=0.9586,校正决定系数R2Adj=0.9172,变异系数为8.04%,说明拟合度较好,置信度较高,实验操作可行,可以用此模型来预测低聚半乳糖合成工艺。
该回归模型中的一次项A、D的P值均小于0.05,具有显著性;二次项A2、B2、C2、D2的P值均小于0.01,具极显著性。由F值可知,四个因素对DP4产率的影响大小依次为A(加酶量)>D(反应pH)>B(反应温度)>C(反应时间)。交互项中AD、BC的P值小于0.01,BD的P值小于0.05,说明加酶量和反应pH、反应温度和反应时间及反应温度和反应pH交互作用显著。
2.4.4 DP4产率的响应面分析
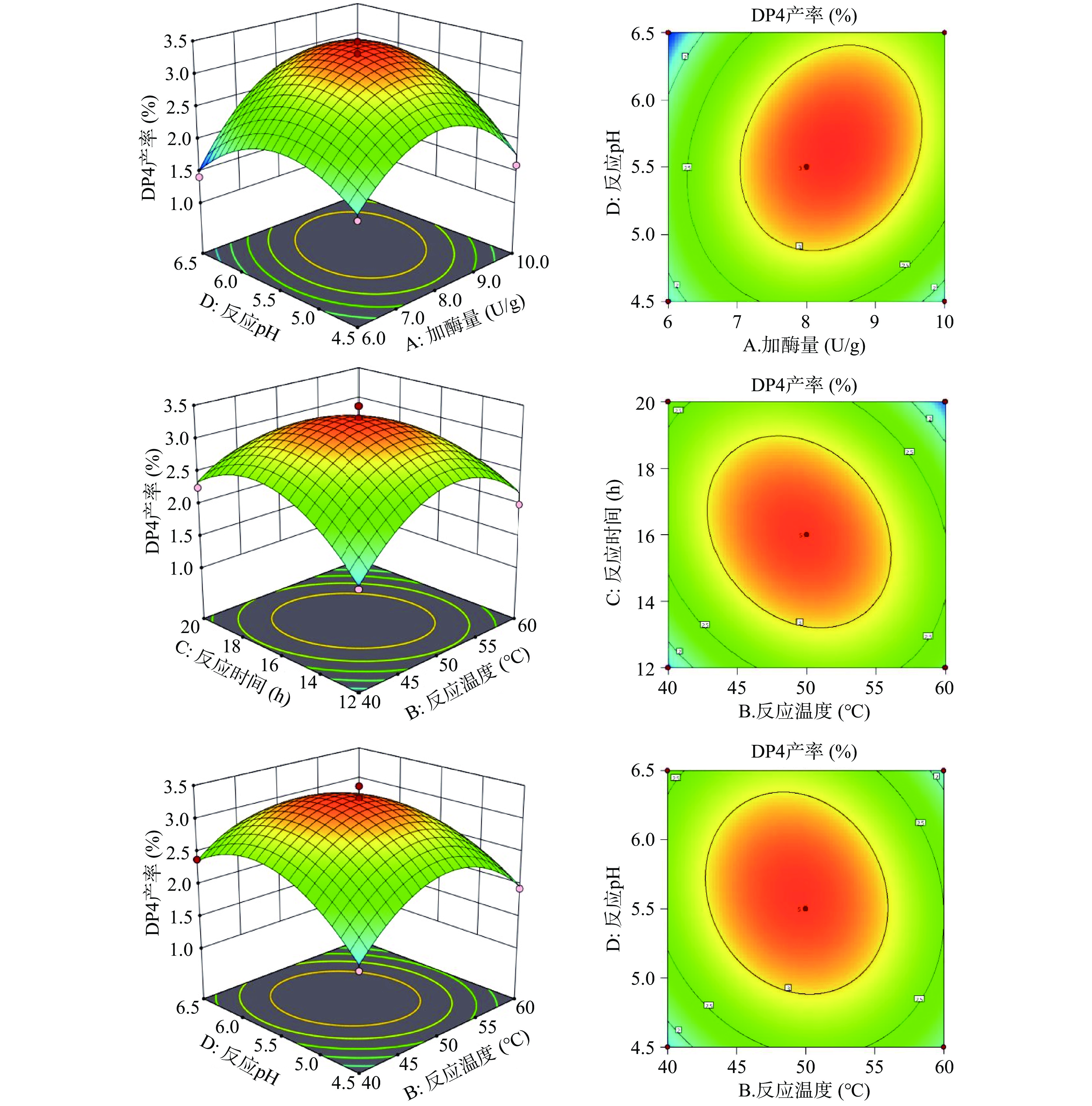
利用Design-Expert 12.0软件对四个因素的交互作用进行分析,选取了AD、BC、BD这三组响应面图和等高线图,直观表示这四个因素对Y2(DP4产率)的交互作用[27-28]。其中响应面坡度越陡峭,表示该因素对于其他因素的改变越敏感,对DP4产率的影响越大。等高线可以直观地反应两因素交互作用的显著程度,其中椭圆形表示两因素之间作用显著,而接近圆形则表示不显著[27,29]。利用软件做出的响应面与等高线图如图10所示,显示四个变量中任取两个变量为0水平时,其余两个变量同时变化对DP4产率的影响。
由图10可知,当反应温度为50 ℃、反应时间16 h时,从响应面坡度可以看出,A和D的交互作用对DP4产率有显著影响;而当加酶量为8 U/g、反应pH5.5固定不变时,B小于50 ℃,C小于16 h时,等高线较密集,表明在此范围内B和C的交互作用对DP4产率的影响显著;当固定加酶量8 U/g、反应时间16 h时,B小于50 ℃,D小于5.5时,等高线较密集,表明在此范围内B和D的交互作用对DP4产率的影响显著。以上结果与方差分析的结果一致。
2.4.5 验证试验
通过响应面试验所获得的GOS产率和DP4产率的二次回归数学模型进行分析,其结果显示,低聚半乳糖合成最佳工艺为:加酶量8.253 U/g、反应温度49.244 ℃、反应时间16.011 h、反应pH5.616。在此工艺下,GOS产率预测值为14.692%,DP4产率预测值为3.334%。为了验证响应面结果的准确性,采用上述低聚半乳糖合成工艺进行实验,为方便实际操作,将条件调整为加酶量8.25 U/g、反应温度49 ℃、反应时间16 h、反应pH5.6,测定GOS产率及DP4产率,实验重复三次,结果表明GOS产率为14.61%±0.19%,DP4产率为3.31%±0.15%,与理论值相差不大,实验结果与模型切合度较好。因此,此响应面所获得的低聚半乳糖合成工艺准确可靠。
3. 结论
本研究在单因素实验的基础上,以GOS产率和DP4产率为响应值,对低聚半乳糖合成工艺进行响应面试验,并建立了响应值和各个因素之间的数学模型。此模型能够较好地预测GOS产率及DP4产率,通过实验与模型验证,很好地证明了模型的可靠性,并得到低聚半乳糖合成最佳工艺:加酶量8.25 U/g、反应温度49 ℃、反应时间16 h、反应pH5.6。在此条件下,GOS产率达到14.61%±0.19%,DP4产率为3.31%±0.15%。结果表明,优化后的工艺参数具有可行性,能够在提高GOS总产率的前提下,有效地选择性提高了DP4产率,这可为高聚合度低聚半乳糖的定向合成及功能性应用提供一定的理论依据,有望为功能性低聚糖类特医食品的研发提供一定的数据参考。
本研究仅在实验室水平考察了选择性提高高聚合度GOS的工艺参数优化,而对β-半乳糖苷酶的高效利用尚缺乏深入研究,导致反应过程中酶及底物的利用率不高。因此,后续将进一步开展β-半乳糖苷酶活性强化研究及酶固定化工艺研究[30-32],提高酶及底物利用率,以期达到更高的生产效率。
-
表 1 响应面试验因素水平设计
Table 1 Factors and levels of response surface methodology
水平 因素 A加酶量(U/g) B反应温度(℃) C反应时间(h) D反应pH −1 6 40 12 4.5 0 8 50 16 5.5 1 10 60 20 6.5 表 2 Box-Behnken试验设计及响应值
Table 2 Design and response value of Box-Behnken experiment
实验号 A B C D Y1(%) Y2(%) 1 0 0 0 0 14.78 3.15 2 0 −1 1 0 11.01 2.26 3 0 1 −1 0 10.17 2.00 4 −1 −1 0 0 9.61 1.64 5 1 0 −1 0 10.58 2.11 6 0 1 0 1 9.77 1.91 7 0 0 −1 1 11.24 2.43 8 0 0 0 0 14.85 3.30 9 0 0 0 0 14.52 3.26 10 1 0 1 0 10.25 2.09 11 −1 1 0 0 8.58 1.56 12 −1 0 −1 0 9.54 1.61 13 0 0 1 1 10.94 2.19 14 0 −1 0 −1 9.89 1.65 15 0 1 0 −1 9.98 1.94 16 1 0 0 1 10.83 2.37 17 0 0 1 −1 10.75 2.31 18 −1 0 0 1 9.41 1.41 19 0 1 1 0 8.34 1.38 20 1 1 0 0 9.92 2.20 21 0 −1 −1 0 9.85 1.67 22 1 −1 0 0 10.3 2.25 23 0 0 0 0 14.49 3.49 24 −1 0 0 −1 10.02 1.72 25 0 0 −1 −1 10.04 1.99 26 1 0 0 −1 9.57 1.60 27 0 −1 0 1 11.07 2.39 28 −1 0 1 0 9.78 1.71 表 3 Y1回归模型方差分析结果
Table 3 Variance analysis of regression model of Y1
来源 平方和 自由度 均方 F值 P值 显著性 模型 98.70 14 7.05 102.40 <0.0001 ** A 1.70 1 1.70 24.62 0.0002 ** B 2.06 1 2.06 29.90 <0.0001 ** C 0.0102 1 0.0102 0.1483 0.7060 D 0.7550 1 0.7550 10.97 0.0051 ** AB 0.1056 1 0.1056 1.53 0.2358 AC 0.0812 1 0.0812 1.18 0.2957 AD 0.8742 1 0.8742 12.70 0.0031 ** BC 2.24 1 2.24 32.46 <0.0001 ** BD 0.4830 1 0.4830 7.02 0.0191 * CD 0.2550 1 0.2550 3.70 0.0748 A2 43.52 1 43.52 632.14 <0.0001 ** B2 43.10 1 43.10 626.05 <0.0001 ** C2 28.00 1 28.00 406.74 <0.0001 ** D2 24.67 1 24.67 358.35 <0.0001 ** 失拟项 0.8648 10 0.0865 3.49 0.1198 误差 0.0991 4 0.0248 总和 99.66 28 决定系数R2 0.9903 校正决定系数R2Adj 0.9807 注:*表示差异显著,P<0.05;**表示差异极显著,P<0.01;表4同。 表 4 Y2回归模型方差分析结果
Table 4 Variance analysis of regression model of Y2
来源 平方和 自由度 均方 F值 P值 显著性 模型 9.85 14 0.7038 23.17 <0.0001 ** A 0.7351 1 0.7351 24.20 0.0002 ** B 0.0631 1 0.0631 2.08 0.1716 C 0.0014 1 0.0014 0.0464 0.8326 D 0.1850 1 0.1850 6.09 0.0271 * AB 0.0002 1 0.0002 0.0074 0.9326 AC 0.0036 1 0.0036 0.1185 0.7358 AD 0.2916 1 0.2916 9.60 0.0079 ** BC 0.3660 1 0.3660 12.05 0.0037 ** BD 0.1482 1 0.1482 4.88 0.0444 * CD 0.0784 1 0.0784 2.58 0.1305 A2 4.15 1 4.15 136.71 <0.0001 ** B2 3.43 1 3.43 113.06 <0.0001 ** C2 2.45 1 2.45 80.80 <0.0001 ** D2 2.30 1 2.30 75.63 <0.0001 ** 失拟项 0.3650 10 0.0365 2.42 0.2043 误差 0.0603 4 0.0151 总和 10.28 28 决定系数R2 0.9586 校正决定系数R2Adj 0.9172 -
[1] 孙纯, 祝文兴, 刘新利. 低聚半乳糖的研究进展[J]. 中国调味品,2017,42(11):170−174. [SUN C, ZHU W X, LIU X L. Research progress on galactooligosaccharides[J]. China Condiment,2017,42(11):170−174. doi: 10.3969/j.issn.1000-9973.2017.11.038 [2] VALDES A M, WALTER J, SEGAL E, et al. Re: Role of the gut microbiota in nutrition and health[J]. BMJ,2018,361(4):17−22.
[3] THONGARAM T, HOEFLINGER J L, CHOW J M, et al. Prebiotic galactooligosaccharide metabolism by probiotic Lactobacilli and Bifidobacteria[J]. J Agric Food Chem,2017,65(20):4184−4192. doi: 10.1021/acs.jafc.7b00851
[4] JING, YAN, AYUMI, et al. Mechanisms of gut microbiota-mediated bone remodeling[J]. Gut Microbes,2017,9(1):84−92.
[5] MAAWIA K, IQBAL S, QAMAR T R, et al. Production of impure prebiotic galacto-oligosaccharides and their effect on calcium, magnesium, iron and zinc absorption in Sprague-Dawley rats[J]. Pharmanutrition,2016,4(4):154−160. doi: 10.1016/j.phanu.2016.10.003
[6] RIGO-ADROVER M, KNIPPING K, GARSSEN J, et al. Prevention of rotavirus diarrhea in suckling rats by a specific fermented milk concentrate with prebiotic mixture[J]. Nutrients,2019,11(1):189. doi: 10.3390/nu11010189
[7] WANG J, TIAN S, YU H, et al. The response of colonic mucosa-associated microbiota composition, mucosal immune homeostasis, and barrier function to early-life galactooligosaccharides intervention in suckling piglets[J]. Journal of Agricultural & Food Chemistry,2018,67(2):578−588.
[8] LOMBÓ F, FERNÁNDEZ J, MORENO F J, et al. A galacto-oligosaccharides preparation derived from lactulose protects against colorectal cancer development in an animal model[J]. Frontiers in Microbiology,2018(9):2004−2018.
[9] ALMEIDA C, CAMARGO M R D, RUSSO E, et al. Role of diet and gut microbiota on colorectal cancer immunomodulation[J]. World Journal of Gastroenterology,2019,25(2):151−162.
[10] CHU H, TAO X, SUN Z, et al. Galactooligosaccharides protects against DSS-induced murine colitis through regulating intestinal flora and inhibiting NF-κB pathway[J]. Life Sciences,2019,242:117220.
[11] 戴竹青. Alpha-低聚半乳糖的酶法合成, 生理活性评价及其构-效关系研究[D]. 南京: 南京农业大学, 2017. DAI Z Q. Enzymatic synthesis of alpha-galactooligosaccharides and evaluation of its physiological function and structure-activity relationship[D]. Nanjing: Nanjing Agricultural University, 2017.
[12] 朱五二, 缪明永, 顾正华, 等. 盐单胞菌S62 β-半乳糖苷酶合成低聚半乳糖的研究[J]. 生物加工过程,2019,17(2):19−25. [ZHU W E, LIAO M R, GU Z H, et al. Synthesis of galactooligosaccharides by β-galactosidase from Halomonas sp. S62[J]. Chinese Journal of Bioprocess Engineering,2019,17(2):19−25. [13] ZONG W R, CHEONG K L, WU D T, et al. Preparation and purification of raffinose family oligosaccharides from Rehmannia glutinosa Libosch. by fast protein liquid chromatography coupled with refractive index detection[J]. Separation & Purification Technology,2014,138:98−103.
[14] COCKBURN D W, KOROPATKIN N M. Polysaccharide degradation by the intestinal microbiota and its influence on human health and disease[J]. Journal of Molecular Biology,2016,428(16):3230−3252. doi: 10.1016/j.jmb.2016.06.021
[15] ABURTO C, GUERRERO C, VERA C, et al. Improvement in the yield and selectivity of lactulose synthesis with Bacillus circulans β-galactosidase[J]. LWT,2020,118:108746. doi: 10.1016/j.lwt.2019.108746
[16] 李泉荟, 刘峰, 栾庆民, 等. 高纯度低聚半乳糖生产技术研究[J]. 中国食品添加剂,2020,31(4):164−168. [LI Q H, LIU F, LUAN Q M, et al. Study on production technology of high purity galactooligosaccharide[J]. Chinese Food Additives,2020,31(4):164−168. doi: 10.19804/j.issn1006-2513.2020.04.021 [17] PÁZMÁNDI M, KOVÁCS Z, BALGA E, et al. Production of high-purity galacto-oligosaccharides by depleting glucose and lactose from galacto-oligosaccharide syrup with yeasts[J]. Yeast,2020,37(9):515−530.
[18] 张金秋, 王少伟, 陶飞, 等. 低聚半乳糖合成研究现状与产业的发展趋势[J]. 食品安全质量检测学报,2019,10(10):2829−2835. [ZHANG J Q, WANG S W, TAO F, et al. Research status and development trend of galacto-oligosaccharide synthesis[J]. Journal of Food Safety & Quality,2019,10(10):2829−2835. doi: 10.3969/j.issn.2095-0381.2019.10.002 [19] 中华人民共和国国家生化检测标准化技术委员会, 国家质量监督检验检疫总局. GB/T 33409-2016, 食品安全国家标准 β-半乳糖苷酶活性检测方法 分光光度法[S]. 北京: 中国标准出版社, 2016. National Biochemical Testing Standardization Technical Committee of the People's Republic of China, General Administration of Quality Supervision, Inspection and Quarantine of the People's Republic of China. GB/T 33409-2016, National food safety standard determination of activity of beta-galactosidase spectrophotometric method[S]. Beijing: China Standards Press, 2016.
[20] COROVIC, MARIJA, BANJANAC, et al. Galacto-oligosaccharide synthesis using chemically modified beta-galactosidase from Aspergillus oryzae immobilised onto macroporous amino resin[J]. International Dairy Journal,2016,54:50−57. doi: 10.1016/j.idairyj.2015.10.002
[21] CG A, CA A, SS A, et al. Improvements in the production of Aspergillus oryzae β-galactosidase crosslinked aggregates and their use in repeated-batch synthesis of lactulose[J]. International Journal of Biological Macromolecules,2020,142:452−462. doi: 10.1016/j.ijbiomac.2019.09.117
[22] TOKOŠOVÁ S, HRONSKÁ. Production of high-content galacto-oligosaccharides mixture using β-galactosidase and Kluyveromyces marxianus entrapped in polyvinylalcohol gel[J]. Chemical Papers-Slovak Academy of Sciences,2016,70(7):1445−1451.
[23] 李美玲, 江波, 张涛. β-半乳糖苷酶催化乳糖合成低聚半乳糖[J]. 食品与生物技术学报,2016,35(3):234−239. [LI M L, JIANG B, ZHANG T. Synthesis of galactooligosaccharides from lactose by β-galactosidase[J]. Journal of Food Science and Biotechnology,2016,35(3):234−239. doi: 10.3969/j.issn.1673-1689.2016.03.002 [24] CV A, CG B, CA B, et al. Conventional and non-conventional applications of β-galactosidases[J]. Biochimica et Biophysica Acta (BBA)-Proteins and Proteomics,2020,1868(1):140271. doi: 10.1016/j.bbapap.2019.140271
[25] FAI A, SIMIQUELI A, GHISELLI G, et al. Sequential optimization approach for prebiotic galactooligosaccharides synthesis by Pseudozyma tsukubaensis and Pichia kluyveri[J]. LWT-Food Science and Technology,2015,63(2):1214−1219. doi: 10.1016/j.lwt.2015.04.064
[26] CINAR K, GUNES G, GULEC H A. Enzymatic synthesis of prebiotic carbohydrates from lactose: Kinetics and optimization of transgalactosylation activity of β-galactosidase from Aspergillus oryzae[J]. Journal of Food Process Engineering,2020,43(8):e13435.
[27] 宫江宁, 陈飞. 响应面法优化龙胆草多糖的脱色工艺[J]. 食品工业科技,2018,39(1):202−207. [GONG J N, CHEN F. Optimization of decolorization of polysaccharide from gentiana by response surface methodology[J]. Science and Technology of Food Industry,2018,39(1):202−207. doi: 10.13386/j.issn1002-0306.2018.01.037 [28] 赵肖通, 解军波, 潘炳成, 等. 响应面分析法优化姬松茸多糖的脱色工艺[J]. 食品工业科技,2016,37(9):207−212. [ZHAO X T, XIE J B, PAN B C, et al. Optimization of decolorization of Agaricus blazei polysaccharide by response surface methodology[J]. Science and Technology of Food Industry,2016,37(9):207−212. doi: 10.13386/j.issn1002-0306.2016.09.032 [29] 陈灿辉, 林彤, 江文韬, 等. 响应面法优化笋头多糖微波-超声波辅助提取工艺[J]. 食品工业科技,2020,41(16):201−206. [CHEN C H, LIN T, JIANG W T, et al. Optimization of microwave-ultrasonic assisted extraction of polysaccharides from basal part of bamboo shoot by response surface methodology[J]. Science and Technology of Food Industry,2020,41(16):201−206. doi: 10.13386/j.issn1002-0306.2020.16.032 [30] CARLA, ABURTO, CECILIA, et al. Co-immobilized β-galactosidase and Saccharomyces cerevisiae cells for the simultaneous synthesis and purification of galacto-oligosaccharides[J]. Enzyme & Microbial Technology,2018,118:102−108.
[31] GONZÁLEZ-DELGADO I, SEGURA Y, MORALES G, et al. Production of high galacto-oligosaccharides by pectinex ultra SP-L: Optimization of reaction conditions and immobilization on glyoxyl-functionalized silica[J]. J Agric Food Chem,2017,65(8):1649−1658. doi: 10.1021/acs.jafc.6b05431
[32] 刘鑫龙, 王立晖, 汤卫华, 等. 固定化半乳糖苷酶催化合成低聚半乳糖的研究[J]. 食品工程,2016(1):20−22. [LIU X L, WANG L H, TANG W H, et al. Study on immobilized galactosidase enzymatic synthesis of galactooligosaccharides[J]. Food Engineering,2016(1):20−22. doi: 10.3969/j.issn.1673-6044.2016.01.007





 下载:
下载:







 下载:
下载:
