Preparation, Characterization and in Vitro Release Performance Evaluation of Konjac Glucomannan Microparticles Loaded with Proanthocyanidins
-
摘要: 本研究以魔芋葡甘聚糖(konjac glucomannan,KGM)为壁材,原花青素(proanthocyanidins, PC)为芯材,利用KGM在乙醇体系下吸水微溶胀的特性制备载PC的KGM微粒,为PC结肠靶向递送提供新的技术思路。实验利用KGM吸附溶于乙醇水溶液中的PC这一方法来制备KGM/PC微粒,采用单因素实验及正交试验优化KGM/PC微粒的制备工艺,通过粒径分析、扫描电镜、红外光谱等对微粒的性质进行表征,并考察了该微粒体外释放性能。结果表明,KGM能成功包封PC,且PC的负载率受KGM及PC添加量的显著影响;正交优化确定KGM负载PC的最佳工艺条件为:在10%(v:v)乙醇溶液中添加16%(w:v)的KGM(粒径为50~90 μm)及11%(w:v)PC时,微粒对PC的负载率为(14.75%±0.27%);同时,经过胃和小肠各消化4 h后,KGM/PC微粒中的PC有79.47%未被释放,可到达结肠部位。综上,该包封微粒在结肠靶向递送方面具有较大的潜力,可为工业生产提供一种简单、有效、安全的包封技术。Abstract: In this study, konjac glucomannan was used as wall material and proanthocyanidins as core material. The micro-swelling properties of KGM in the ethanol system were used to prepare PC-loaded KGM microparticles, which provided a new technical idea for colon-targeted delivery of PC. KGM/PC microparticles were prepared by KGM adsorption of PC dissolved in ethanol aqueous solution. Single factor experiment and orthogonal experiment were used to optimize the preparation process of KGM/PC microparticles, and the properties of the microparticles were characterized by particle size analysis, scanning electron microscopy, infrared spectroscopy, etc. The release performance of the microparticles in vitro was investigated. The results showed that KGM could successfully encapsulate PC and the loading rate of PC was significantly affected by KGM and the amount of PC added. The optimum process conditions of encapsulating PC with KGM determined by orthogonal optimization, that is, when 16% (w:v) KGM (particle size 50~90 μm) and 11% (w:v) PC were added into 10% (v:v) ethanol solution, the loading rate of PC was (14.75%±0.27%). At the same time, after digestion in the stomach and small intestine for 4 h, 79.47% of PC in the KGM/PC microparticles was not released and reached the colon. To sum up, the encapsulated microparticles have great potential in colon-targeted delivery, which can provide a simple, effective, and safe encapsulation technology for industrial production.
-
Keywords:
- konjac glucomannan /
- procyanidins /
- targeted delivery /
- microparticles /
- encapsulation /
- sustained release
-
膳食结构的改变可直接影响结肠疾病的发生与发展[1],通过调节膳食结构预防肠道疾病在目前正受到广泛关注。原花青素(proanthocyanidins, PC)作为一类常见的多酚类物质,其强抗氧化性使它能够清除自由基,预防癌症、心脑血管等疾病[2-3]。同时,研究发现PC在结肠类疾病的预防中也有着巨大潜力[4]:PC可抑制结肠癌细胞的增殖并促进其凋亡[5];动物在食用富含PC的食物后,其结肠中具有抗炎活性的代谢物显著增加,炎症症状明显减轻[6]。然而,由于PC主要在小肠被吸收,且稳定性较差,易被消化液破坏,难以作用于结肠部位[7]。因此,可以利用包封技术提高PC的稳定性,避免PC在上消化道中被分解和吸收,从而实现结肠靶向递送。目前,对PC进行保护的方法包括利用微胶囊、凝胶等对其进行包封,如吴晓琼等[8]利用壳聚糖水凝胶对PC多重乳液进行包裹,纪秀凤等[9]以明胶和阿拉伯胶为壁材,通过复凝聚法制备红树莓籽低聚原花青素微胶囊增加PC稳定性。但这些包封技术存在制备工艺复杂、包封材料性能差、需要其它添加剂的协调作用等不足。因此,需要在这些方面对PC的包封进一步研究改善。
魔芋葡甘聚糖(konjac glucomannan,KGM)作为一种天然高分子多糖,因其生物安全性和特殊的抗消化性,往往被认为是包封材料的良好选择[10-11]。同时,KGM具有预防肿瘤癌变[12]、抗氧化自由基、改善肠道生态[13]等诸多作用,在预防肠道疾病方面也有着良好的应用前景。因此,将KGM作为包封材料应用于PC的靶向递送,不仅可以使PC实现结肠靶向缓释的目的,也可在一定程度上利用KGM改善肠道功能的功效。随着KGM作为包封材料的研究不断深入[11,14],其溶胀度高、粘度大、凝胶可塑性弱、溶胶稳定性差等缺陷,使它往往需要通过物理和化学改性加以改进。如CHEN等[15]将KGM与丙烯酸共聚形成水凝胶,可以使模型药物释放受水凝胶肿胀和降解控制;SHI等[16]以羧甲基KGM和2-羟丙基三甲基氯化铵壳聚糖为载体,静电络合法制备了新型复合纳米球。虽然这些技术取得了一定的效果,但这些改性技术工艺复杂,生产成本较高,且在食品安全方面面临着不少挑战。因此,需要探索一些绿色、安全的KGM包封技术,来降低生产成本,并增加PC的食品安全性。
目前,关于KGM包封PC的研究鲜有报道,寻找简单易操作的KGM包封技术成为亟待解决的工业问题。因此,本文探究了一种新的KGM包封技术,即利用KGM在乙醇体系下吸水微溶胀的特性,在乙醇溶液中用KGM对PC进行吸附包封。实验通过单因素及正交试验优化KGM/PC微粒的制备工艺,利用粒径分析、扫描电镜、红外光谱等对微粒的性质进行表征,从而确定该方法下KGM能成功包封负载PC。同时,通过模拟体外消化评估了KGM/PC微粒的缓释性能,以期为其在结肠控释方面的应用提供技术支持。
1. 材料与方法
1.1 材料与仪器
纯化魔芋精粉(纯度≥86%) 湖北十堰花仙子魔芋制品有限公司;原花青素(纯度≥95%) 原叶生物科技有限公司;胃蛋白酶(≥250 U/mg)、胰酶(4×USP) 美国Sigma-Aldrich公司;β-甘露聚糖酶(40000 U/g) 北京索来宝科技有限公司;其他化学试剂 均为国产分析纯。
AXTG16G型医用离心机 盐城市安信实验仪器有限公司; LGJ-10型真空冷冻干燥机 北京松源华兴科技发展有限公司;TU-1950双光束紫外可见分光光谱仪 北京普析通用仪器有限责任公司;S-3000N型扫描电镜 HITACHI公司;Mastersizer 3000型激光粒度分析仪 英国马尔文公司;Spectrum100红外光谱仪 美国PerkinElmer 公司; SHZ-88型水浴恒温振荡器 常州朗越仪器制造有限公司。
1.2 实验方法
1.2.1 KGM/PC微粒的制备工艺优化
1.2.1.1 载PC的KGM微粒的制备
称取一定量的PC,于室温下加入到25 mL一定浓度的乙醇水溶液中,待PC完全溶解,加入一定量的KGM,磁力搅拌15 min后,经离心(1500 r/min)10 min,弃去上清液,用同浓度乙醇溶液清洗3遍,再次离心,取沉淀物冷冻后真空冷冻干燥12 h后,获得KGM/PC微粒。
1.2.1.2 单因素实验
按1.2.1.1中的方法制备KGM/PC微粒,选取KGM添加量(14%、16%、18%、20%、22%、24%、26%)、KGM粒径(粒径分为5个等级,由1~5分别对应的粒径范围为210~250、170~210、130~170、90~130和50~90 μm)、乙醇浓度(10%、12%、14%、16%、18%、20%)及PC添加量(5%、6%、7%、8%、9%、10%、11%)4个因素进行单因素实验,选择20%的KGM添加量、50~90 μm的KGM颗粒、14%乙醇浓度和7%的PC添加量为各单因素的控制变量。探究各因素对KGM/PC微粒负载率的影响,每个因素平行实验3次,取平均值。
1.2.1.3 正交试验
在单因素实验的基础上,选取乙醇浓度、KGM添加量和PC添加量为考察因素,以KGM/PC微粒的负载率为评价指标,采用L9(34)正交表进行试验设计,确定KGM/PC微粒的最佳制备条件。因素水平如表1所示。
表 1 正交试验因素与水平Table 1. Factors and levels of orthogonal test水平 因素 A 乙醇浓度(%) B PC添加量(%) C KGM添加量
(%)1 10 9 16 2 12 10 18 3 14 11 20 1.2.1.4 KGM/PC微粒的负载率的测定
取20 mg制备好的KGM/PC微粒加入20 mL的β-甘露聚糖酶液(5 mg/mL)中,37 °C水浴保温并磁力搅拌1 h,待KGM/PC微粒完全酶解,混匀后取2 mL于离心机经离心(1500 r/min)10 min后,用硫酸-香草醛比色法[17]测量上清液中原花青素含量,并用公式(1)计算PC的负载率:
负载率(%)=mM×100 (1) 式中:m为KGM/PC微粒中PC的含量,mg;M为KGM/PC微粒的总质量,mg。
1.2.2 KGM/PC微粒的表征
1.2.2.1 颗粒粒径测定
参考毕会敏等[18]的方法并作适当修改,采用英国马尔文公司的Mastersizer 3000型激光粒度分析仪测定载药微粒的粒径分布,以无水乙醇为分散系,折射率为1.52,折光度范围:8%~20%。
1.2.2.2 颗粒表观形态及结构特征
将KGM负载PC前后的颗粒样品置于培养皿中,用相机拍摄颗粒的表观形态;用研钵充分研磨KGM负载PC前后的颗粒样品从而破坏颗粒表面结构,将研磨前后的样品颗粒固定在双面导电胶上,在真空下对样品进行离子溅射喷金处理,用电子扫描显微镜(SEM)在500×, 5000×下对颗粒的表面形态进行观察,并选择合适的区域拍照。
1.2.2.3 傅立叶红外光谱分析
参考YAN等[19]的方法,将KGM、PC、KGM-PC混合物和KGM/PC微粒分别使用傅立叶变换红外光谱仪在4000~600 cm−1范围内检测,累积扫描次数为32。
1.2.3 KGM/PC微粒体外释放性能的测定
1.2.3.1 人工模拟消化液的配制
参照ANA-ISABEL等[20]的方法并作适当修改,制备胃模拟消化液(简称胃液,pH2.0)和小肠/结肠模拟消化液(简称肠液,pH7.4)。模拟消化前,在胃液中加入胃蛋白酶,配制成胃蛋白酶液(10 mg/mL)备用;在肠液中分别加入胰酶和β-甘露聚糖酶配制成胰酶液(10 mg/mL)和β-甘露聚糖酶液(10 mg/mL)备用。
1.2.3.2 体外消化及PC释放率的测定
参考文献[20-22]的方法并作适当修改,将0.1 g KGM/PC微粒用1 mL去离子水溶解形成凝胶后,置于 90 mL人工模拟液胃液中,添加胃蛋白酶液10 mL并密封,然后于恒温振荡器中消化4 h(37 ℃,175 r/min)。胃消化结束后,用1 mol/mL的NaHCO3调节体系pH7.4,并添加80 mL模拟肠液和20 mL胰酶液,密封后于恒温振荡器(37 ℃,175 r/min)继续消化4 h。待胃部和小肠模拟消化后,向小肠消化体系中加入20 mL β-葡甘聚糖酶液,于恒温振荡器(37 ℃,175 r/min)中再消化8 h以模拟微粒在结肠环境中的释放情况。整个体外消化过程中,制备间隔1 h的不同时间段的反应体系,待反应时间结束,从消化体系中取1 mL混合液于2 mL PE离心管中,并将剩余反应体系沸水浴5 min以钝化酶的活性。取出的样液则经离心(1500 r/min)10 min后,取上清液测定PC的释放率,PC释放率用公式(2)计算。同时,按照KGM/PC中PC的含量,将未包封的PC与KGM均匀混合后,按照以上步骤进行消化,作为对照实验。
释放率(%)=CtC×100 (2) 式中:Ct为t时间内释放液中PC的含量,mg;C为体外释放前KGM/PC微粒中PC的含量,mg。
1.3 数据分析与处理
所有实验数据统计分析均用SPSS 25.0进行方差分析,Origin 8.5作图,所得结果均以3个独立样本的平均值±标准偏差表示,Duncan式检验法(P<0.05)判定其显著性差异。
2. 结果与分析
2.1 KGM/PC微粒的制备优化
2.1.1 单因素实验结果
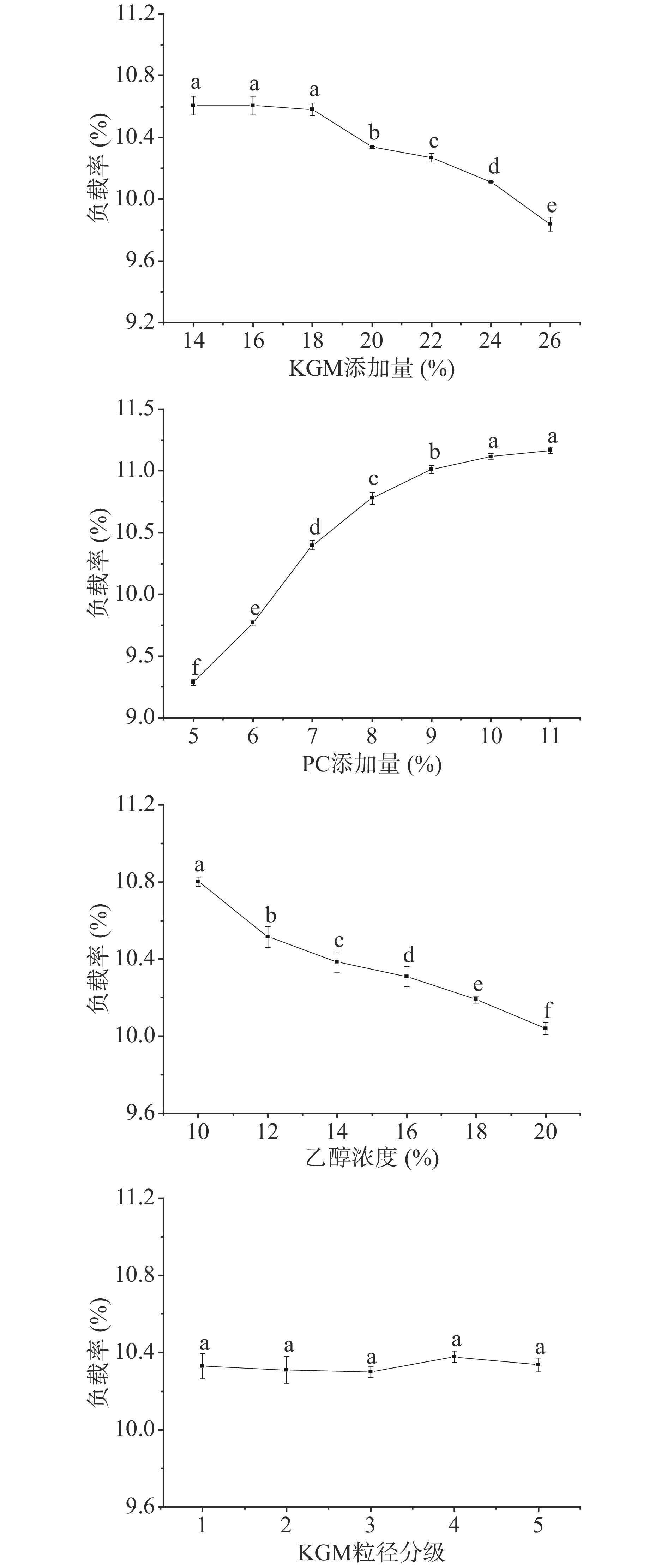
乙醇浓度、PC添加量、KGM添加量和KGM粒径对KGM/PC微粒负载率的影响结果如图1所示。由图1可知,KGM/PC微粒的负载率随KGM添加量的增加,呈现先稳定后降低的趋势。由于KGM在固定乙醇浓度和PC添加量的体系下吸水率不变,单位KGM可装载的PC量不变,微粒负载率无显著变化。当KGM添加量到达18%以后,体系内PC的量不变,KGM分子之间相互竞争,导致微粒负载率下降。因此,确定正交试验中KGM添加量的水平分别为16%、18%和20%。随着PC添加量的增加,KGM/PC微粒负载率先增加后稳定。可能是KGM颗粒内部可装载PC的空间有限,当PC添加量增加到10%后,KGM负载PC的量趋于饱和;且实验得出该体系下PC的最大添加量为11%。故确定正交试验中PC添加量的水平分别为9%、10%和11%。KGM/PC微粒的负载率随乙醇浓度的增加而下降。由于PC随KGM吸收水分时进入KGM颗粒内部,乙醇作为溶胀抑制剂降低了KGM的吸水率[23],随着乙醇浓度的增加,KGM的吸水率下降,导致KGM/PC微粒的负载率随之减小;且实验发现当乙醇浓度小于10%,冻干后无法获得颗粒态微粒。综上,确定正交试验中乙醇浓度的水平分别为10%、12%和14%。粒径变化对KGM/PC微粒的负载率无显著性影响。随着KGM颗粒粒径的降低,KGM的吸水性会显著增加[24],理论上来讲,微粒负载率应随着KGM粒径的降低而增大。实践中由于乙醇对KGM吸水性有较强的抑制作用,该作用程度大于粒径对KGM吸水性的影响程度,限制KGM吸水溶胀,而不表现出负载率的显著变化。因此,正交试验时不考虑此因素。
2.1.2 正交试验结果
在单因素实验结果的基础上进行正交试验,确定KGM/PC微粒的最佳制备条件。得到正交试验结果见表2,方差分析结果见表3。由表3可知,因素A、B对KGM/PC微粒负载率的影响显著(P<0.05),因素C为不显著因素,由F值大小确定各因素对微粒负载率的影响大小顺序:A>B>C。结合表2得到KGM/PC微粒的最佳制备条件为A1B3C1。该制备条件在正交试验中未出现,不能确定此组合是否为最佳工艺,因此需要进行验证实验,在A1B3C1条件下进行平行实验,得到平均负载率为(14.75%±0.27%),高于其他组的负载率,说明乙醇浓度10%、PC添加量11%、KGM添加量16%为相对最佳工艺。同时,对比相似研究发现,该方法下制备得KGM/PC微粒的负载率高于SUSANTI等[23]采用泡沫垫干燥法对富含PC的红高粱提取物进行包封(PC含量为9.11~9.23 mg/g);与葛莹莹等[25]制备的石墨烯/KGM多孔干凝胶的负载率相近,该凝胶对5-氟尿嘧啶的负载率达到154 mg/g。说明该制备方法不仅简单有效,还可以获得较高负载量的微粒。
表 2 KGM/PC微粒负载率正交试验设计与结果Table 2. The orthogonal experimental design and results for loading rate of KGM/PC particles试验号 A
乙醇浓度B
PC添加量C
KGM添加量负载率
(%)1 1 1 1 12.30 2 1 2 2 13.06 3 1 3 3 12.76 4 2 1 2 11.42 5 2 2 3 12.15 6 2 3 1 12.62 7 3 1 3 10.72 8 3 2 1 11.77 9 3 3 2 12.06 K1 38.12 34.44 36.69 K2 36.19 36.98 36.54 K3 34.55 37.44 35.63 k1 12.71 11.48 12.23 k2 12.06 12.33 12.18 k3 11.52 12.48 11.88 极差/R 1.19 1.00 0.35 表 3 KGM/PC微粒负载率正交试验方差分析Table 3. The variance analysis of orthogonal test for loading rate of KGM/PC particles方差来源 III 类平方和 自由度 均方 F 显著性(P) 修正模型 4.089a 6 0.681 23.222 0.042* 截距 1316.722 1 1316.722 44871.259 0.000 A 2.129 2 1.064 36.273 0.027* B 1.740 2 0.870 29.654 0.033* C 0.219 2 0.110 3.738 0.211 误差 0.059 2 0.029 总计 1320.869 9 修正后总计 4.147 8 注:*表示显著(P<0.05);a:R2=0.986(调整后R2=0.943)。 2.2 KGM/PC微粒的表征
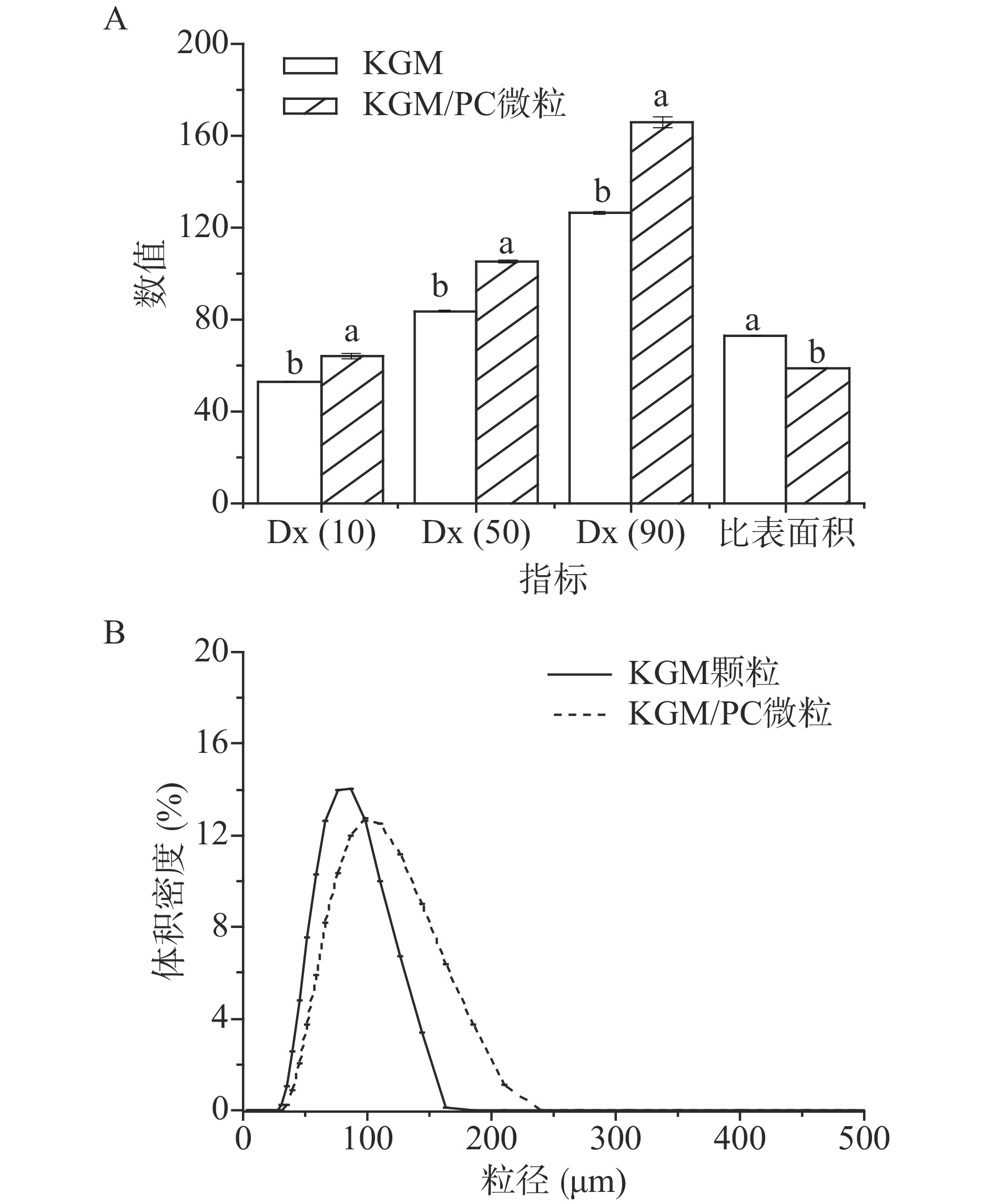
2.2.1 KGM颗粒负载PC前后的粒径变化
KGM颗粒负载PC前后粒径的变化情况如图2所示,KGM和KGM/PC 微粒的粒径图均为单峰分布曲线,两者粒径主要分布在40~170 μm之间。与未负载PC的KGM颗粒对比,KGM/PC微粒的Dx(10)、Dx(50)和Dx(90)值均明显增加,比表面积由78.4 m2/Kg减小为59.03 m2/Kg。说明KGM颗粒负载PC后体积增大,这可能是由KGM吸水溶胀过程中PC随水分进入KGM,冻干后水分升华,PC保留在KGM颗粒内部所导致的。
2.2.2 KGM颗粒负载PC前后的颗粒表观形态及结构特征
KGM颗粒负载PC前后的颗粒表观形态如图3所示。由图3可知,KGM颗粒表观呈白色颗粒状,PC为红褐色粉末,KGM/PC微粒呈浅红褐色颗粒状,而按相同比例混合制备的KGM-PC混合物为白色和红褐色相间的颗粒状,说明乙醇体系下KGM能够负载PC,从而形成均匀的KGM/PC微粒。
KGM颗粒负载PC前后的结构特征如图4所示。KGM颗粒负载PC前后表观状态无明显变化,均呈表面平整的不规则颗粒状。进一步研磨破碎颗粒表面,发现KGM颗粒微观结构呈现较完整的排列有序的片层纤维结构,这与唐兰兰等[26]的研究结果一致。但KGM/PC微粒颗粒内部具有大量网状多孔洞结构,可能是由于KGM颗粒在低浓度乙醇溶液中吸水微溶胀,冷冻干燥过程中内部水分升华形成的。同时,这些孔洞结构可以为KGM包封PC提供空间基础,也说明了KGM颗粒负载PC后体积增大的原因。
2.2.3 傅立叶红外光谱分析
图5为KGM、PC、KGM/PC微粒和KGM-PC混合物的红外图谱,KGM-PC混合物的红外谱图显示了来自KGM的各特征吸收峰,同时在1605.76、1519.91、1437.04 cm−1处检测到三个连续的吸收峰,这是来自PC苯环骨架中的C=C特征伸缩振动峰[27],在1279.97、1208.42 cm−1处检测到PC的酚羟基伸缩振动及面内弯曲振动峰,表明该混合物中KGM与PC二者只存在单一混合。KGM/PC微粒红外图谱中的特征吸收峰主要是KGM的各吸收峰,但在1520.93 cm−1左右出现了一个PC苯环骨架C=C的特征伸缩振动峰,说明该微粒中含有PC;而PC的其他特征吸收峰未出现,说明微粒并不是壁材与芯材的简单物理混合物[28]。并且在形成的微粒中未发现新的特征吸收峰,说明在制备过程中未形成新的化学键,KGM与PC之间并未发生化学反应[29]。上述结果表明,KGM成功将PC进行了包封,且在该反应过程中未改变KGM和PC的化学性质。结合粒径与扫描电镜的结果,推测PC随KGM的吸水过程进入KGM颗粒内部,冻干后附着在KGM颗粒内的孔洞结构中,从而达到KGM负载PC的效果。
2.3 KGM/PC微粒的体外缓释性能
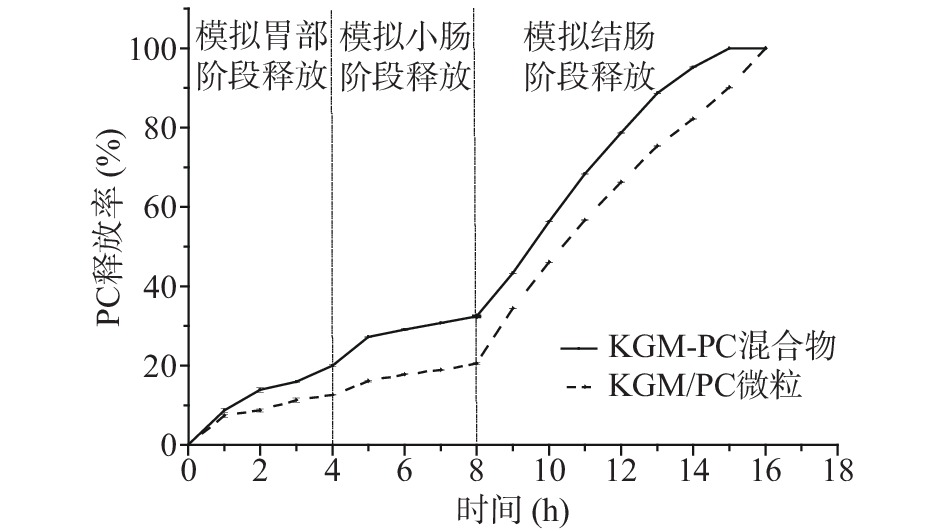
KGM/PC微粒体外缓释测定实验的结果如图6所示。经胃部和小肠模拟消化后,KGM-PC混合凝胶和KGM/PC微粒凝胶中PC的释放率分别为32.46%和 20.53%,微粒凝胶较混合凝胶降低了36.75%的释放率。PC释放差异性的原因可能与KGM-PC混合粉和KGM/PC微粒形成的凝胶结构有关,当KGM/PC微粒吸水形成凝胶时,由于PC被包封于KGM内部,不影响KGM与水分子和KGM分子以氢键结合形成凝胶[30],而在 KGM-PC混合体系中PC在一定程度上会阻碍KGM分子间的缔合,从而影响凝胶结构的形成。所以微粒凝胶结合更牢固,在胃部和小肠阶段的PC释放率更低。
在模拟结肠消化阶段,KGM/PC微粒凝胶和KGM-PC混合凝胶分别于8和7 h后达到完全释放,对比凝胶在模拟胃部和小肠阶段的释放情况,发现模拟结肠环境中PC的释放速度更快,这主要是因为结肠环境中的β-甘露聚糖酶具有降解KGM的特性[31],从而促进了PC的释放。同时,凝胶表面附近的PC主要通过KGM吸水溶胀过程中形成的水孔或通道扩散,KGM的酶降解在一定程度上导致了新孔的出现,网络部分受损,孔径增大,使得PC的释放速率进一步增加[32]。综上所述,KGM/PC微粒凝胶经过胃部和小肠消化后,还有80%左右的PC可到达结肠部位释放,因此判断微粒可以起到结肠靶向的作用。
3. 结论
本实验通过正交试验确定KGM/PC微粒的最优制备工艺为:乙醇浓度10%、PC添加量为11%、KGM添加量为16%,在该条件下可得到负载率为(14.75%±0.27%)的KGM/PC微粒,并以粒径、表观结构及红外光谱分析证实了在乙醇体系下利用KGM吸水微溶胀特性制备优良KGM/PC微粒的可行性。同时,利用体外模拟消化实验确定该KGM/PC微粒具有较好的体外缓释性能,可为PC的结肠靶向递送提供借鉴意义。本实验制备的KGM/PC微粒的工艺相比于文中提到的其它方法(复凝聚法、泡沫垫干燥法等)更简单,且无需对KGM进行改性处理,从而确保了KGM/PC微粒的食品安全性,可为工业生产提供一种简单有效、安全风险更低、生产成本更小的包封技术。
-
表 1 正交试验因素与水平
Table 1 Factors and levels of orthogonal test
水平 因素 A 乙醇浓度(%) B PC添加量(%) C KGM添加量
(%)1 10 9 16 2 12 10 18 3 14 11 20 表 2 KGM/PC微粒负载率正交试验设计与结果
Table 2 The orthogonal experimental design and results for loading rate of KGM/PC particles
试验号 A
乙醇浓度B
PC添加量C
KGM添加量负载率
(%)1 1 1 1 12.30 2 1 2 2 13.06 3 1 3 3 12.76 4 2 1 2 11.42 5 2 2 3 12.15 6 2 3 1 12.62 7 3 1 3 10.72 8 3 2 1 11.77 9 3 3 2 12.06 K1 38.12 34.44 36.69 K2 36.19 36.98 36.54 K3 34.55 37.44 35.63 k1 12.71 11.48 12.23 k2 12.06 12.33 12.18 k3 11.52 12.48 11.88 极差/R 1.19 1.00 0.35 表 3 KGM/PC微粒负载率正交试验方差分析
Table 3 The variance analysis of orthogonal test for loading rate of KGM/PC particles
方差来源 III 类平方和 自由度 均方 F 显著性(P) 修正模型 4.089a 6 0.681 23.222 0.042* 截距 1316.722 1 1316.722 44871.259 0.000 A 2.129 2 1.064 36.273 0.027* B 1.740 2 0.870 29.654 0.033* C 0.219 2 0.110 3.738 0.211 误差 0.059 2 0.029 总计 1320.869 9 修正后总计 4.147 8 注:*表示显著(P<0.05);a:R2=0.986(调整后R2=0.943)。 -
[1] LIU L, NISHIHARA R, QIAN Z R, et al. Association between inflammatory diet pattern and risk of colorectal carcinoma subtypes classified by immune responses to tumor[J]. Gastroenterology,2017,153(6):1517−1530. doi: 10.1053/j.gastro.2017.08.045
[2] NÚÑEZIGLESIAS M J, NOVIO S, GARCÍA C, et al. Co-adjuvant therapy efficacy of catechin and procyanidin b2 with docetaxel on hormone-related cancers in vitro[J]. International Journal of Molecular Sciences,2021,22(13):7178−7178. doi: 10.3390/ijms22137178
[3] RAUF A, IMRAN M, ABU-IZNEID T, et al. Proanthocyanidins: A comprehensive review[J]. Biomedicine & Pharmacotherapy,2019,116(5):108999.
[4] GRACE N J, EVANGELINE C S, SWAMINATHAN A, et al. Cytotoxicity and apoptotic cell death induced by vitis vinifera peel and seed extracts in a431 skin cancer cells[J]. Cytotechnology,2018,70(2):537−54. doi: 10.1007/s10616-017-0125-0
[5] VAID M, SINGH T, PRASAD R, et al. Bioactive proanthocyanidins inhibit growth and induce apoptosis in hum an melanoma cells by decreasing the accum ulation of beta-catenin[J]. Int J Oncol,2016,48(2):624−34. doi: 10.3892/ijo.2015.3286
[6] WU Y, MA N, SONG P X, et al. Grape seed proanthocyanidin affects lipid metabolism via changing gut microflora and enhancing propionate production in weaned pigs[J]. The Journal of Nutrition,2019,149(9):1523−1532. doi: 10.1093/jn/nxz102
[7] 付欣, 周浩, 钟清, 等. 原花青素-介孔二氧化硅纳米颗粒复合体制备及释放研究[J]. 食品科学技术学报,2020,38(1):67−73. [FU X, ZHOU H, ZHONG Q, et al. Study on preparation and release of proanthocyanidins-mesoporous silica nanoparticles complexes[J]. Journal of Food Science and Technology,2020,38(1):67−73. doi: 10.3969/j.issn.2095-6002.2020.01.009 [8] 吴晓琼, 贾定坤, 傅志贤, 等. 原花青素多重乳液水凝胶的制备及评价[J]. 粮食与油脂,2020,33(12):125−128. [WU X Q, JIA D K, BO Z X, et al. Preparation and evaluation of multiple emulsion hydrogel of procyanidin[J]. Grains and Fats,2020,33(12):125−128. doi: 10.3969/j.issn.1008-9578.2020.12.033 [9] 纪秀凤, 吕长鑫, 芦宇, 等. 红树莓籽低聚原花青素微胶囊制备工艺优化及其稳定性分析[J]. 食品工业科技,2019,40(3):165−172. [JI X F, LU C X, LU Y, et al. Optimization of preparation technology of microencapsulation of oligomeric proanthocyanidins from red raspberry seeds and its stability analysis[J]. Food Industry Science and Technology,2019,40(3):165−172. [10] ZHANG C, CHENJ D, YANG F Q. Konjac glucomannan, a promising polysaccharide for OCDDS[J]. Elsevier,2014,104:175−181.
[11] WANG L, LIN L ZZ, CHEN X H, et al. Synthesis and characteristics of konjac glucomannan films incorporated with functionalized microcrystalline cellulose[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects,2018,563:237−245.
[12] LI J Y, SUN F, ZHOU H F, et al. A systematic review exploring the anticancer activity and mechanisms of glucomannan[J]. Frontiers in Pharmacology,2019,10:930. doi: 10.3389/fphar.2019.00930
[13] BAKHT R S, LI B, WANG L, et al. Health benefits of konjac glucomannan with special focus on diabetes[J]. Bioactive Carbohydrates and Dietary Fibre,2015,5(2):179−187. doi: 10.1016/j.bcdf.2015.03.007
[14] YUAN Y, WANG L, MU R J, et al. Effects of konjac glucomannan on the structure, properties, and drug release characteristics of agarose hydrogels[J]. Carbohyd Polym,2018,190:196−203. doi: 10.1016/j.carbpol.2018.02.049
[15] CHEN L G, LIU Z L, ZHUO R X. Synthesis and properties of degradable hydrogels of konjac glucomannan grafted acrylic acid for colon-specific drug delivery[J]. Polymer,2005,46(16):6274−6281. doi: 10.1016/j.polymer.2005.05.041
[16] SHI C J, ZHU P, CHEN N, et al. Preparation and sustainable release of modified konjac glucomannan/chitosan nanospheres[J]. International Journal of Biological Macromolecules,2016,91:609−614. doi: 10.1016/j.ijbiomac.2016.05.073
[17] 石磊, 高哲, 刘丽南, 等. 四种原花青素含量测定方法比较[J]. 食品工业科技,2019,40(15):242−247,253. [SHI L, GAO Z, LIU L N, et al. Comparison of four methods for quantitation of proanthocyanidin[J]. Food Industry Science and Technology,2019,40(15):242−247,253. [18] 毕会敏, 范方宇, 杨宗玲, 等. 纳米SiO2/大豆分离蛋白为壁材的核桃油微胶囊特性[J]. 食品与发酵工业,2020,46(21):147−153. [BI H M, FAN F Y, YANG Z L, et al. Characteristics of walnut oil microcapsules with nano-SiO2/soy protein isolate as wall material[J]. Food and Fermentation Industries,2020,46(21):147−153. [19] YAN L, ZENG F Y, CHEN Z J, et al. Improvement of wood decay resistance by salicylic acid/silica microcapsule: Effects on the salicylic leaching, microscopic structure and decay resistance[J]. International Biodeterioration & Biodegradation,2021,156:105−134.
[20] ANA-ISABEL M C, EGGER L, PORTMANN R, et al. A standardised semi-dynamic in vitro digestion method suitable for food-an international consensus[J]. Food & Function,2020,11(2):1702−1720.
[21] 方坤, 李坚斌, 魏群舒, 等. 改性葡甘露聚糖/海藻酸钠微囊体外释药研究[J]. 食品与发酵工业,2018,44(12):86−91. [FANG K, LI J B, WEI Q S, et al. Drug-release of carboxymethyl konjac glucomannan-alginate microcapsule in vitro[J]. Food and Fermentation Industries,2018,44(12):86−91. [22] 李培培. pH-时滞双敏感KGM-SA结肠靶向凝胶微丸的研究[D]. 成都: 成都中医药大学, 2016: 30−35. LI P P. The investigation of pH and time-lag double sensitive KGM–SA colon-targeted gel microspheres[D]. Chengdu: Chengdu University of Traditional Chinese Medicine, 2016: 30−35.
[23] SUSANTI D Y, SEDIAWAN W B, FAHRURROZI M, et al. Encapsulation of red sorghum extract rich in proanthocyanidins: Process formulation and mechanistic model of foam-mat drying at various temperature[J]. Chemical Engineering and Processing Process Intensification,2021(4):108375.
[24] 李耀玲, 林立, 王富聚, 等. 魔芋葡甘聚糖物理改性研究进展[J]. 包装与食品机械,2013,31(5):48−52. [LI Y L, LIN L, WANG F J, et al. Research progress in the physical modification of konjac glucomannan[J]. Packaging and Food Machinery,2013,31(5):48−52. doi: 10.3969/j.issn.1005-1295.2013.05.013 [25] 葛莹莹, 彭琪, 于永生. 石墨烯/魔芋葡甘聚糖多孔干凝胶的制备及对5-氟尿嘧啶的吸附和释药研究[J]. 西北药学杂志,2020,35(3):413−417. [GE Y Y, PENG Q, YU Y S, et al. Preparation of graphene/konjac glucomannan porous xerogel and study on its adsorption and drug release properties for 5-fluorouracil[J]. Northwest Pharmaceutical Journal,2020,35(3):413−417. doi: 10.3969/j.issn.1004-2407.2020.03.022 [26] 唐兰兰, 张世奇, 卫子颜, 等. 红外烘烤对魔芋葡甘露聚糖表观黏度以及微观结构的影响[J/OL]. 食品科学: 1−11 [2021-03-25]. http://kns.cnki.net/kcms/detail/11.2206.TS.20201229.0957.046.html. TANG L L, ZHANG S Q, WEI Z Y, et al. Study on the effect of apparent viscosity and micro-structure of konjac glucomannan under infrared baking heat treatment[J/OL]. Food Science: 1−11 [2021-03-25].
[27] VOLNEI B S, MARCELO T, MARIANA A. et al. Functional properties and encapsulation of a proanthocyanidin rich cinnamon extract (Cinnamomum zeylanicum) by complex coacervation using gelatin and different polysaccharides[J]. Food Hydrocolloids,2018,77:297−306. doi: 10.1016/j.foodhyd.2017.09.040
[28] 石泽栋, 蒋雅萍, 孙英杰, 等. 牛至精油微胶囊的制备、表征及在杏贮藏期的抑菌效果[J]. 食品科学,2021,42(11):186−194. [SHI Z D, JIANG Y P, SUN Y J, et al. Preparation and characterization of oregano essential oil microcapsules and its sterilization effects on apricot fruit during storage[J]. Food Science,2021,42(11):186−194. doi: 10.7506/spkx1002-6630-20200712-155 [29] 宁亚维, 王瑶, 侯琳琳, 等. Brevilaterin微胶囊化技术及缓释特性分析[J]. 食品科学,2021,42(4):38−43. [NING Y W, WANG Y, HOU L L, et al. Optimization of brevilaterin microencapsulation and analysis of slow release characteristics[J]. Food Science,2021,42(4):38−43. doi: 10.7506/spkx1002-6630-20191120-237 [30] 吴妹. 魔芋葡甘聚糖凝胶稳定性及其动力学分析[D]. 福州: 福建农林大学, 2015. WU M. Study on gel stability and dynamics of konjac glucomannan[D]. Fuzhou: Fujian Agriculture and Forestry University, 2015.
[31] FITTREE H, SANTAD W, PISSARED K. Amelioration of gut dysbiosis and gastrointestinal motility by konjac oligo-glucomannan on loperamide-induced constipation in mice[J]. Nutrition,2020,73:110715. doi: 10.1016/j.nut.2019.110715
[32] XU Q, HUANG W J, JIANG L B, et al. KGM and PMAA based pH-sensitive interpenetrating polymer network hydrogel for controlled drug release[J]. Carbohydrate Polymers,2013,97(2):565−570. doi: 10.1016/j.carbpol.2013.05.007





 下载:
下载:
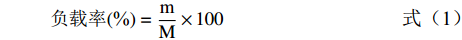
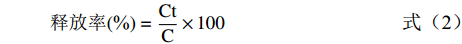



 下载:
下载:
