Kinetic Effects of KCl Substitution for NaCl in Different Proportions on Lipid Oxidation in Pork
-
摘要: 为探究KCl部分替代NaCl对猪肉加工中脂肪氧化的影响,以绞碎的猪背最长肌为原料,加入3%或4%的盐,并分别以15%、30%、45%和60%的KCl替代NaCl,经不同温度处理后,研究脂肪氧化的动力学变化。结果表明,当盐的组成和含量不变时,脂肪初级及次级氧化速率常数均随温度的增加而增加。当温度不变时,脂肪初级氧化速率常数在3%盐浓度时,随KCl替代比的增加而减小;而在4%盐含量时,其随替代比的增加先增加后减少,在45%替代比时达最大值。Arrhenius方程分析表明:总盐浓度为3%时,随KCl替代比的增加,脂肪初级和次级氧化的活化能都呈线性显著增加(P<0.05);而当盐的总浓度为4%时,KCl替代对初级和次级脂肪氧化的活化能均无显著影响(P>0.05)。因此,总盐浓度为3%时,KCl部分替代NaCl可随替代比线性增加猪肉中脂肪的氧化稳定性;而当盐浓度为4%时,KCl的替代对脂肪氧化稳定性影响很小。Abstract: To investigate the effects of KCl substitution for NaCl in different proportions on lipid oxidation in pork processing, 3% or 4% of NaCl, which was partly replaced by 15%, 30%, 45%, or 60% of KCl, respectively, were added to the minced longissimus muscles, then kinetic law of lipid oxidation was studied after treatment at different temperature. The results showed that at a fixed salt content and composition, both the primary and the secondary lipid oxidation rate constants increased with the increasing temperature. At a fixed temperature, lipid primary oxidation rate constants decreased with the increasing of KCl substitution proportion at a 3% salt content, while which first increased and then decreased with the KCl substitution proportion when salt concentration was fixed at 4%, reaching a maximum at 45% of KCl proportion. The Arrhenius equation analysis showed that at 3% salt concentration, the activation energies of both lipid primary oxidation and lipid secondary oxidation increased linearly with the increasing of KCl substitution proportion (P<0.05), while when salt content was at 4%, partial replacement of NaCl with KCl had no significant effect on the activation energies of lipid oxidation (P>0.05). Therefore, partial replacement of NaCl with KCl could improve the lipid oxidation stability in pork linearly with the substitution proportion if total salt concentration is at about 3%, and no significant effect was observed if total salt content was at about 4%.
-
Keywords:
- pork /
- KCl /
- NaCl /
- lipid oxidation
-
氯化钠(NaCl)是肉制品加工中最重要的辅料之一,适量的NaCl能改善肉制品的多汁性,延长保质期,进而影响肉制品的风味、色泽、质构等品质[1-2]。随着加工食品的日益增多,人们过量摄入NaCl,使体内钠钾比增加[3]。研究显示,过量摄入钠盐可造成血压升高,增加心血管疾病的发病率,还与一些肿瘤的发生密切相关[4-6]。因此,在肉制品工业中寻找NaCl的替代品,进而减少NaCl的添加量已成必然趋势。一些学者将氯化钾、氯化镁、氯化钙、乳酸钾、抗坏血酸钙、甘氨酸等作为NaCl的替代品[5,7-8],因氯化钾与氯化钠性质接近[9],很多学者对氯化钾替代氯化钠对肉制品品质的影响作了研究,包括感官、质构、水分活度、pH、脂肪氧化、脂肪酸组成、离子含量、色泽、盐渗透动力学、微生物、挥发性成份等方面的变化[10-14]。
脂肪氧化对火腿、腊肉、香肠等肉制品的质量至关重要,若脂肪氧化受限,则肉制品风味会比较平淡;若脂肪氧化过度,则会引起酸败、异味等质量问题[15-16]。关于肉制品加工中脂肪氧化和抗氧化的研究较多,关于肉制品中NaCl对脂肪氧化的影响也有很多探索,大都认为NaCl在一定浓度范围内会促进脂肪氧化,超过一定范围则会抑制脂肪氧化,如RHEE等[17]研究牛肉和鸡肉时发现2.5%的NaCl有最大促氧化效果;MIN等[18]报道氯化钠在2%左右时对肉制品促氧化作用最强,此后,随浓度增加,促氧化作用将逐渐减小。关于KCl部分替代NaCl后脂肪氧化的变化也有一些报道,但这些报道的结果并不一致,有的认为KCl部分替代NaCl后会促进肉中脂肪氧化[1,19],另一些研究则得到相反的结论[20-21]。究其原因,可能与各研究中盐浓度、加工条件不同有关,但同时也说明KCl部分替代NaCl后对肉制品脂肪氧化的影响还缺乏系统、深入研究。因此,为降低肉制品中NaCl含量,并为进一步寻找替代品奠定更好的理论依据,有必要对KCl或其它盐类部分替代NaCl后对脂肪氧化的动力学规律进行探究。根据一些学者的研究,当KCl的替代量超过40%~50%后会显著降低肉制品品质[10,22-23],现在干腌肉制品加工中常使用的NaCl浓度范围为3%~4%,因此本文拟研究在盐浓度为3%和4%时,15%~60%的NaCl被KCl取代后,猪肉肌内脂肪氧化包括初级氧化与次级氧化的动力学变化规律。
1. 材料与方法
1.1 材料与仪器
猪背最长肌 购于重庆市永辉超市,去掉表面可见脂肪、筋膜和结缔组织,真空包装后于−18 ℃保藏待用;NaCl(批号:20190112)、KCl(批号:20180718) 重庆金锦乐化工有限公司;三氯乙酸批号(20180326)、乙二胺四乙酸二钠(批号:20180628)、硫代巴比妥酸(批号:20180415) 、1,1,3,3-四乙氧基丙烷(批号:20170212)、冰乙酸(批号:20180522)、三氯甲烷(批号:20180627)、碘化钾(批号:20181106)、硫代硫酸钠(批号:20180824)、石油醚(批号:20181112) 、无水硫酸钠(批号:20180125) 均为分析纯(AR),成都市科龙化工试剂厂。
FSH-2A匀浆机 上海梅香仪器有限公司;BSC-259恒温恒湿箱 上海博迅实业有限公司;U-3900H分光光度计 日本Hitachi公司;JYS-A800绞肉机 山东九阳电器有限公司;RE-52AA旋转蒸发仪 上海亚荣生化仪器厂。
1.2 实验方法
1.2.1 样品处理
猪背最长肌样品于4 ℃解冻24 h,绞碎并混匀,平分为10组,每组1200 g,其中5组分别加入3%的盐,盐的组成分别为100%NaCl、85%NaCl+15%KCl、70%NaCl+30%KCl、55%NaCl+45%KCl、40%NaCl+60%KCl;另外5组分别加4%的盐(盐的组成同3%的5组猪背最长肌)。各组平均分成60份,每份20 g左右,分别用铝箔袋包装,不封口。每组的60份再平均分成4组,分别于15、20、25、30 ℃恒温箱中保温,每个温度条件下分别于5个时间点取样,每次取样3份(作为3个重复),具体每个处理的5个时间点根据预试验确定,温度高的处理时间相对较短,反之时间较长,以使每个时间点都能观察到明显的脂肪氧化(即POV和TBARS值的明显上升)以利于计算脂肪氧化常数,如15 ℃的保温时间分别为0、20、40、60、80 h,而30 ℃的保温时间分别为0、5、10、15、20 h。处理结束后,立即分析各样品的过氧化值(POV,Peroxide value)和硫代巴比妥酸反应物值(TBARS,Thiobarbituric acid reactive substances)。
1.2.2 脂肪氧化测定
脂肪氧化程度用POV值和TBARS值来衡量,其中POV值表示脂肪初级氧化,其测定根据GB5009.227-2016的滴定法;TBARS值表示脂肪次级氧化,其测定根据GB5009.181-2016的分光光度法。
1.2.3 脂肪氧化动力学研究
根据预试验和资料显示[24],在一定的温度下,脂肪氧化的动力学变化规律可以用一级反应动力学方程(1)进行描述。
ln(A/A0)=kt (1) 式中:A、A0分别为处理时间为t和0时的POV或TBARS值;t为保温处理时间,h;k为脂肪氧化速率常数,h−1。
因此,利用SPSS的线性回归程序,可从脂肪氧化值(POV或TBARS)的自然对数ln(A/A0)与时间t的一次回归直线斜率得到某一特定盐含量、温度条件下的脂肪氧化速率常数k。
Arrhenius方程(2)经常用来评价温度对反应速率常数k的影响,因此在本试验中也用来评定温度对脂肪氧化速率常数的影响,具体影响程度用反应活化Ea(kJ/mol)来衡量。
ln(k)=ln(k0)−EaRT (2) 式中:R为通用气体常数,8.314 J/(mol·K);T为温度,K;k0为指前因子。
同样,利用SPSS的线性回归程序,在不同盐含量或组成条件下,以ln(k)为因变量,−1/RT为自变量作线性回归分析,所得斜率即为不同盐含量和组成条件下的Ea。
1.3 数据统计分析
实验重复测定3 次,采用SPSS软件对数据进行处理,实验结果表示为平均值±标准差。
2. 结果与分析
2.1 脂肪氧化速率常数
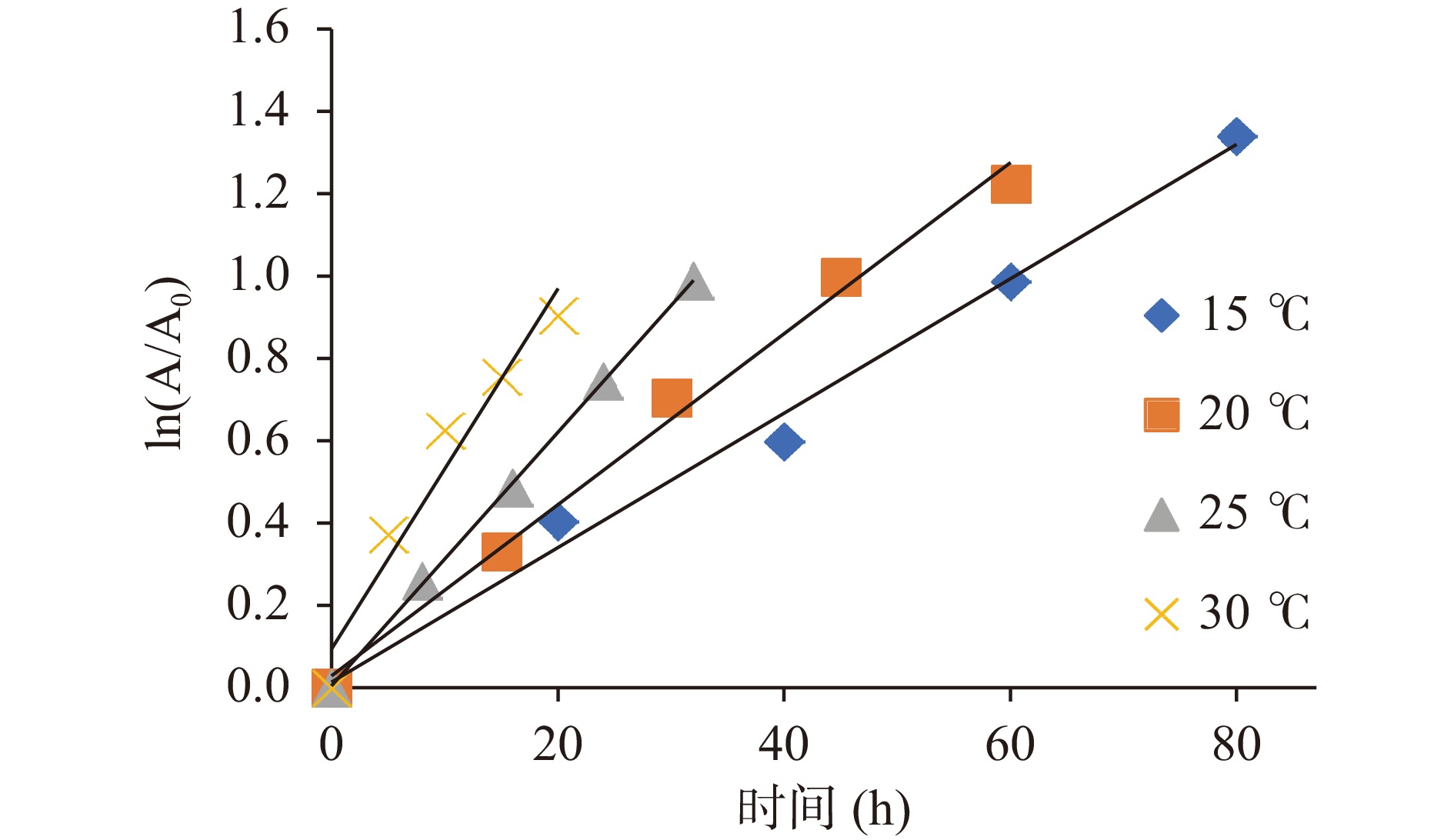
根据方程(1),在某一固定温度、盐含量和KCl替代比条件下,测得不同时间点样品的POV或TBARS值后,作ln(A/A0)对保温时间t的线性回归,得到各处理样品初级或次脂肪氧化的速率常数,分别如表1和表2所示。图1为添加3%NaCl时,在不同处理温度条件下POV值随时间的变化,可以看出,各温度条件下都能用一级反应动力学方程进行拟合(相关系数均在0.95以上),其余未在图中显示的处理得到的回归方程均显著(P<0.05)。因此,本试验用一级动力学方程拟合脂肪氧化速率常数是可行的。有报道显示在食品加工与贮藏过程中,大多与质量有关的品质变化都符合零级或一级反应动力学规律[24],特别是一级动力学是目前评价食品品质动力学变化的最常用模型[25]。关于脂肪氧化的速率常数,不同学者也进行了研究,王强[24]用一级动力学模型拟合了香肠贮藏过程中的脂肪氧化,而靳国锋[16]则用零级模型对五花肉的脂肪氧化进行了拟合。在预备试验中,本研究也同时采用两种模型进行了拟合,结果表明两种模型均能很好地拟合脂肪氧化速率,但一级动力学模型更显著,这可能与脂肪氧化启动较慢有关,再加上本研究选取的时间点都比较靠前以确保在研究范围内脂肪氧化处于上升阶段;也可能是由于脂肪氧化是介于零级与一级反应之间的一种混合模型。
表 1 不同含量及组成的盐对脂肪氧化(以POV衡量)速率常数和活化能的影响Table 1. Estimated reaction rate constant and activation energy for lipid oxidation measured by POV value with different content and component of salt盐添加量及组成 k(×10−3 h−1) 15 ℃ 20 ℃ 25 ℃ 30 ℃ Ea(kJ/mol) 3%盐含量 100%NaCl 16.3±0.8 20.8±1.1 30.8±1.3 43.9±2.0 48.81±1.73a 85%NaCl+15%KCl 14.8±0.7 19.7±1.3 28.4±1.6 42.6±1.9 51.31±1.59ab 70%NaCl+30%KCl 14.0±1.1 19.3±1.7 27.4±1.3 42.3±1.7 53.21±2.33bc 55%NaCl+45%KCl 13.1±0.9 17.6±1.0 26.9±1.5 41.5±1.4 56.33±2.08cd 40%NaCl+60%KCl 12.8±0.7 15.9±1.1 26.1±1.2 41.8±2.5 58.63±3.18d 4%盐含量 100%NaCl 14.0±0.5 19.8±0.9 27.6±1.3 43.1±1.6 53.77±3.07a 85%NaCl+15%KCl 14.3±1.1 21.4±0.6 28.7±1.0 44.5±2.1 53.71±1.98a 70%NaCl+30%KCl 15.4±1.4 22.3±1.2 30.5±0.8 45.2±2.4 51.45±2.37a 55%NaCl+45%KCl 16.1±0.6 22.8±1.3 31.7±1.1 46.1±2.5 50.61±1.19a 40%NaCl+60%KCl 15.8±0.9 21.9±0.7 29.8±1.4 45.1±1.9 50.13±2.30a 注:不同小写字母表示同一盐含量条件下活化能显著差异(P<0.05),表2同。 表 2 不同含量及组成的盐对脂肪氧化(以TBARS衡量)速率常数和活化能的影响Table 2. Estimated reaction rate constant and activation energy for lipid oxidation measured by TBARS value with different content and component of salt盐添加量及组成 k(×10−3 h−1) 15 ℃ 20 ℃ 25 ℃ 30 ℃ Ea(kJ/mol) 3%盐含量 100%NaCl 15.5±0.4 19.8±1.3 29.4±1.9 37.2±1.9 43.89±1.80a 85%NaCl+15%KCl 14.3±0.9 20.4±0.7 27.3±1.6 36.5±2.2 45.09±1.34a 70%NaCl+30%KCl 13.4±0.9 18.6±1.0 25.9±1.4 36.1±2.3 47.98±0.73b 55%NaCl+45%KCl 12.2±0.8 19.2±1.3 25.7±1.6 34.6±1.8 49.73±2.87bc 40%NaCl+60%KCl 11.5±0.9 17.4±0.9 24.3±0.9 33.3±2.4 51.22±1.71c 4%盐含量 100%NaCl 13.9±1.1 17.8±1.1 27.3±1.4 36.1±1.9 47.78±1.68a 85%NaCl+15%KCl 13.6±0.8 18.1±1.0 26.5±1.8 36.3±2.1 48.29±2.21a 70%NaCl+30%KCl 14.8±0.7 19.5±1.6 28.4±1.3 36.8±1.2 45.15±2.05a 55%NaCl+45%KCl 15.3±0.4 21.4±0.8 30.6±1.1 37.2±1.0 43.97±2.98a 40%NaCl+60%KCl 15.4±1.1 20.9±1.3 31.3±1.6 37.1±1.7 44.24±2.51a 就脂肪初级氧化而言,从表1可以看出,在固定盐含量和KCl替代比时,速率常数随温度的增加而增加,这说明温度的上升能增加脂肪的氧化;且温度越高,速率常数增加的幅度越大。当盐浓度固定在3%时,在同一温度下脂肪氧化速率常数随KCl替代比的增加而减少,这说明当KCl逐渐增加时,猪肉脂肪的氧化更慢,稳定性会增加。而当盐浓度为4%时,在同一温度下不同KCl替代比样品速率常数的变化不及3%时幅度大,且与3%时变化规律差异较大;速率常数先随KCl替代比的增加而增加,到45%替代比时达最大值,然后降低。这些差异的可能原因将在后面深入分析。
从表2可以看出,脂肪次级氧化速率常数大都低于相应的初级氧化速率常数,这可能是因为脂肪次级氧化是在初级氧化之后发生的,初级氧化的产物只有一部分分解为次级氧化产物。初级氧化的产物主要是一些氢过氧化物,但其很不稳定,一部分会很快分解为次级氧化产物,如一些小分子的醛、酮类。在固定盐含量和KCl替代比时,速率常数随温度的变化规律与初级氧化完全一致;在固定温度和盐浓度时,次级氧化速率常数随KCl替代比的变化虽与初级氧化速率常数相似,但规律性不及初级氧化明显,特别是在4%的NaCl浓度下,这可能是因为脂肪初级氧化先于次级氧化发生,因此更能反映脂肪氧化的整体情况。
2.2 盐含量3%时KCl替代比对脂肪氧化活化能的影响
利用SPSS的线性回归程序(方程2)可以求得各盐含量和组成条件下脂肪初级氧化与次级氧化的活化能,分别如表1和表2所示。利用方程(2)求出的各活化能差异显著(P<0.05),说明用Arrhenius方程进行脂肪氧化的拟合是可行的;各活化能均为正值,这进一步说明在某一特定盐含量和组成条件下脂肪氧化速率常数随温度的升高而增加。
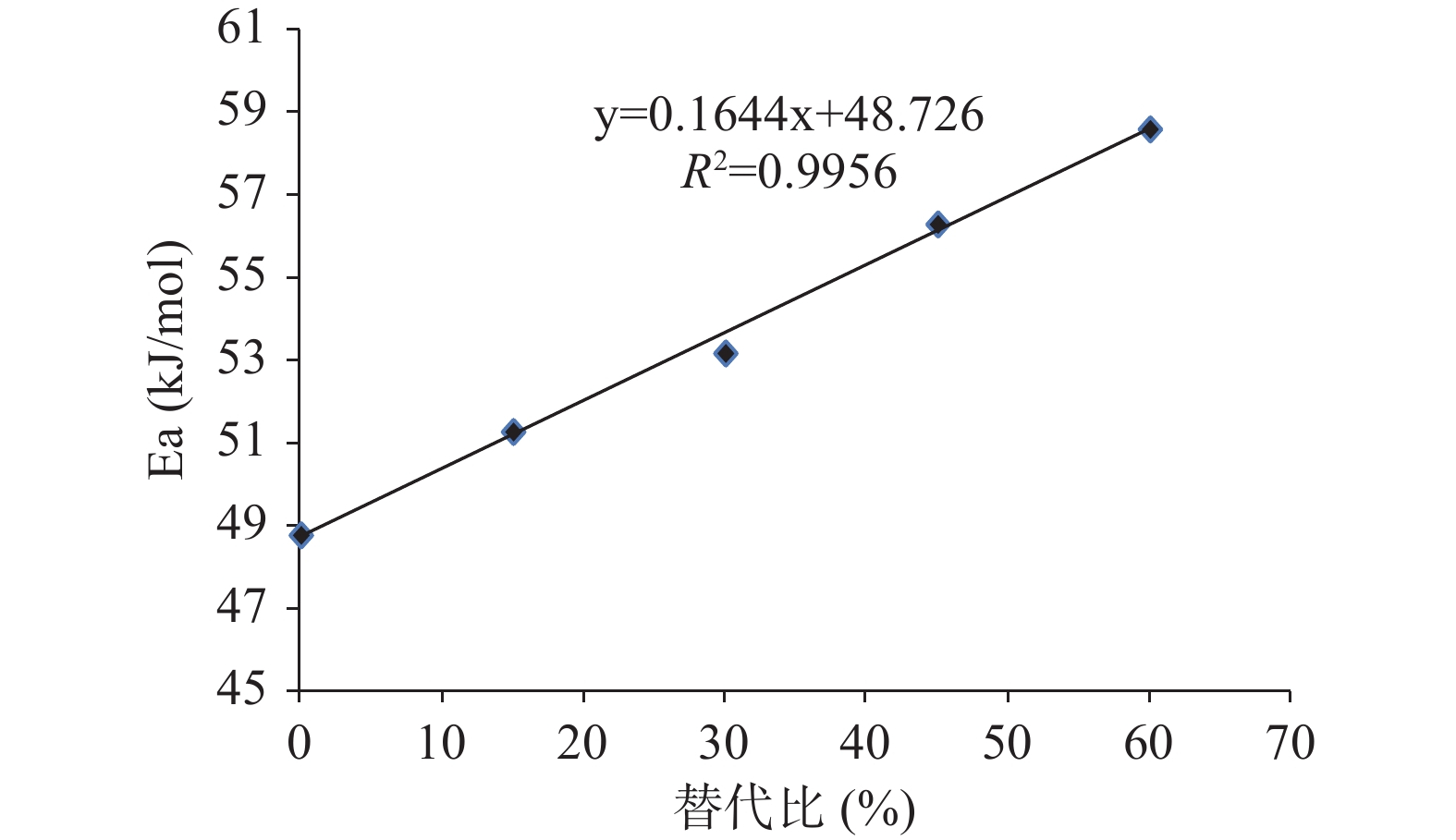
盐含量为3%时,从表1可以看出,脂肪初级氧化活化能随KCl替代比的增加显著增加(P<0.05),这说明在3%盐含量条件下,KCl比例增加后脂肪氧化所需克服的能量障碍更高,可以提高猪肉脂肪氧化稳定性。很多研究都显示NaCl浓度较低时,盐浓度的增加会促进肉中脂肪氧化,但当NaCl超过一定含量时,又会降低脂肪的氧化,但临界点在不同的研究中有所不一样,如张东[26]发现腊肉加工中2%或3%的NaCl会促进脂肪氧化,而4%及以上脂肪氧化明显降低;MIN[18]、RHEE[17]、靳国锋[16]分别报道氯化钠在2%、2.5%和3.1%时促氧化作用最强。因此可以推断,本研究中在3%的NaCl浓度范围内,NaCl浓度的提高会促进肉中脂肪氧化;当氯化钠被部分氯化钾替代后,因相同质量浓度KCl的离子强度低于NaCl,再加上同等离子强度的氯化钾对脂肪氧化的促进作用低于氯化钠[27],以及KCl可能会激活肉中的一些抗氧化酶[28],如谷胱甘肽过氧化酶,因此在盐含量3%时,脂肪初级氧化活化能随KCl替代比的增加显著增加。本研究的结果与ZANARDI[29]报道的有所差异,其在研究意大利腊肠加工中盐总量为2.7%,当50%被氯化物(钾、镁、钙)替代时,脂肪氧化反而被加强,这可能与加工条件的不同有关,他们的研究是在实际加工中,且加入了亚硝酸盐等调料;也可能与他们加入的二价离子镁盐和钙盐有关。将活化能随KCl替代比的变化用SPSS的曲线回归进行拟合,发现线性模型的拟合性高,如图2所示,拟合的模型为:Ea=0.164X+48.726(X为KCl替代分比),模型的决定系数为0.9956。
从图2可以看出,在3%盐浓度条件下,次级氧化的活化能变化规律与初级氧化相似,也随KCl替代比的增加显著增加(P<0.05),但活化能值均低于初级氧化,这显示脂肪初级氧化对温度比次级氧化有更高的敏感性;也说明脂肪初级氧化需要克服的能量障碍高于次级氧化,即一旦初级氧化启动后,次级氧化会很快发生,不需要额外的能量。这与靳国锋[16]研究五花肉脂肪氧化的结果是一致的,但与王强[24]研究香肠中脂肪氧化时得到的结果不一致,这可能与研究对象不同有关。同样,次级氧化活化能随KCl替代比的增加可用线性模型进行拟合,拟合的模型为Ea=0.129X+43.722,模型的决定系数为0.984。初级与次级氧化拟合的一致性,说明两者均可用来表征肉中氧化,同时说明本研究中采用的模型有效。
一些研究者也报道过脂肪氧化的活化能,靳国锋[16]测得无NaCl存在时,五花肉的一级、二级脂肪氧化活化能分别为92.35、65.66 kJ/mol,1%~5%的NaCl浓度下一次、二次氧化活化能分别为54.75~68.29 kJ/mol、45.82~50.30 kJ/mol,与本研究得到的活化能值相近。王强[25]报道香肠贮藏过程中初级和次级氧化的活化能分别为37.68、51.38 kJ/mol,其中初级氧化的活化能值明显低于本研究,可能与实验条件和原料不一致有关。另外,GHOSH[30]发现向日葵和芝麻混合油的氧化活化能为92.05~99.17 kJ/mol,YESILSU[31]报道微胶囊鱼油中脂肪氧化活化能最高不超过31.62 kJ/mol,可以看出,鱼油的脂肪氧化活化能明显偏低,这可能与鱼中多不饱和脂肪酸含量高有关。
2.3 盐含量4%时KCl替代比对脂肪氧化速率常数和活化能的影响
从表1和表2可以看出,当盐含量为4%时,KCl替代比对脂肪氧化活化能的影响规律明显不同于3%盐浓度时。无论是初级氧化还是次级氧化,不同比例的KCl替代均对活化能没有显著影响(P>0.05),因此可认为在4%盐浓度条件下,KCl的添加对脂肪氧化影响较小。虽然活化能间没有显著差异,但也存在一些小的变化规律,对初级氧化而言,当KCl替代比为15%时,相对于对照组活化能基本不变,而当KCl替代比超过30%时,活化能随KCl替代比的增加线性减小,线性模型为:Ea=−0.062X+53.588(X为KCl替代分比),模型的决定系数为0.973。对次级氧化而言,活化能的变化与初级氧化相似,当KCl替代比为15%时活化能基本不变,当KCl替代比超过30%时,活化能明显减小,但随KCl替代比的增加并不呈线性变化的趋势。因此,可以推测,当KCl替代比大于30%时,可降低脂肪氧化稳定性。这可能是由于NaCl在3%左右时对脂肪氧化有最大促进作用,而其浓度进一步增加时,会表现出对脂肪氧化的逐渐抑制;在4%的NaCl浓度条件下,随着KCl替代比的增加,肉中总的离子强度会减小,再加上同等离子强度的氯化钾对脂肪氧化的促进作用低于氯化钠[27],因此,随KCl替代比的增加会使盐对脂肪氧化的促进作用更趋近于3%的NaCl,相比于4%的NaCl替代组会促进脂肪氧化;但另一方面KCl能更好地保留肉中一些抗氧化酶的活性以提高肉中脂肪氧化稳定性[28],因此两相抵消,表现出活化能相对于没有添加KCl的样品变化差异不显著。
很多学者都研究了肉中KCl部分替代NaCl后对脂肪氧化的影响,有的认为KCl部分替代NaCl后会促进肉中脂肪氧化[1,19],另一些研究则得到相反的结论[20-21]。究其原因,除了可能与加工条件、原料以及加入的辅料不同有关外,从本研究可以看出,也与所使用的盐含量及以氯化钾的替代比有关。因此,实际肉制品加工中,可通过盐含量及组成的不同来调控脂肪氧化,一般情况下,3%的盐添加量并用40%~50%氯化钾替代氯化钠可以实现低盐目标及提高产品的氧化稳定性;在一些干腌肉制品加工中,有时候需要适当促进脂肪氧化以形成独特风味,另外为了增加产品的保藏性也需适当提高盐浓度,因此可以添加4%左右的盐,并用30%~50%的氯化钾替代氯化钠,这样在不增加消费者氯化钠摄入量的前提下,仍可以促进产品风味物质的产生及增加产品的保藏性。
3. 结论
在3%和4%盐浓度和15~30 ℃条件下,猪肉脂肪初级氧化速率常数大都大于次级氧化速率常数;当盐的组成和浓度不变时,脂肪氧化速率常数随温度而增加;当温度不变时,初级氧化速率常数在3%盐浓度时随KCl替代比的增加而减小;在4%盐含量时,随KCl替代比的增加先增加后减少,在45%替代比时达最大值;而脂肪次级氧化速率常数随KCl替代比的变化规律性不强。在处理条件相同时,脂肪初级氧化活化能大于次级氧化;总盐浓度3%时,随KCl替代比的增加,初级和次级氧化活化能均呈线性显著增加(P<0.05);总盐浓度为4%时,KCl替代比的变化对脂肪初级及次级氧化活化能无显著影响(P>0.05),但在替代比大于30%时,有使活化能减小的趋势。猪肉加工中,若KCl部分替代NaCl,当总盐浓度为3%左右时,脂肪的氧化稳定性会随KCl替代比的增加而增加;而当盐的总浓度为4%时,KCl的替代对脂肪氧化稳定性影响不显著,在替代比大于30%时有降低脂肪氧化稳定性的趋势。
-
表 1 不同含量及组成的盐对脂肪氧化(以POV衡量)速率常数和活化能的影响
Table 1 Estimated reaction rate constant and activation energy for lipid oxidation measured by POV value with different content and component of salt
盐添加量及组成 k(×10−3 h−1) 15 ℃ 20 ℃ 25 ℃ 30 ℃ Ea(kJ/mol) 3%盐含量 100%NaCl 16.3±0.8 20.8±1.1 30.8±1.3 43.9±2.0 48.81±1.73a 85%NaCl+15%KCl 14.8±0.7 19.7±1.3 28.4±1.6 42.6±1.9 51.31±1.59ab 70%NaCl+30%KCl 14.0±1.1 19.3±1.7 27.4±1.3 42.3±1.7 53.21±2.33bc 55%NaCl+45%KCl 13.1±0.9 17.6±1.0 26.9±1.5 41.5±1.4 56.33±2.08cd 40%NaCl+60%KCl 12.8±0.7 15.9±1.1 26.1±1.2 41.8±2.5 58.63±3.18d 4%盐含量 100%NaCl 14.0±0.5 19.8±0.9 27.6±1.3 43.1±1.6 53.77±3.07a 85%NaCl+15%KCl 14.3±1.1 21.4±0.6 28.7±1.0 44.5±2.1 53.71±1.98a 70%NaCl+30%KCl 15.4±1.4 22.3±1.2 30.5±0.8 45.2±2.4 51.45±2.37a 55%NaCl+45%KCl 16.1±0.6 22.8±1.3 31.7±1.1 46.1±2.5 50.61±1.19a 40%NaCl+60%KCl 15.8±0.9 21.9±0.7 29.8±1.4 45.1±1.9 50.13±2.30a 注:不同小写字母表示同一盐含量条件下活化能显著差异(P<0.05),表2同。 表 2 不同含量及组成的盐对脂肪氧化(以TBARS衡量)速率常数和活化能的影响
Table 2 Estimated reaction rate constant and activation energy for lipid oxidation measured by TBARS value with different content and component of salt
盐添加量及组成 k(×10−3 h−1) 15 ℃ 20 ℃ 25 ℃ 30 ℃ Ea(kJ/mol) 3%盐含量 100%NaCl 15.5±0.4 19.8±1.3 29.4±1.9 37.2±1.9 43.89±1.80a 85%NaCl+15%KCl 14.3±0.9 20.4±0.7 27.3±1.6 36.5±2.2 45.09±1.34a 70%NaCl+30%KCl 13.4±0.9 18.6±1.0 25.9±1.4 36.1±2.3 47.98±0.73b 55%NaCl+45%KCl 12.2±0.8 19.2±1.3 25.7±1.6 34.6±1.8 49.73±2.87bc 40%NaCl+60%KCl 11.5±0.9 17.4±0.9 24.3±0.9 33.3±2.4 51.22±1.71c 4%盐含量 100%NaCl 13.9±1.1 17.8±1.1 27.3±1.4 36.1±1.9 47.78±1.68a 85%NaCl+15%KCl 13.6±0.8 18.1±1.0 26.5±1.8 36.3±2.1 48.29±2.21a 70%NaCl+30%KCl 14.8±0.7 19.5±1.6 28.4±1.3 36.8±1.2 45.15±2.05a 55%NaCl+45%KCl 15.3±0.4 21.4±0.8 30.6±1.1 37.2±1.0 43.97±2.98a 40%NaCl+60%KCl 15.4±1.1 20.9±1.3 31.3±1.6 37.1±1.7 44.24±2.51a -
[1] 唐静. KCl部分替代NaCl对干腌火腿脂肪氧化及风味物质形成的影响[D]. 南京: 南京农业大学, 2015: 17−29. TANG J. Influence of partial substitution of NaCl by KCl on fat oxidation and the formation of flavor compounds in day-cured ham[D]. Nanjing: Nanjing Agricultural university, 2015: 17−29.
[2] 马晓丽, 黄雅萍, 张龙涛, 等. 肉制品加工中的低钠策略研究[J]. 食品与发酵工业,2019,54(14):256−262. [MA X L, HUANG Y P, ZHANG L T, et al. Strategies for sodium reduction in meat products: A review[J]. Food and fermentation industries,2019,54(14):256−262. [3] MESIAS M, HOLGADO F, MARQUEZ-RUIZ G, et al. Effect of sodium replacement in cookies on the formation of process contaminants and lipid oxidation[J]. LWT-Food Science and Technology,2015,62(1):633−639. doi: 10.1016/j.lwt.2014.11.028
[4] OH Y S, APPEL L J, GALIS Z S, et al. National heart, lung, and blood institute working group report on salt in human health and sickness building on the current scientific evidence[J]. Hypertension, Hypertension,2016,68(2):681−688.
[5] INGUGLIA E S, ZHANG Z, TIWARI B K, et al. Salt reduction strategies in processed meat products-A review[J]. Trends in Food Science & Technology,2017,59:70−78.
[6] 张东, 李洪军, 吴练军, 等. 减少肉制品中氯化钠含量的研究进展[J]. 食品与发酵工业,2017,43(11):238−243. [ZHANG D, LI H J, WU L J, et al. Research progress on reducing sodium chloride in meat products[J]. Food and Fermentation Industries,2017,43(11):238−243. [7] 丁习林, 王桂瑛, 王雪峰, 等. 肉制品加工中镁盐部分替代氯化钠的应用研究进展[J]. 食品工业科技,2019,40(17):327−332,339. [DING X L, WANG G Y, WANG X F, et al. Application research progress of the partial replacement of sodium chloride by magnesium salt in meat processing[J]. Science of Technology of Food Industry,2019,40(17):327−332,339. [8] HUANG J W, JIN S K, HUR S J, et al. Quality changes in fat-reduced sausages by partial replacing sodium chloride with other chloride salts during five weeks of refrigeration[J]. LWT - Food Science and Technology,2018,97:818−824. doi: 10.1016/j.lwt.2018.08.004
[9] PIETRASIK Z, GAUDETTE N J, JOHNSTON S P. The use of high pressure processing to enhance the quality and shelf life of reduced sodium naturally cured restructured cooked hams[J]. Meat Science,2016,116(6):102−109.
[10] LORENZO J M, BERMUDEZ R, DOMINGUEZ R, et al. Physicochemical and microbial changes during the manufacturing process of dry-cured lacon salted with potassium, calcium and magnesium chloride as a partial replacement for sodium chloride[J]. Food Control,2015,50:763−769. doi: 10.1016/j.foodcont.2014.10.019
[11] ALINO M, GRAU R, BAIGTS D, et al. Influence of sodium replacement on the salting kinetics of pork loin[J]. Journal of Food Engineering,2009,95(4):551−557. doi: 10.1016/j.jfoodeng.2009.06.016
[12] SANTOS B A, CAMPAGNOL P C B, FAGUNDES M B, et al. Generation of volatile compounds in Brazilian low-sodium dry fermented sausages containing blends of NaCl, KCl, and CaCl2 during processing and storage[J]. Food Research International,2015,74:306−314. doi: 10.1016/j.foodres.2015.04.042
[13] 丁习林, 王桂瑛, 邹颖玲, 等. 基于气相色谱-离子迁移谱结合多元统计学分析KCl部分替代NaCl对宣威火腿挥发性风味化合物的影响[J]. 食品科学,2020,41(24):190−198. [DING X L, WANG G Y, ZOU Y L, et al. Influence of partial replacement of NaCl with KCl on the volatile compounds of Xuanwei ham investigated by gas chromatography-ion mobility spectrometry combined with multivariate statistical analysis[J]. Food Science,2020,41(24):190−198. doi: 10.7506/spkx1002-6630-20191226-311 [14] 陈文彬, 黎良浩, 王健, 等. 部分KCl替代NaCl对强化高温成熟工艺干腌火腿肌肉色泽形成的影响[J]. 食品科学,2017,38(17):77−84. [CHEN W B, LI L H, WANG J, et al. Effect of partial replacement of NaCl with KCl combined with high-temperature ripening on color formation in dry-cured hams[J]. Food Science,2017,38(17):77−84. doi: 10.7506/spkx1002-6630-201717014 [15] MOTTRAM D S. Flavour formation in meat and meat products: a review[J]. Food Chemistry,1998,62(4):415−424.
[16] 靳国锋. 干腌培根加工过程中脂肪氧化调控机制研究[D]. 南京: 南京农业大学, 2011: 97−109. JING G F. Study on the mechanism of fat oxidation regulation during the processing of dry-cured bacon[D]. Nanjing: Nanjing Agricultural University, 2011: 97−109.
[17] RHEE K S, ZIPRIN Y A. Pro-oxidative effects of NaCl in microbial growth-controlled and uncontrolled beef and chicken[J]. Meat Science,2001,57(1):105−112. doi: 10.1016/S0309-1740(00)00083-8
[18] MIN B, AHN D U. Mechanism of lipid peroxidation in meat and meat products-a review[J]. Food Science and Biotechnology,2005,14(1):152−163.
[19] RIPOLLES S, CAMPAGNOL P C B, ARMENTEROS M, et al. Influence of partial replacement of NaCl with KCl, CaCl2 and MgCl2 on lipolysis and lipid oxidation in dry-cured ham[J]. Meat Science,2011,89(1):58−64. doi: 10.1016/j.meatsci.2011.03.021
[20] 张维悦, 夏杨毅, 侯佰慧, 等. KCl 部分替代NaCl对腊肉脂肪氧化和脂肪酸变化的影响[J]. 食品与发酵工业,2018,44(9):156−162. [ZHANG W Y, XIA Y Y, HOU B H, et al. Influence of partial replacement of NaCl with KCl on lipid oxidationand fatty acid composition of cured meat[J]. Food and Fermentation Industries,2018,44(9):156−162. [21] KING A J, EARLL A. Effect of selected sodium and potassium salts on TBA values of dark meat Turkey patties[J]. Journal of Food Science,1988,53(3):723−726. doi: 10.1111/j.1365-2621.1988.tb08940.x
[22] WU H, ZHANG Y Y, LONG M, et al. Proteolysis and sensory properties of dry-cured bacon as affected by the partial substitution of sodium chloride with potassium chloride[J]. Meat Science,2014,96(3):1325−1331. doi: 10.1016/j.meatsci.2013.10.037
[23] PARK J N, HWANG K T, KIM S B, et al. Partial replacement of NaCl by KCl in salted mackerel (Scomber japonicus) fillet products: effect on sensory acceptance and lipid oxidation[J]. International Journal of Food Science and Technology 2009, 44(8), 1572−578.
[24] 王强. 香肠脂肪氧化动力学特性及温度对其影响研究[J]. 食品科学,2013,34(11):130−133. [WANG Q. Kinetic charateristics of lipid oxidation in sausages as affected by temperature[J]. Food Science,2013,34(11):130−133. doi: 10.7506/spkx1002-6630-201311029 [25] OILLIC S, LEMOINE E, GROS J B, et al. Kinetic analysis of cooking losses from beef and other animal muscles heated in a water bath-effect of sample dimensions and prior freezing and ageing[J]. Meat Science,2011,88(3):338−346. doi: 10.1016/j.meatsci.2011.01.001
[26] 张东, 李洪军, 王鑫月, 等. 食盐添加量对腊肉品质的影响[J]. 食品与发酵工业,2017,43(11):159−164,171. [ZHANG D, LI H J, WANG X Y, et al. Effect of different amounts of salt on the quality of Chinese bacon[J]. Food and Fermentation Industries,2017,43(11):159−164,171. [27] RHEE K S, SMITH G C, TERRELL R N. Effect of reduction and replacement of sodium chloride on rancidity development in raw and cooked pork[J]. Journal of Food Protection,1983,46(7):578−581. doi: 10.4315/0362-028X-46.7.578
[28] HERNANDEZ P, PARK D, RHEE K S. Chloride salt type/ionic strength, muscle site and refrigeration effects on antioxidant enzymes and lipid oxidation in pork[J]. Meat Science,2002,61(4):405−410. doi: 10.1016/S0309-1740(01)00212-1
[29] ZANARDI I E, GHIDINI S, CONTER M, et al. Mineral composition of Italian salami and effect of NaCl partial replacement on compositional, physico-chemical and sensory parameters[J]. Meat Science,2010,86(3):742−747. doi: 10.1016/j.meatsci.2010.06.015
[30] GHOSH M, UPADHYAY R, MAHATO D K, et al. Kinetics of lipid oxidation in omega fatty acids rich blends of sunflower and sesame oils using Rancimat[J]. Food Chemistry,2018,272:471−477.
[31] YESILSU A F, ÖZYURT G. Oxidative stability of microencapsulated fish oil with rosemary, thyme and laurel extracts: a kinetic assessment[J]. Journal of Food Engineering,2018,240:171−182.







 下载:
下载:
 下载:
下载:
