Effect of High Intensity Ultrasound on the Conformational and Physicochemical Properties of Soy 7S and 11S Globulin
-
摘要: 以大豆7S和11S球蛋白为对象,研究了高强度超声处理(150、450、1350 W)在不同时间条件(15、30 min)下对7S和11S结构和理化性质的影响。结果表明:超声处理不改变7S和11S的一级结构,但能够使二级结构中各组分含量发生改变。同时,7S和11S的荧光强度在超声处理后降低,表面疏水性(H0)显著增加(P<0.05)。粒径分布测定显示7S和11S经超声处理后液滴粒径分布更加均匀,蛋白溶液的稳定性有所提升。DSC结果可以看出,超声后7S的焓值(ΔH)从1.22 J/g最多下降至0.17 J/g,11S从1.41 J/g最多下降至0.53 J/g,展开蛋白质结构所需的能量更少。在理化性质方面,超声处理后7S和11S的乳化活性和乳化稳定性显著增加(P<0.05),溶解度最多分别提高了12.85%和10.57%。此外,冷冻扫描电子显微镜(Cryo-SEM)观察微观结构显示,7S和11S超声后从较为有序的网状聚集状态转变为无序的状态。因此,采用高强度超声处理能够显著影响7S和11S的结构和理化性质。Abstract: The effects of high intensity ultrasound treatment (150, 450, 1350 W) on the conformational and physicochemical properties of soy 7S and 11S globulin for different durations (15, 30 min) were investigated. The results showed that ultrasound treatment did not change the primary structures of 7S and 11S, but were able to change the content of the components in the secondary structure. Ultrasound treatment resulted varying degrees of reduction in fluorescence intensity and a significant increase (P<0.05) in surface hydrophobicity (H0) for 7S and 11S. Particle size distribution measurements showed that the droplets of 7S and 11S were more uniformly distributed after ultrasound treatment and that the stability of the protein solutions was improved. Differential scanning calorimetry (DSC) results showed that the enthalpy (ΔH) decreased from 1.22 J/g to 0.17 J/g for 7S and from 1.41 J/g to 0.53 J/g for 11S after sonication, requiring less energy to unfold the protein structure. In terms of physicochemical properties, the emulsification activity and emulsion stability of 7S and 11S increased significantly (P<0.05) after sonication, and the solubility increased by up to 12.85% and 10.57%, respectively. In addition, cryo-scanning electron microscopy (Cryo-SEM) observations revealed that the microstructure of 7S and 11S changed after sonication from a more ordered reticular aggregated state to a disordered state. Thus, high intensity ultrasound treatment can obviously affect the structure and physicochemical properties of 7S and 11S.
-
Keywords:
- soy protein /
- 7S/11S /
- high intensity ultrasound /
- structure /
- physicochemical properties
-
大豆蛋白组分按离心过程中的沉淀性质可以分为四种—2S、7S、11S和15S,其中7S和11S球蛋白是大豆蛋白的主要成分,占总量的65%~80%[1]。7S主要组成部分为β-伴大豆球蛋白,分子量约150~200 kDa,糖含量约为5%,是由β(~47.8 kDa)、α(~63.5 kDa)和α'(~67.2 kDa)三个亚基通过氢键、静电相互作用和疏水相互作用组成的三聚糖蛋白[2]。11S主要组成部分为大豆球蛋白,分子量约为320~375 kDa,是一种六聚体蛋白质,它由两个重叠的六边形环组成,由酸性亚基A(~38 kDa)和碱性亚基B(~20 kDa)通过疏水相互作用和静电相互作用结合在一起[3]。有研究将六聚体中的五个亚基分为两个亚基组合,根据氨基酸序列的特点分为亚基组Ⅰ(A1aB2,A1bB1b和A2B1a)和亚基组Ⅱ(A3B4和A5A4B3)。作为大豆蛋白的两个主要组成部分,7S和11S由于其结构的固有差异,会影响大豆蛋白的功能特性。然而,天然大豆蛋白具有紧密的球状结构,因此其功能性会被其复杂的结构所限制。因此,需要对大豆蛋白进行结构改造,使其具有更高的表面活性状态,以改善特定的功能性质,这可以通过物理、化学或酶法来实现[4]。
超声处理是一种非热加工技术,具有环境友好、节能、无毒、相对经济和易于操作的特点[5]。超声处理的应用被认为是食品工业的一个潜在增长领域,在提高食品质量方面具有良好的效果[6]。超声波可分为两种类型,即高频低强度(100 kHz~1 MHz,强度<1 W/cm2)和低频高强度(16~100 kHz,强度10~2000 W/cm2)[7]。低频高强度超声也被称为“功率超声”,广泛用于改变食品的特性[8]。
近年来,高强度超声处理作为一种可以改变蛋白质结构和性质的物理方法,一直是研究的热门话题。以往的研究表明,超声处理可以破坏大豆蛋白的非共价相互作用从而改变其结构[9]。Morales等[10]发现,大豆蛋白在20 kHz、4.27 W的超声处理下,蛋白的粒径减小。Huang等[1]的研究表明,当超声时间较短时,大豆蛋白样品α-螺旋含量较低,无规卷曲量较高;而在较长时间(超过20 min)处理的中则相反,样品α-螺旋较高,无规卷曲含量较低,说明蛋白的二级结构发生了改变。Zheng等[11]的研究发现,超声处理还可以有效地提升大豆分离蛋白的疏水性和巯基含量。然而目前,超声处理对7S和11S的结构和理化性质的影响少有报道,也缺乏关于超声对二者热特性影响的研究。另外,在以往的研究中,高强度超声处理蛋白的应用通常被限制在100 W/cm2以下的相对较小的范围内。
因此,本研究通过施加更高功率(150 、450 、1350 W)不同时间(15 、30 min)的超声处理,探究7S和11S二三级结构、粒径分布、微观形貌、溶解性、乳化性等结构和功能性质以及热特性在超声后的变化,为高强度超声处理在大豆蛋白开发利用方面的研究提供进一步的理论基础。
1. 材料与方法
1.1 材料与仪器
大豆 东北农业大学农学院提供;大豆油 九三粮油工业集团有限公司;十二烷基硫酸钠聚丙烯酰胺凝胶电泳(Sodium-dodecyl-sulfate polyacrylamide gel electrophoresis, SDS-PAGE)制备试剂盒、2×蛋白上样缓冲液、彩虹广谱蛋白分子量标准品 北京索莱宝科技有限公司;尿素(Urea)、三羟甲基氨基甲烷(Tris)、十二烷基磺酸钠(Sodium dodecyl sulfate,SDS)、甘氨酸 美国Amresco公司;β-巯基乙醇 Geniview公司; 考马斯亮蓝R-250 国药集团化学试剂有限公司;8-苯胺-1-萘磺酸(ANS) 美国Sigma-Aldrich;其它所有化学试剂 均为国产分析纯。
XH-300A+电脑微波超声波组合合成萃取仪 北京祥鹄科技发展有限公司;KjelFlex K-370凯氏定氮仪 瑞士步琦公司;Mini-PROTEAN Trtra垂直电泳槽 Bio-Rad公司;Gel DocTM EZ imager 凝胶电泳成像系统 Bio-Rad公司;MAGNA-IR560 傅里叶红外光谱仪 梅特勒-托利多国际贸易有限公司;RF-6000 型荧光分光光度计 日本岛津公司;NANO ZS90 粒度及电位分析仪 英国马尔文仪器有限公司;DSC Q2000 差示扫描量热仪 美国TA仪器公司;SU8010 场发射扫描电子显微镜(配备PP3010T型冷冻传输系统) 日本日立公司。
1.2 实验方法
1.2.1 7S和11S的制备
7S和11S按照Matsumura等[12]的方法制备。将成熟大豆磨碎成细粉,按1:5(w/w)的比例用正己烷脱脂。将脱脂豆粉分散在去离子水(1:8,w/v)中,用2.0 mol/L NaOH调pH至8.0,在20 °C下连续搅拌1 h后,将分散液在10000×g,4 °C下离心30 min收集上清液。收集的上清液中加入1.0 mmol/L的还原剂Na2SO3以增加蛋白质的溶解度,并用2.0 mol/L的HCl调节溶液的pH至5.8。然后将溶液在6500×g离心30 min,沉淀得到11S粗品。分离后得到的剩余水相部分,用2.0 mol/L盐酸调节至pH5.0。将酸化后的样品在室温下搅拌1 h,然后在10000×g和4 °C下再次离心30 min。收集上清液,使用2.0 mol/L的HCl调pH至4.5并离心(20 min,6500×g,4 °C),分离得到7S粗品。将分离出的7S或11S粗品分散在去离子水中,用2.0 mol/L的NaOH调节pH至中性,然后用去离子水洗涤3次。将7S和11S冷冻干燥,并储存在干燥器中。用凯氏定氮法[13]测定出制得的7S和11S样品的蛋白质含量分别为92.21%和93.37%。
1.2.2 7S和11S的超声处理
将等量的7S和11S分散于去离子水(1:25,w/v)中,搅拌2 h,用NaOH(2.0 mol/L)调节溶液的pH至7.0。分别对7S和11S溶液进行超声处理,频率为20 kHz,功率输出为150、450和1350 W,超声处理时间设定为15 min和30 min。通过浸泡在冰水浴中,样品在整个超声处理过程中一直保持在较低的温度。然后将7S和11S在4 °C下保存或冻干以备后续分析。由于超声系统中能量的损失,介质中的实际超声能量水平低于设定的输出功率。因此,实际的超声强度是通过量热法[14]确定的,基于实验前30 s内的温度升高值进行计算。当输出功率为150、450和1350 W时,计算出实际超声强度分别为18.31、44.75和111.86 W/cm2。
1.2.3 十二烷基硫酸钠-聚丙烯酰胺凝胶电泳
十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)参考Wu等[15]之前描述的方法进行。将冻干的7S和11S溶解在SDS-PAGE缓冲液(0.124 mol/L Tris-HCl,15%甘油,2% SDS,5% β-巯基乙醇和0.0025%溴酚蓝,pH=6.8)中,蛋白质浓度为4 mg/mL,然后在100 °C的水中煮沸5 min,以10000×g离心3 min。将10 μL上清液上样至凝胶上。分别在80 V和120 V的电压下在浓缩胶和分离胶中进行电泳。用考马斯亮蓝R-250染色,并在脱色液(40%甲醇和10%冰醋酸)中脱色过夜。使用带有Image Lab软件的凝胶成像分析系统对凝胶进行拍照。
1.2.4 傅里叶变换红外光谱分析
根据本课题组以前研究中的实验方法[16],用傅里叶变换红外光谱(FTIR)表征超声处理前后7S和11S的二级结构。冻干的7S和11S与KBr按照1:10的比例充分混合进行研磨,压片放入托盘中。然后,托盘被转移到样品架上进行光谱扫描。光谱仪的分辨率设定为4 cm−1,进行11次扫描。用PeakFit Version 4.12软件对酰胺I、II和III带的数据进行去卷积、峰分离和拟合分析,通过高斯积分面积计算7S和11S二级结构各组分的含量百分比。
1.2.5 内源荧光光谱分析
将超声处理前后的7S和11S溶解在0.01 mol/L的PBS缓冲液(pH7.0)中,使样品最终浓度为0.05 mg/mL。将样品溶液置于石英比色皿中进行内源荧光光谱分析,激发波长设置为280 nm,激发和发射狭缝宽度均设置为5 nm。发射波长范围为300~450 nm,扫描速度为10 nm/s。
1.2.6 粒径分布分析
由Wu等[15]描述的方法进行粒径分布测定。将冻干的7S和11S溶解在PBS(0.01 mol/L,pH7.0)中,以达到0.5 mg/mL的最终浓度。然后将分散液通过醋酸纤维素水溶液滤膜(颗粒保留率0.45 μm)过滤,以去除不溶性部分。使用Zetasizer Nano ZS90粒径电位分析仪将1 mL滤液加入到透明的zeta cell中进行粒度测定。
1.2.7 表面疏水性的测定
根据Kato等 [17]的方法,用1-苯胺基-8-萘磺酸(ANS)作为荧光探针测定表面疏水性。将冻干的7S和11S分散在0.1 mol/L PBS(pH7.0)中,在室温下搅拌1 h,然后离心(10000×g,30 min)。上清液用0.1 mol/L PBS(pH7.0)稀释得到0.05~0.4 mg/mL不等的梯度浓度,蛋白质浓度由Lowry法[18]测定。将40 μL ANS溶液(0.008 mol/L ANS溶解在0.1 mol/L PBS缓冲液中,pH7.0)与每个样品的4 mL混合,并在黑暗中静置3 min。用荧光光谱仪在波长390 nm(激发)和470 nm(发射)下测定样品荧光强度。绘制荧光强度与蛋白质浓度的关系图,线性回归分析计算的初始斜率取为H0。
1.2.8 差示扫描量热法分析
使用DSC Q2000热分析仪检测样品的热变化。冻干的7S和11S按照Ren等[19]描述的方法进行处理。准确地称取每个样品2 mg放在铝制坩埚中。然后,用0.01 mol/L PBS(pH7.0)以约1:5(w/v)的比例润湿样品后密封。坩埚置于室温下24 h以达到平衡,然后在氮气环境下以5 °C/min的速度从25 °C加热到110 °C,测定其热吸收曲线。以密封的空坩埚作为参照物。
1.2.9 溶解度测定
根据Nazari等 [20]的方法测定溶解度。用去离子水稀释7S和11S分散液至1%(w/w)的浓度,并调整pH至7.0。将等体积的各个样品在23 ℃下以20000×g离心15 min。使用Lowry法[18]测定上清液中的蛋白质含量,并使用牛血清白蛋白作为标准品。随后用下式计算蛋白质的溶解度:
溶解度(%)=m1m2×100 (1) 式中:m1表示上清液中蛋白质含量,g;m2表示离心前分散液中蛋白质的含量,g。
1.2.10 乳化性和乳化稳定性的测定
使用Jamdar等[21]的方法稍作修改测定乳化活性指数(EAI)和乳化稳定性指数(ESI)。将7S和11S样品溶液稀释至蛋白浓度为2 mg/mL,然后与大豆油以3:1(v/v)混合后在20000 r/min下均质2 min。分别在刚结束均质时和均质后10 min从容器底部吸取乳液(50 μL),然后用0.1%的SDS溶液(0.01 mol/L,pH7.0的PBS制备)将乳液稀释至5 mL,混匀后用紫外-可见分光光度计在500 nm处测定吸光度,读取吸光值。EAI和ESI根据如下公式(2)和(3)进行计算:
EAI(m2/g)=2×2.303×A0×DF10000×θ×φ×C (2) ESI(min)=A0A0−A10×10 (3) 式中:DF表示稀释倍数(100);A0表示刚结束均质时乳液的吸光度;A10表示均质后10 min时乳液的吸光度;φ表示比色皿的光程(1 cm);θ表示油相体积分数(0.25);C表示蛋白质的初始浓度,g/mL。
1.2.11 冷冻扫描电子显微镜的表征
根据Whitby等[22]的方法,使用冷冻扫描电子显微镜观察形态。将7S和11S蛋白溶液滴入位于支架上的冷冻扫描电子显微镜短管中,并在氮气中进行冷冻。然后,将短管转移到超真空低温室中,在−95 °C下切割并蚀刻60 s,切割后的切面涂上铂金,转移到扫描电镜的冷冻室内(−170 °C)。用显微镜控制软件拍摄超声处理前后的7S和11S的显微图像。
1.3 数据处理
本研究结果以3次平行的实验数据均值±标准差的方式表示。每组数据重复3次,利用SPSS 25.0软件进行单因素方差分析(ANOVA)和Duncan检验(P<0.05)作为事后检验,以比较3组实验数据是否具有显著性差异。
2. 结果与分析
2.1 7S和11S的SDS-PAGE
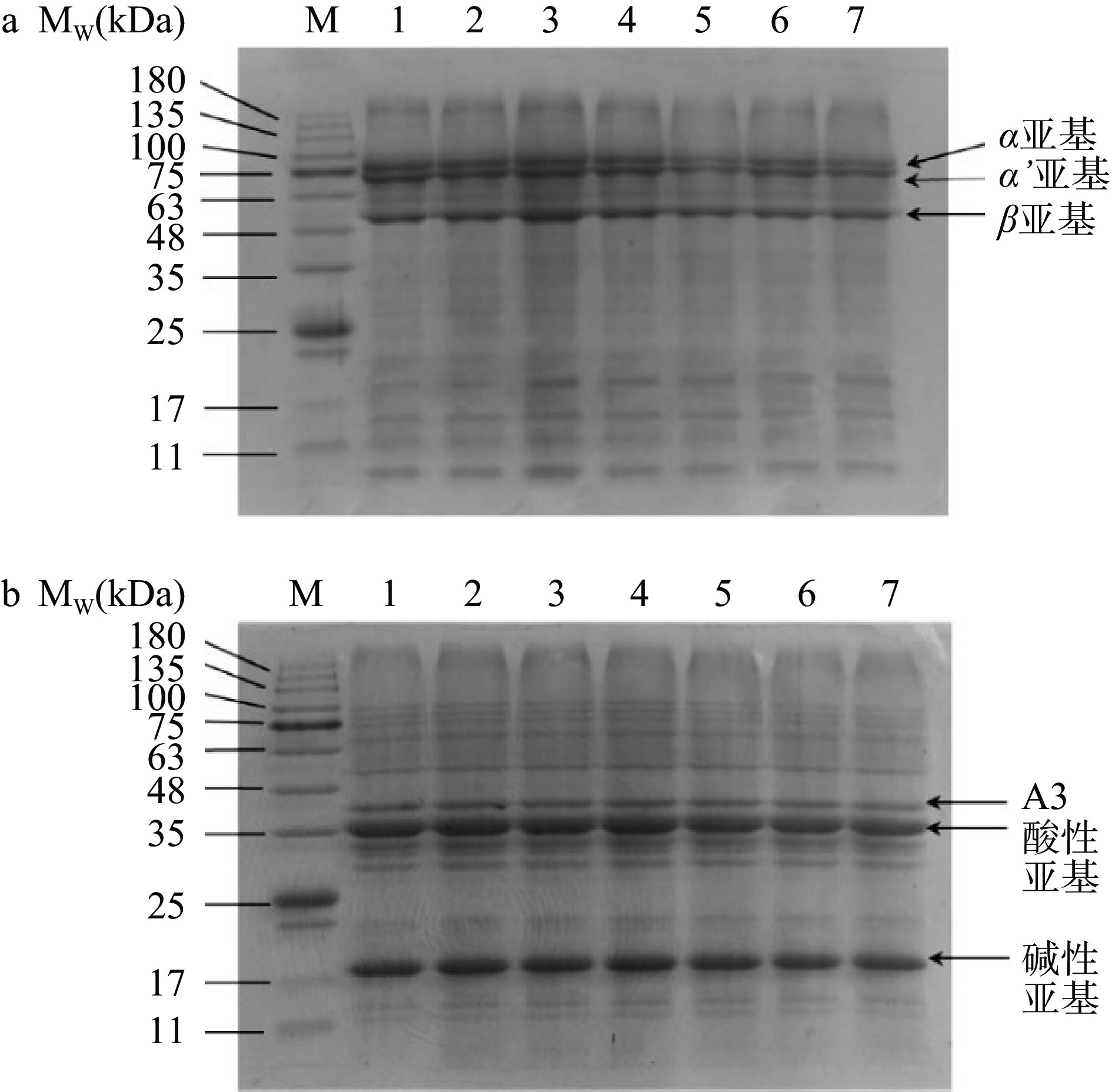
经超声处理和未经超声处理的7S和11S SDS-PAGE图谱如图1,可以清楚地表明本实验提取出的7S和11S的分子量,其中7S在约67、71和50 kDa处有条带,而11S在约35和22 kDa处有条带,这与过去报道的中的亚基分子量大致相同[23]。然而,超声处理并没有改变这两种蛋白质的分子量,这一点从SDS-PAGE图像中相似的条带上可以看出。这说明超声处理没有改变蛋白质的主要结构。同样,O'sullivan等[24]也报道了在超声处理后豌豆蛋白的分子量几乎没有变化。超声处理后蛋白质的分子量几乎不变,说明超声处理可能不会破坏共价键,也就是说蛋白质分子的一级结构没有改变[25]。
2.2 7S和11S红外光谱分析
傅立叶变换红外光谱(FTIR)是测定蛋白质二级结构的常用技术[26]。在蛋白质的二级结构中,α-螺旋结构主要通过多肽中CO和NH基团之间的氢键来稳定。每4个氨基酸形成的α-螺旋结构是非常稳定的,因为,每一个氨基酸,其-CO-NH-基团都会参与形成两个氢键。β-折叠结构,无论是平行还是反平行,都是通过氢键来稳定的。无规则卷曲则可以赋予蛋白质极大的灵活性,这对蛋白质的功能性质来说是必不可少的。
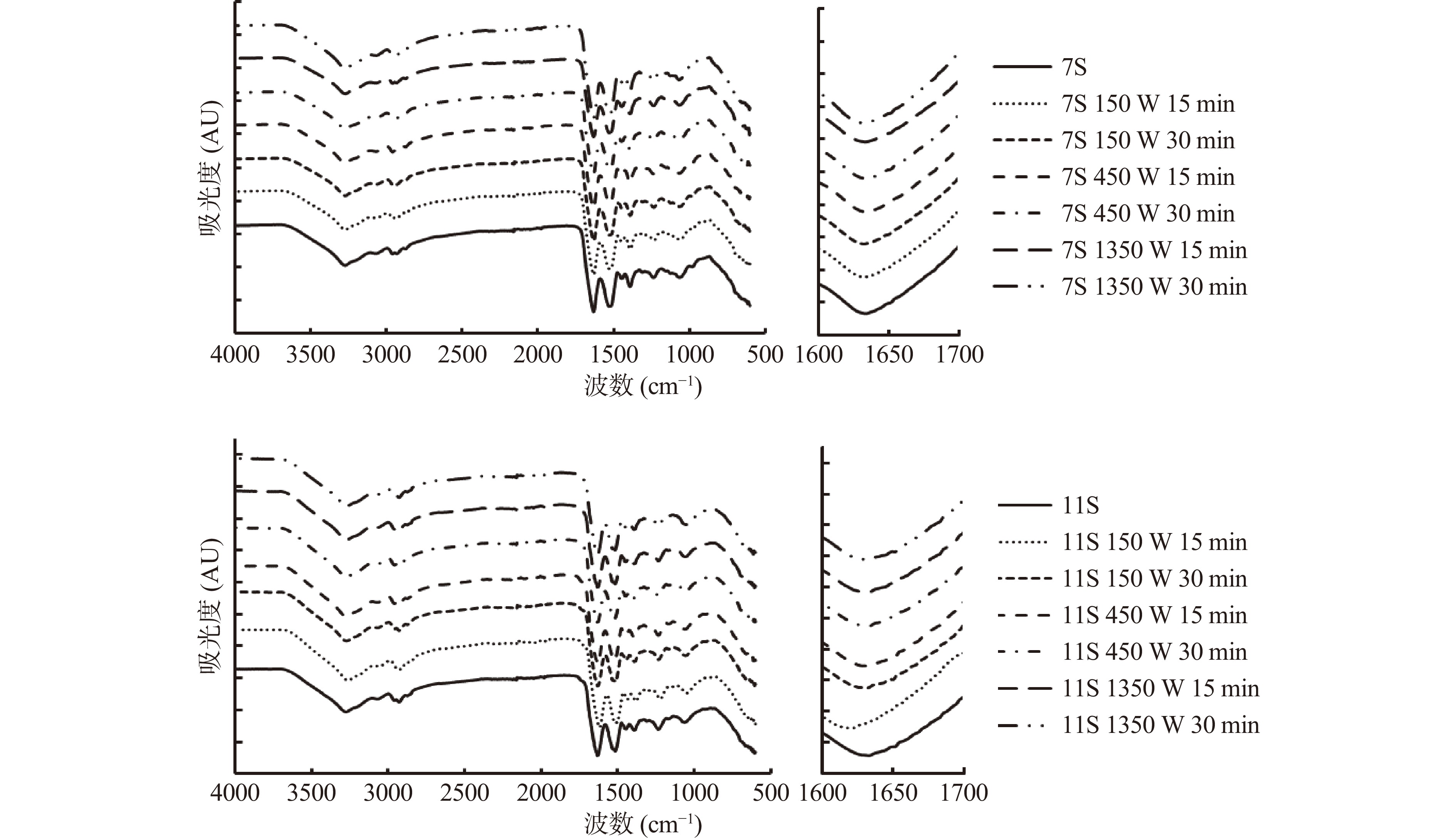
酰胺I带(1700~1600 cm−1的光谱区域)揭示了多肽结构的振荡与蛋白质连接的C=O键的拉伸振动有关[27]。振荡使得酰胺I带对蛋白质二级结构的改变很敏感,因此酰胺I带也被称为蛋白质二级结构的指纹[28-29]。通过将光谱的酰胺I带(图2)进行去卷积来预测二级结构的百分比。从表1中可以看出,超声处理对7S和11S的二级结构有显著影响(P<0.05)。超声处理使7S的β-折叠展开,同时形成α-螺旋、β-转角和无规则卷曲。经不同超声时间和功率条件处理的7S各结构含量差别较小,尤其是无规则卷曲的含量,各样品之间差异不显著(P>0.05)。与未处理组,11S蛋白的二级结构中α-螺旋、β-转角和无规则卷曲的含量略有减少,而β-折叠的含量在超声条件为1350 W、30 min时增加了5.95%。β-折叠一般埋藏在多肽链内部[30],因此β-折叠的减少说明超声处理改变了蛋白的空间构象,导致蛋白质结构松散。无规则卷曲含量的增加进一步证实了超声处理过程中形成了更多无序的分子结构。结构含量的变化可能是由于超声处理诱导了氢键的变化,导致11S的疏水区域暴露度进一步增强[31]。在以往的研究中,Zou等[32]报道,随着超声处理时间的延长,贻贝肌浆蛋白的α-螺旋的含量降低(从36.9%到29.2%),β-折叠含量增加了6.2%。Wang等[33]则报道了超声处理使α-螺旋结构和β-折叠含量减少。这些研究同样表明,超声处理可以破坏蛋白质分子中的氢键等分子间相互作用,从而削弱蛋白质的刚性结构,导致二级结构的变化[34]。
表 1 7S和11S的二级结构含量Table 1. Secondary structure contents of 7S and 11S样品 超声条件 α-螺旋(%) β-折叠(%) β-转角(%) 无规则卷曲(%) 7S − 17.79±0.04c 47.91±0.56a 12.57±0.34c 21.73±0.34b 7S 150 W,15 min 20.54±0.32b 41.17±0.21bc 15.36±1.21b 22.51±0.82a 7S 150 W,30 min 20.32±0.07b 42.74±0.15b 16.20±0.68ab 22.92±0.97a 7S 450 W,15 min 20.47±0.36b 40.45±0.03c 15.24±0.77b 23.84±0.91a 7S 450 W,30 min 21.07±0.09a 40.73±0.09c 15.46±0.15b 22.74±0.46a 7S 1350 W,15 min 21.98±0.11a 39.17±0.29d 17.37±0.44a 23.48±0.32a 7S 1350 W,30 min 21.26±0.73a 38.74±0.64d 17.75±0.41a 22.25±0.75a 11S − 19.90±0.58a 42.29±0.11b 15.29±0.06a 22.51±0.90a 11S 150 W,15 min 18.03±0.01b 47.66±0.05a 12.45±0.12b 20.86±0.08b 11S 150 W,30 min 17.98±0.13b 47.32±0.06a 12.85±0.10b 20.78±0.24b 11S 450 W,15 min 17.77±1.04b 48.19±0.16a 12.38±1.55b 21.26±0.94b 11S 450 W,30 min 17.72±0.54b 47.73±0.05a 12.46±0.47b 21.24±0.29b 11S 1350 W,15 min 17.98±0.05b 48.17±0.31a 12.36±0.40b 21.38±0.42b 11S 1350 W,30 min 17.64±0.22b 48.24±0.62a 12.17±0.45b 21.94±0.72ab 注:所有样品测定3次取平均值,−表示未处理,同一列中单一样品之间字母不同表示有显著性差异(P<0.05)。 2.3 7S和11S内源荧光光谱分析
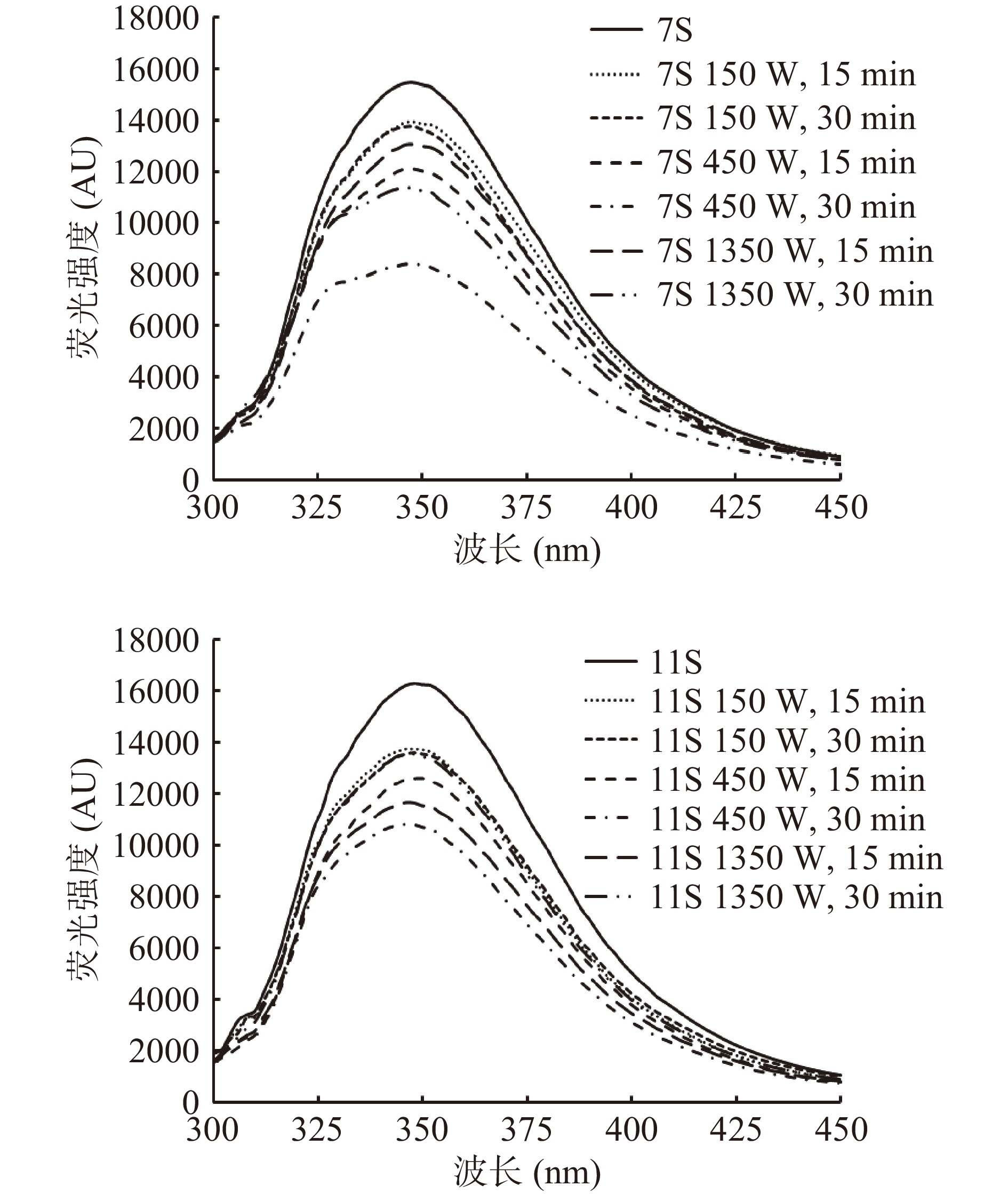
蛋白质中的色氨酸(Trp)和酪氨酸(Tyr),尤其是Trp残基,与蛋白质的折叠状态密切相关,可以用来描述蛋白质三级结构的变化[5]。而Trp和Tyr基团周围的局部分子环境变化可以通过蛋白的荧光光谱反映出来[35]。图3展示了7S和11S在进行和未进行超声处理时的内源荧光光谱,可以看出7S和11S的荧光发射峰的最大吸收波长(λmax)分别在348 nm和352 nm处,并且在超声处理后保持不变。但未进行超声处理的7S和11S的荧光强度均为最高,而超声处理后所有样品的荧光强度均有不同程度的下降。具体来说,随着超声功率的增大,荧光强度呈现先减小后增大的趋势,且在超声条件为450 W、30 min 时7S和11S荧光强度降低幅度最大,分别高达12.65%和6.82%。超声处理后荧光强度的降低与Wen等[36]的报道结果一致。荧光强度降低的可能原因是本实验相对于其他报道中使用了更高的超声强度,在极端的超声强度下,蛋白质分子暴露的发色团被淬灭,从而降低了荧光强度[37]。此外,超声处理会导致更多的发色团被埋没,变得无法检测,这也可能是荧光强度降低的原因之一[5]。但当超声功率为1350 W 时,超声促使蛋白中部分被掩埋的发色基团重新暴露,形成了一个反复的过程,这使得荧光强度又重新有所升高,但仍低于未经过超声处理的样品。这种超声处理后荧光强度降低但λmax不变的结果表明,超声处理对Trp和Tyr等发色团周围的极性微环境影响较小,但会影响发色团的暴露,导致蛋白质的三级结构发生一些变化[38]。
2.4 7S和11S粒径分布分析
蛋白质的聚集程度可以通过测量颗粒的大小来表示[39]。如图4所示,未经过超声处理的7S和11S的粒径分布均呈现双峰,且峰差明显。7S的峰值强度分别位于43.8和225 nm处,11S的峰值强度分别位于37.8和220 nm处。出现这种分布,第一个峰可能是由于低聚物或单体的存在,第二个峰则是由于较大的聚集物所致[40]。超声处理后,7S和11S的粒径分布均向小颗粒方向移动,且蛋白质的粒径分布范围缩小。对于7S,在以450 W持续超声处理30 min时,粒径减小最为明显;而对于11S,在1350 W的功率下持续超声处理30 min时,粒径减小最为明显。超声处理后蛋白质粒径的减小可能是由于超声空化和声流的综合效应,它们提高了蛋白质颗粒的碰撞速度和强度,导致大的蛋白质聚集体被分解成更小的碎片,同时降低了蛋白质颗粒的粒径[41-42]。随着粒径的减小,蛋白质和水分子之间接触的表面积增加,这可能会导致蛋白质与水的相互作用增强,进而增加溶解度。多项研究表明,超声处理可以减小蛋白质的粒径。Arredondo-Parada等[43]对巨鱿地幔的蛋白浓缩物进行超声处理后,发现功率为38 W的超声处理比22 W处理更能降低蛋白的粒径。然而,与本文结果相反,Gülseren等报道[44],当超声处理时间超过40 min时,牛血清白蛋白的平均粒径随着超声处理时间的延长而增加,这种现象的可能原因是过长的超声处理时间反而促进了蛋白质聚集。
2.5 7S和11S表面疏水性分析
蛋白质的表面疏水性(H0)可以用于评价蛋白质受构象变化影响导致的功能特性变化[45]。它衡量蛋白质中暴露的疏水氨基酸残基的数量,同时也表现蛋白质亲水/疏水基团之间的平衡,反映了蛋白质的展开程度[46]。7S和11S的表面疏水性如图5所示。从图中可以看出,随着超声强度和时间的增加,样品的H0逐渐增大。超声处理后的7S和11S的H0均显著高于对照样品(P<0.05)。当超声处理条件为1350 W,持续30 min时,7S的H0从16299增加到64608,11S的H0在此条件下也是最高的,比未进行超声处理的11S增加了约157%。此外,在同样的超声处理条件下,11S的疏水性始终高于7S。Zhang等[47]也发现,超声处理后,鸡胸肉中肌纤维蛋白的H0增强。对这一现象的一种可能的解释是,超声处理过程中不同空化水平引起的湍流、剪切和微流体效应导致了蛋白质结构的扰动,促进了蛋白质侧链的部分展开[48]。这种展开导致之前被阻断的疏水基团的暴露,进一步导致了探针与之前被阻断的疏水位点结合时,H0增加[49]。
2.6 7S和11S差示扫描量热法分析
DSC是一种研究蛋白质热变性和热力学性质的通用方法,因为它可以显示超声后不同处理条件导致的蛋白质自然结构损伤的空间变化[50]。图6显示了经过超声处理和未经过超声处理的7S和11S的DSC图,所有样品都观察到了吸热曲线。同时分析了变性温度(T峰)以及焓值来评估7S和11S的变性程度。由表2中数据可以看出,未经超声处理的7S和11S的变性温度分别为77.29和93.93 °C,这与之前的研究结果基本一致[51]。超声处理后,蛋白质的焓值(ΔH)与对照组相比均出现了减小。一般来说,ΔH与诱导构象变化所需的能量有关,而T峰则反映了蛋白质结构的稳定性[20]。在6种超声处理条件下,7S的ΔH由1.22 J/g最多下降到0.17 J/g,11S的ΔH由1.41 J/g最多下降到0.53 J/g。超声处理后的7S和11S需要较少的能量来展开蛋白质结构,反映出蛋白原有的空间结构结构被超声所破坏,从而降低了蛋白质变性所需的能量[52]。而7S和11S之间ΔH变化程度的差异可能是由于11S的结构更为致密,二硫键更多更稳定。因此,11S受超声处理的影响比缺乏二硫键的7S小。这种稳定性的差异也可以通过2.3所述的超声处理后荧光强度下降的程度反映出来。另外,观察到T峰位置随超声处理而变化,但变化不明显。T峰与蛋白质结构有关,所以T峰的轻微变化是由于超声处理后7S和11S的结构变化造成的[33],而这种结构变化可能是由于蛋白质中疏水键的改变。Mir等[53]也报道了藜麦种子分离蛋白的类似结果。超声处理25 min后,藜麦种子蛋白的ΔH从46.78 J/g下降到38.75 J/g。
表 2 超声处理后的7S和11S的DSC分析Table 2. Analysis of DSC of 7S and 11S with and without sonication样品 超声条件 变性温度(°C) ΔH(J/g) 7S − 77.29 1.22 7S 150 W,15 min 76.34 0.77 7S 150 W,30 min 76.98 0.86 7S 450 W,15 min 77.05 0.28 7S 450 W,30 min 78.53 0.56 7S 1350 W,15 min 77.79 0.17 7S 1350 W,30 min 77.65 0.20 11S − 93.93 1.41 11S 150 W,15 min 95.12 0.94 11S 150 W,30 min 94.34 0.91 11S 450 W,15 min 94.93 0.97 11S 450 W,30 min 94.53 0.86 11S 1350 W,15 min 94.19 0.53 11S 1350 W,30 min 95.03 1.02 2.7 7S和11S溶解度分析
由于溶解度是一种影响蛋白质功能特性的重要性质,本文测定了7S和11S在超声处理后和未经过超声处理时的溶解度。如图7所示,与未经超声处理的7S相比,所有超声处理后的7S的溶解度均显著增加(P<0.05)。在6种不同的处理条件下,7S的溶解度分别增加了3.14%、4.30%、6.18%、3.08%、9.32%和12.85%。在超声处理条件为450 W、30 min时,7S的溶解度增加最少。11S表现出与7S相似的变化规律,超声处理使其溶解度最高增加10.57%。但当强度和时间分别为1350 W和15 min时,11S的溶解度没有明显改善(P>0.05)。
在自然状态下,蛋白质以聚集的形式存在。而超声处理破坏了蛋白质的分子内键,使肽链变得疏松,促进了可溶性蛋白质聚合体或单体的形成[54]。此时蛋白质与水分子结合的能力增强,从而提高其溶解度。Jiang等[55]也提出,蛋白质分子与一些较小颗粒解聚形成亚单位的过程是溶解度提高的有效驱动力。蛋白质溶解度增强的另一个可能原因是超声处理在蛋白质表面制造了高速的声波流动,导致蛋白质表面活性增加,亲水性增强[56]。然而,随着超声功率的持续增加及时间的延长,7S和11S的溶解度又出现了一定程度的下降。这一现象可能是因为蛋白质分子进一步展开和膨胀,暴露出了更多的疏水基团和巯基[33]。这些结果表明,超声处理对蛋白质的影响是一个反复的过程,其效果可能因蛋白质和超声处理条件的不同而不同。
2.8 7S和11S的乳化性及乳化稳定性
乳化性能表示蛋白质单位重量稳定的界面面积,表征蛋白质对油水界面的吸附能力[57]。超声处理对7S和11S的乳化性能(EAI和ESI)的影响如图8所示。两种蛋白经超声处理后,EAI均显著高于对照组样品(P<0.05)。7S超声处理条件为1350 W,30 min时,EAI增加80.55%,11S超声处理条件为450 W,30 min时,EAI增加48.96%。而当超声处理条件为1350 W时,11S的EAI有所下降,但仍高于未经超声处理的样品。7S和11S的ESI与EAI的变化趋势相似,超声处理后均显著升高(P<0.05)。这一发现与已发表的几项研究一致,这些研究报道了超声处理过的乳清蛋白[15]、小麦谷蛋白[58]的EAI和ESI都有显著(P<0.05)的改善。超声处理减小了7S和11S的颗粒大小,部分展开了7S和11S的结构。更无序的结构增加了蛋白质在油水界面的吸附倾向[20],从而提高了7S和11S的EAI。此外,更高的溶解度也加速了蛋白质在界面上的扩散。ESI与蛋白质的高疏水性之间有很强的正相关性[59]。表面疏水性的增加增强了界面蛋白之间的疏水性相互作用,从而提高了ESI。
2.9 7S和11S冷冻电镜表征
为了进一步观察不同超声处理条件对7S和11S结构的影响,拍摄了如图9所示的蛋白质溶液冷冻电镜照片。图中可以很明显地观察到7S和11S在经过和未经过超声处理时的不同图像。对于7S,随着超声强度和时间的增加,可以观察到蛋白质结构从有序的致密网状结构(A~G)逐渐发生变化。当样品在150 W的强度下超声处理30 min时,7S结构已经变得疏松(C)。当超声处理条件为1350 W,持续30 min时,蛋白质表面更粗糙,更不规则(G)。而没有经过超声处理的11S则以有序、分散的结构存在(H)。在450 W的功率下,超声处理后的11S微观结构长度比对照组变短(K、L)。在超声功率为1350 W的处理下,11S显现出更多的无序结构和许多不规则的孔隙(M、N)。7S和11S发生这些变化可能是因为超声处理破坏了蛋白质分子之间的交联[60]。这使得分子结构随着蛋白质的空间构象的变化而展开[29]。这些结果与超声处理下蛋白质颗粒大小的变化是一致的,并为超声处理导致蛋白质团聚体破坏的假说增加了证据。
![]() 图 9 超声处理前后7S(A~G)和11S(H~N)冷冻电镜分析注:A~G和H~N分别代表7S和11S的7组超声条件不同的样品,即:对照组,150 W&15 min、 150 W&30 min、450 W&15 min, 450 W&30 min、1350 W&15 min、 1350 W&30 min。Figure 9. Cryo-scanning electron microscopy analysis of 7S (A-G) and 11S (H-N) with and without sonication
图 9 超声处理前后7S(A~G)和11S(H~N)冷冻电镜分析注:A~G和H~N分别代表7S和11S的7组超声条件不同的样品,即:对照组,150 W&15 min、 150 W&30 min、450 W&15 min, 450 W&30 min、1350 W&15 min、 1350 W&30 min。Figure 9. Cryo-scanning electron microscopy analysis of 7S (A-G) and 11S (H-N) with and without sonication3. 结论
超声处理不改变7S和11S的分子量,但可以破坏蛋白质分子中的氢键等分子间相互作用,削弱蛋白质的刚性结构,导致二级结构的变化。超声处理使蛋白质分子暴露的生色团淬灭,样品的荧光强度下降。经超声处理后,7S和11S样品焓值下降,展开蛋白质结构所需的能量变少。超声处理提高了7S和11S的表面疏水性、溶解性和乳化性,减小了平均粒径,且粒径分布范围缩小,7S和11S从较为有序的网状聚集状态转变为无序的状态。
以上结果表明超声处理能一定程度地调控7S和11S的空间结构,进而改善其理化特性。本研究为超声处理7S和11S对蛋白结构和理化性质产生的影响提供了部分参考,使超声改性蛋白的合理应用有一定的理论依据。
-
图 9 超声处理前后7S(A~G)和11S(H~N)冷冻电镜分析
注:A~G和H~N分别代表7S和11S的7组超声条件不同的样品,即:对照组,150 W&15 min、 150 W&30 min、450 W&15 min, 450 W&30 min、1350 W&15 min、 1350 W&30 min。
Figure 9. Cryo-scanning electron microscopy analysis of 7S (A-G) and 11S (H-N) with and without sonication
表 1 7S和11S的二级结构含量
Table 1 Secondary structure contents of 7S and 11S
样品 超声条件 α-螺旋(%) β-折叠(%) β-转角(%) 无规则卷曲(%) 7S − 17.79±0.04c 47.91±0.56a 12.57±0.34c 21.73±0.34b 7S 150 W,15 min 20.54±0.32b 41.17±0.21bc 15.36±1.21b 22.51±0.82a 7S 150 W,30 min 20.32±0.07b 42.74±0.15b 16.20±0.68ab 22.92±0.97a 7S 450 W,15 min 20.47±0.36b 40.45±0.03c 15.24±0.77b 23.84±0.91a 7S 450 W,30 min 21.07±0.09a 40.73±0.09c 15.46±0.15b 22.74±0.46a 7S 1350 W,15 min 21.98±0.11a 39.17±0.29d 17.37±0.44a 23.48±0.32a 7S 1350 W,30 min 21.26±0.73a 38.74±0.64d 17.75±0.41a 22.25±0.75a 11S − 19.90±0.58a 42.29±0.11b 15.29±0.06a 22.51±0.90a 11S 150 W,15 min 18.03±0.01b 47.66±0.05a 12.45±0.12b 20.86±0.08b 11S 150 W,30 min 17.98±0.13b 47.32±0.06a 12.85±0.10b 20.78±0.24b 11S 450 W,15 min 17.77±1.04b 48.19±0.16a 12.38±1.55b 21.26±0.94b 11S 450 W,30 min 17.72±0.54b 47.73±0.05a 12.46±0.47b 21.24±0.29b 11S 1350 W,15 min 17.98±0.05b 48.17±0.31a 12.36±0.40b 21.38±0.42b 11S 1350 W,30 min 17.64±0.22b 48.24±0.62a 12.17±0.45b 21.94±0.72ab 注:所有样品测定3次取平均值,−表示未处理,同一列中单一样品之间字母不同表示有显著性差异(P<0.05)。 表 2 超声处理后的7S和11S的DSC分析
Table 2 Analysis of DSC of 7S and 11S with and without sonication
样品 超声条件 变性温度(°C) ΔH(J/g) 7S − 77.29 1.22 7S 150 W,15 min 76.34 0.77 7S 150 W,30 min 76.98 0.86 7S 450 W,15 min 77.05 0.28 7S 450 W,30 min 78.53 0.56 7S 1350 W,15 min 77.79 0.17 7S 1350 W,30 min 77.65 0.20 11S − 93.93 1.41 11S 150 W,15 min 95.12 0.94 11S 150 W,30 min 94.34 0.91 11S 450 W,15 min 94.93 0.97 11S 450 W,30 min 94.53 0.86 11S 1350 W,15 min 94.19 0.53 11S 1350 W,30 min 95.03 1.02 -
[1] HUANG L R, DING X N, Li Y L, et al. The aggregation, structures and emulsifying properties of soybean protein isolate induced by ultrasound and acid[J]. Food Chemistry,2019,279:114−119. doi: 10.1016/j.foodchem.2018.11.147
[2] MARUYAMA N, ADACHI M, TAKAHASHI K, et al. Crystal structures of recombinant and native soybean β-conglycinin β homotrimers[J]. European Journal of Biochemistry,2001,268(12):3595−3604. doi: 10.1046/j.1432-1327.2001.02268.x
[3] KITAMURA K, SHIBASAKI K. Isolation and some physico-chemical properties of the acidic subunits of soybean 11S globulin[J]. Agricultural and Biological Chemistry,1975,39(5):945−951.
[4] JIANG J, CHEN J, XIONG Y L. Structural and emulsifying properties of soy protein isolate subjected to acid and alkaline pH-shifting processes[J]. Journal of Agricultural and Food Chemistry,2009,57(16):7576−7583. doi: 10.1021/jf901585n
[5] SUN X Y, ZHANG W, ZHANG L F, et al. Effect of ultrasound‐assisted extraction on the structure and emulsifying properties of peanut protein isolate[J]. Journal of the Science of Food and Agriculture,2021,101(3):1150−1160. doi: 10.1002/jsfa.10726
[6] MA X B, YAN T Y, HOU F R, et al. Formation of soy protein isolate (SPI)-citrus pectin (CP) electrostatic complexes under a high-intensity ultrasonic field: Linking the enhanced emulsifying properties to physicochemical and structural properties[J]. Ultrasonics sonochemistry,2019,59:104748. doi: 10.1016/j.ultsonch.2019.104748
[7] MCCLEMENTS D J. Advances in the application of ultrasound in food analysis and processing[J]. Trends in Food Science & Technology,1995,6(9):293−299.
[8] FAN X J, LI S, ZHANG A, et al. Mechanism of change of the physicochemical characteristics, gelation process, water state, and microstructure of okara tofu analogues induced by high-intensity ultrasound treatment[J]. Food Hydrocolloids,2021,111:106241. doi: 10.1016/j.foodhyd.2020.106241
[9] O’SULLIVAN J J, PARK M, BEEVERS J, et al. Applications of ultrasound for the functional modification of proteins and nanoemulsion formation: A review[J]. Food Hydrocolloids,2017,71:299−310. doi: 10.1016/j.foodhyd.2016.12.037
[10] MORALES R, MARTÍNEZ K D, RUIZ-HENESTROSA V M P, et al. Modification of foaming properties of soy protein isolate by high ultrasound intensity: Particle size effect[J]. Ultrasonics Sonochemistry,2015,26:48−55. doi: 10.1016/j.ultsonch.2015.01.011
[11] ZHENG T, LI X H, TAHA A, et al. Effect of high intensity ultrasound on the structure and physicochemical properties of soy protein isolates produced by different denaturation methods[J]. Food Hydrocolloids,2019,97:105216. doi: 10.1016/j.foodhyd.2019.105216
[12] MATSUMURA Y, SIRISON J, ISHI T, et al. Soybean lipophilic proteins-Origin and functional properties as affected by interaction with storage proteins[J]. Current Opinion in Colloid & Interface Science,2017,28:120−128.
[13] JUNG S, RICKERT D, DEAK N, et al. Comparison of Kjeldahl and Dumas methods for determining protein contents of soybean products[J]. Journal of the American Oil Chemists' Society,2003,80(12):1169. doi: 10.1007/s11746-003-0837-3
[14] MARGULIS M, MARGULIS I. Calorimetric method for measurement of acoustic power absorbed in a volume of a liquid[J]. Ultrasonics Sonochemistry,2003,10(6):343−345. doi: 10.1016/S1350-4177(03)00100-7
[15] WU D, WU C, MA W C, et al. Effects of ultrasound treatment on the physicochemical and emulsifying properties of proteins from scallops (Chlamys farreri)[J]. Food Hydrocolloids,2019,89:707−714. doi: 10.1016/j.foodhyd.2018.11.032
[16] TIAN R, FENG J R, HUANG G, et al. Ultrasound driven conformational and physicochemical changes of soy protein hydrolysates[J]. Ultrasonics Sonochemistry,2020,68:105202. doi: 10.1016/j.ultsonch.2020.105202
[17] KATO A, NAKAI S. Hydrophobicity determined by a fluorescence probe method and its correlation with surface properties of proteins[J]. Biochimica et Biophysica acta (BBA)-Protein Structure,1980,624(1):13−20. doi: 10.1016/0005-2795(80)90220-2
[18] LOWRY O H, ROSEBROUGH N J, FARR A L, et al. Protein measurement with the Folin phenol reagent[J]. Journal of Biological Chemistry,1951,193:265−275. doi: 10.1016/S0021-9258(19)52451-6
[19] REN C, XIONG W F, LI J, et al. Comparison of binding interactions of cyanidin-3-O-glucoside to β-conglycinin and glycinin using multi-spectroscopic and thermodynamic methods[J]. Food Hydrocolloids,2019,92:155−162. doi: 10.1016/j.foodhyd.2019.01.053
[20] NAZARI B, MOHAMMADIFAR M A, SHOJAEE-ALIABADI S, et al. Effect of ultrasound treatments on functional properties and structure of millet protein concentrate[J]. Ultrasonics Sonochemistry,2018,41:382−388. doi: 10.1016/j.ultsonch.2017.10.002
[21] JAMDAR S, HARIKUMAR P. A rapid autolytic method for the preparation of protein hydrolysate from poultry viscera[J]. Bioresource Technology,2008,99(15):6934−6940. doi: 10.1016/j.biortech.2008.01.023
[22] WHITBY C P, FORNASIERO D, RALSTON J. Effect of adding anionic surfactant on the stability of Pickering emulsions[J]. Journal of Colloid and Interface Science,2009,329(1):173−181. doi: 10.1016/j.jcis.2008.09.056
[23] SUI X N, ZHANG T Y, JIANG L Z. Soy protein: Molecular structure revisited and recent advances in processing technologies[J]. Annual Review of Food Science and Technology,2020,12:119−147.
[24] O'SULLIVAN J, MURRAY B, FLYNN C, et al. The effect of ultrasound treatment on the structural, physical and emulsifying properties of animal and vegetable proteins[J]. Food hydrocolloids,2016,53:141−154. doi: 10.1016/j.foodhyd.2015.02.009
[25] O'SULLIVAN J, ARELLANO M, PICHOT R, et al. The effect of ultrasound treatment on the structural, physical and emulsifying properties of dairy proteins[J]. Food Hydrocolloids,2014,42:386−396. doi: 10.1016/j.foodhyd.2014.05.011
[26] JACKSON M, MANTSCH H H. The use and misuse of FTIR spectroscopy in the determination of protein structure[J]. Critical reviews in Biochemistry and Molecular biology,1995,30(2):95−120. doi: 10.3109/10409239509085140
[27] VERA A, VALENZUELA M, YAZDANI-PEDRAM M, et al. Conformational and physicochemical properties of quinoa proteins affected by different conditions of high-intensity ultrasound treatments[J]. Ultrasonics Sonochemistry,2019,51:186−196. doi: 10.1016/j.ultsonch.2018.10.026
[28] ZHAO J, HE J, DANG Y L, et al. Ultrasound treatment on the structure of goose liver proteins and antioxidant activities of its enzymatic hydrolysate[J]. Journal of Food Biochemistry,2020,44(1):e13091.
[29] XU B, YUAN J, WANG L, et al. Effect of multi-frequency power ultrasound (MFPU) treatment on enzyme hydrolysis of casein[J]. Ultrasonics Sonochemistry,2020,63:104930. doi: 10.1016/j.ultsonch.2019.104930
[30] MA X B, HOU F R, ZHAO H H, et al. Conjugation of soy protein isolate (SPI) with pectin by ultrasound treatment[J]. Food Hydrocolloids,2020,108:106056. doi: 10.1016/j.foodhyd.2020.106056
[31] LI K, FU L, ZHAO Y Y, et al. Use of high-intensity ultrasound to improve emulsifying properties of chicken myofibrillar protein and enhance the rheological properties and stability of the emulsion[J]. Food Hydrocolloids,2020,98:105275. doi: 10.1016/j.foodhyd.2019.105275
[32] ZOU H N, ZHAO N, SUN S, et al. High-intensity ultrasonication treatment improved physicochemical and functional properties of mussel sarcoplasmic proteins and enhanced the stability of oil-in-water emulsion[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects,2020,589:124463. doi: 10.1016/j.colsurfa.2020.124463
[33] WANG J Y, YANG Y L, TANG X Z, et al. Effects of pulsed ultrasound on rheological and structural properties of chicken myofibrillar protein[J]. Ultrasonics Sonochemistry,2017,38:225−233. doi: 10.1016/j.ultsonch.2017.03.018
[34] WANG F, ZHANG Y Z, XU L, et al. An efficient ultrasound-assisted extraction method of pea protein and its effect on protein functional properties and biological activities[J]. LWT,2020,127:109348. doi: 10.1016/j.lwt.2020.109348
[35] XIONG W F, WANG Y T, ZHANG C L, et al. High intensity ultrasound modified ovalbumin: Structure, interface and gelation properties[J]. Ultrasonics Sonochemistry,2016,31:302−309. doi: 10.1016/j.ultsonch.2016.01.014
[36] WEN Q H, TU Z C, ZHANG L, et al. Effect of high intensity ultrasound on the gel and structural properties of Ctenopharyngodon idellus myofibrillar protein[J]. Journal of Food Biochemistry,2017,41(1):e12288. doi: 10.1111/jfbc.12288
[37] LI Y H, CHENG Y, ZHANG Z L, et al. Modification of rapeseed protein by ultrasound-assisted pH shift treatment: Ultrasonic mode and frequency screening, changes in protein solubility and structural characteristics[J]. Ultrasonics Sonochemistry,2020,69:105240. doi: 10.1016/j.ultsonch.2020.105240
[38] ZHANG M C, LI F F, DIAO X P, et al. Moisture migration, microstructure damage and protein structure changes in porcine longissimus muscle as influenced by multiple freeze-thaw cycles[J]. Meat Science,2017,133:10−18. doi: 10.1016/j.meatsci.2017.05.019
[39] CAI L, ZHANG W D, CAO A L, et al. Effects of ultrasonics combined with far infrared or microwave thawing on protein denaturation and moisture migration of Sciaenops ocellatus (red drum)[J]. Ultrasonics Sonochemistry,2019,55:96−104. doi: 10.1016/j.ultsonch.2019.03.017
[40] LI Z Y, WANG J Y, ZHENG B D, et al. Impact of combined ultrasound-microwave treatment on structural and functional properties of golden threadfin bream (Nemipterus virgatus) myofibrillar proteins and hydrolysates[J]. Ultrasonics Sonochemistry,2020,65:105063. doi: 10.1016/j.ultsonch.2020.105063
[41] KHATKAR A B, KAUR A, KHATKAR S K, et al. Characterization of heat-stable whey protein: Impact of ultrasound on rheological, thermal, structural and morphological properties[J]. Ultrasonics Sonochemistry,2018,49:333−342. doi: 10.1016/j.ultsonch.2018.08.026
[42] LIU R, LIU Q, XIONG S B, et al. Effects of high intensity unltrasound on structural and physicochemical properties of myosin from silver carp[J]. Ultrasonics Sonochemistry,2017,37:150−157. doi: 10.1016/j.ultsonch.2016.12.039
[43] ARREDONDO-PARADA I, TORRES-ARREOLA W, SUÁREZ-JIMÉNEZ G M, et al. Effect of ultrasound on physicochemical and foaming properties of a protein concentrate from giant squid (Dosidicus gigas) mantle[J]. LWT,2020,121:108954. doi: 10.1016/j.lwt.2019.108954
[44] GÜLSEREN İ, GÜZEY D, BRUCE B D, et al. Structural and functional changes in ultrasonicated bovine serum albumin solutions[J]. Ultrasonics Sonochemistry,2007,14(2):173−183. doi: 10.1016/j.ultsonch.2005.07.006
[45] PAN M M, XU F R, WU Y, et al. Application of ultrasound-assisted physical mixing treatment improves in vitro protein digestibility of rapeseed napin[J]. Ultrasonics Sonochemistry,2020,67:105136. doi: 10.1016/j.ultsonch.2020.105136
[46] ZHANG Z L, WANG Y, JIANG H, et al. Effect of dual-frequency ultrasound on the formation of lysinoalanine and structural characterization of rice dreg protein isolates[J]. Ultrasonics Sonochemistry,2020,67:105124. doi: 10.1016/j.ultsonch.2020.105124
[47] ZHANG C, LI X A, WANG H, et al. Ultrasound-assisted immersion freezing reduces the structure and gel property deterioration of myofibrillar protein from chicken breast[J]. Ultrasonics Sonochemistry,2020,67:105137. doi: 10.1016/j.ultsonch.2020.105137
[48] DABBOUR M, HE R, MINTAH B, et al. Changes in functionalities, conformational characteristics and antioxidative capacities of sunflower protein by controlled enzymolysis and ultrasonication action[J]. Ultrasonics Sonochemistry,2019,58:104625. doi: 10.1016/j.ultsonch.2019.104625
[49] DE FIGUEIREDO FURTADO G, MANTOVANI R A, CONSOLI L, et al. Structural and emulsifying properties of sodium caseinate and lactoferrin influenced by ultrasound process[J]. Food Hydrocolloids,2017,63:178−188. doi: 10.1016/j.foodhyd.2016.08.038
[50] ZOU Y, XU P P, WU H H, et al. Effects of different ultrasound power on physicochemical property and functional performance of chicken actomyosin[J]. International Journal of Biological Macromolecules,2018,113:640−647. doi: 10.1016/j.ijbiomac.2018.02.039
[51] SOBRAL P A, PALAZOLO G G, WAGNER J R. Thermal behavior of soy protein fractions depending on their preparation methods, individual interactions, and storage conditions[J]. Journal of Agricultural and Food Chemistry,2010,58(18):10092−10100. doi: 10.1021/jf101957f
[52] SUN Q X, CHEN Q, XIA X F, et al. Effects of ultrasound-assisted freezing at different power levels on the structure and thermal stability of common carp (Cyprinus carpio) proteins[J]. Ultrasonics Sonochemistry,2019,54:311−320. doi: 10.1016/j.ultsonch.2019.01.026
[53] MIR N A, RIAR C S, SINGH S. Physicochemical, molecular and thermal properties of high-intensity ultrasound (HIUS) treated protein isolates from album (Chenopodium album) seed[J]. Food Hydrocolloids,2019,96:433−441. doi: 10.1016/j.foodhyd.2019.05.052
[54] ARZENI C, MARTÍNEZ K, ZEMA P, et al. Comparative study of high intensity ultrasound effects on food proteins functionality[J]. Journal of Food Engineering,2012,108(3):463−472. doi: 10.1016/j.jfoodeng.2011.08.018
[55] JIANG S S, DING J Z, ANDRADE J, et al. Modifying the physicochemical properties of pea protein by pH-shifting and ultrasound combined treatments[J]. Ultrasonics Sonochemistry,2017,38:835−842. doi: 10.1016/j.ultsonch.2017.03.046
[56] O’DONNELL C, TIWARI B, BOURKE P, et al. Effect of ultrasonic processing on food enzymes of industrial importance[J]. Trends in Food Science & Technology,2010,21(7):358−367.
[57] SUI X N, BI S, QI B K, et al. Impact of ultrasonic treatment on an emulsion system stabilized with soybean protein isolate and lecithin: Its emulsifying property and emulsion stability[J]. Food Hydrocolloids,2017,63:727−734. doi: 10.1016/j.foodhyd.2016.10.024
[58] ZHANG H, CLAVER I P, ZHU K X, et al. The effect of ultrasound on the functional properties of wheat gluten[J]. Molecules,2011,16(5):4231−4240. doi: 10.3390/molecules16054231
[59] BA F, URSU A V, LAROCHE C, et al. Haematococcus pluvialis soluble proteins: Extraction, characterization, concentration/fractionation and emulsifying properties[J]. Bioresource Technology,2016,200:147−152. doi: 10.1016/j.biortech.2015.10.012
[60] JIN J, MA H L, WANG K, et al. Effects of multi-frequency power ultrasound on the enzymolysis and structural characteristics of corn gluten meal[J]. Ultrasonics Sonochemistry,2015,24:55−64. doi: 10.1016/j.ultsonch.2014.12.013





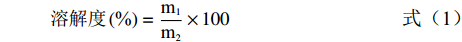

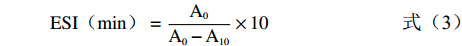
 下载:
下载:






 下载:
下载:
