Application Progress of Fluorescent Nanomaterials as Mimic Enzymes in Biochemical Analysis
-
摘要: 荧光纳米材料主要包括荧光碳纳米材料、荧光金属纳米材料、多功能复合纳米材料和金属框架等,该材料不仅具有特定的荧光强度和较高的光稳定性,还具有纳米材料特有的量子效应、尺寸小等性质。近年来由于其高稳定性、低成本、易制备等特点逐渐成为模拟酶的优选材料,为食品、医疗和生化领域都带来了崭新的发展机遇。本文简要总结了近年来荧光纳米材料作为模拟酶在生化分析中的应用以及最新的研究进展,并对荧光纳米材料作为模拟酶的未来挑战和前景进行展望。Abstract: Fluorescent nanomaterials mainly include fluorescent carbon nanomaterials, fluorescent metal nanomaterials, multifunctional composite nanomaterials and metal frames. The materials not only have unique fluorescence intensity and high photostability, but also have unique quantum effect, small size and other properties of nanomaterials. In recent years, due to its high stability, low cost, easy preparation and other characteristics, it has gradually become the preferred material for mimic enzyme, which has brought new development opportunities for food, medical and biochemical fields. In this paper, the application of fluorescent nanomaterials as mimetic enzymes in biochemical analysis in recent years and the latest research progress are briefly summarized, and the future challenges and prospects of fluorescent nanomaterials as mimetic enzymes are prospected.
-
荧光纳米粒子是指可发出荧光的半导体纳米微晶体或将荧光团通过各种方式引入有机或无机纳米粒子中,并让纳米粒子承担有机小分子荧光染料的检测、标记等功能[1]。荧光纳米材料由荧光纳米粒子组成,由于部分荧光纳米材料具有荧光特性和模拟酶活性,成为近年来科学工作者广泛研究的对象。
荧光纳米粒子作为模拟酶材料不仅克服了天然酶制备繁琐、苛刻条件下变性率高、纯化和保存过程成本高等众多缺陷[2],还具有低毒性、易制备、高稳定性以及良好的生物相容性等优势,因此成为近年来模拟酶领域中最具潜力的纳米材料。此外,由于荧光纳米材料独特的荧光特性,部分荧光纳米材料在作为模拟酶催化物质的同时发生荧光强度的改变,从而达到物质检测的目的,所以荧光纳米材料在生化分析领域中显示出巨大的潜力。
本文综述了荧光纳米材料作为模拟酶在生化分析中的应用进展,旨在为更好地研究开发及利用新型荧光纳米模拟酶材料,为新型荧光纳米模拟酶的性能优化及拓宽应用领域提供理论依据。
1. 荧光碳纳米材料作为模拟酶在生化分析中的应用
荧光纳米模拟酶材料中的碳基质纳米材料如氧化石墨烯[3]、碳纳米管[4]、碳量子点[5]和石墨烯量子点[6]等具有过氧化物酶或超氧化物歧化酶活性。它们具有低细胞毒性、优异的生物相容性、高表面积、高底物特异性、高光稳定性和独特的激发依赖荧光性质[7-10]。因此,荧光碳纳米材料通常以模拟酶或生物传感器的方式广泛应用于食品[11]、生物[12]、医药[13]、环境[14]等方面。
1.1 H2O2的检测
过氧化氢(H2O2)作为一种活性物质,是生命系统中的重要代谢产物。它被认为是氧化应激和生理活性的信号分子和生物标志物[15]。人体内的众多代谢产物都可以通过相应的酶催化反应产生副产物H2O2。因此,开发有效的H2O2检测方法具有重要的价值和意义。
REN等[16]将可再生海洋废弃物生物质浒苔利用简单煅烧的方法绿色合成了具有类氧化酶、类过氧化物酶性质和荧光性质的分级多孔碳(EPC)。基于其氧化酶模拟活性,开发了H2O2荧光生物传感器,由于荧光指示剂巯基乙酸(thioglycolicacid,TA)在羟基存在的条件下转化为强荧光的HTA,所以向EPC-TA体系中加入H2O2,整个体系荧光强度随着H2O2浓度的增加而逐渐增强,不仅验证了EPC的过氧化物酶活性,还实现了对H2O2的检测。该研究首次报道荧光碳纳米材料表现出优异的双重模拟酶活性,为荧光生物传感应用开辟了一个新的道路,为海洋食品样品中H2O2的检测、纳米医学、工业催化和环境工程等领域开辟了新的途径。
氧化石墨烯(graphene oxide,GO)是碳纳米材料之一,由于其特殊的光学和物理化学性质,在生物分子检测方面表现出优异的分析性能。SIDDIQUI等[17]通过GO掺杂硫原子使GO表面改性,相邻的碳原子被激活,并在GO的晶格网络中引起活性边缘和结构缺陷,然后增强催化活性和化学特性。硫掺杂氧化石墨烯(sulfur doped graphene oxide,SGO)由于其良好的吸附和催化能力,可与罗丹明B染料(Rhd-B)和H2O2相互作用。加入H2O2后,羟基自由基的产生淬灭了电荷转移络合物Rhd-B+SGO的荧光。SGO的表面形态和化学性质都有助于该方法的猝灭效率和灵敏度。因此利用SGO的高结合亲和力和淬灭能力,提出了一种高度灵敏和选择性的H2O2检测方法。SGO的低成本、易合成和稳定性等优势,将促进和激发SGO催化剂在表面科学和生物医学中更加广阔的应用前景。
1.2 胆固醇的检测
胆固醇(cholest-5-en-3β-ol)及其酯衍生物是所有动物细胞膜中必需的结构成分之一,是类固醇激素、胆汁酸和维生素D形成的主要前体[18]。高胆固醇血症是心脏骤停、冠心病和其他心血管疾病的主要原因[19]。所以,对胆固醇的检测成为近年来的研究热点。
HASSANZADEH等[20]将葡糖糖粉末以热裂解的方法简单快速地制备了石墨烯量子点(GQDs),通过热处理二硫化钼纳米片获得二硫化钼量子点(MoS2QDs),基于MoS2QDs和GQDs的协同过氧化物酶活性,引入了一种简单并具有选择性的荧光探针的方法检测胆固醇;胆固醇在发生酶促氧化后会产生H2O2,将MoS2QDs和GQDs以3:2的比例混合,向其中加入碱性罗丹明B和胆固醇氧化后得到的H2O2,在1.5~460 nmol·L−1范围内,体系荧光强度随H2O2浓度的增加而增强,并且呈线性关系,基于该方法用于胆固醇的间接测定,成功地分析了人血清样品中游离胆固醇和总胆固醇的含量。
ARYAL等[21]将碳纳米管(CNT)、热还原氧化石墨(TRGO)和CNT-TRGO用对磺酸盐[4]芳烃(SC4)进行官能化,然后在罗丹明6G(R6G)存在下研究胆固醇的荧光检测;所有复合材料(SC4-碳纳米管、SC4-TRGO和SC4-碳纳米管-TRGO)都显示出在没有胆固醇的情况下R6G荧光强度的有效猝灭,但是荧光强度随着胆固醇的加入而显著增加,原因可能是荧光分子R6G占据SC4主体分子的吸附位点空穴,使R6G的特征荧光将由于电荷和能量转移效应而被猝灭;在胆固醇存在的情况下,SC4宿主位点将被胆固醇占据,然后R6G从SC4宿主腔中释放出来,因此恢复R6G的荧光强度。这项工作为水溶性芳烃衍生物在其他生物分子如色氨酸、酪氨酸和组氨酸的荧光检测中的广泛应用指明了方向。
2. 荧光金属纳米材料作为模拟酶在生化分析中的应用
金属纳米团簇由于其易于合成、低成本、优异的光学性质和良好的生物相容性等优点,越来越受到人们的关注[22]。与广泛研究的贵金属纳米团簇(如银纳米团簇和金纳米团簇)相比,铜纳米团簇等显示出独特的光致发光特性、低毒性和便于表面功能化的特点,并且由于相对丰富和廉价的制备前体而更加便宜[23]。本文主要介绍荧光金属纳米材料作为模拟酶用于物质检测和酶活性验证。
2.1 H2O2的检测
金纳米团簇因其易于合成、生物相容性、有限的光漂白和明亮的荧光特性而受到广泛研究。JAIN等[24]利用合成的牛血清白蛋白-抗体修饰的金纳米团簇固有荧光检测人肝细胞(WRL-68)中的H2O2,结果表明,牛血清白蛋白纳米粒呈现鲜红色荧光,牛血清白蛋白纳米粒催化过氧化氢降解为水和分子氧,类似于过氧化氢酶,因此H2O2的暴露导致纳米团簇的荧光强度显著降低,基于此检测H2O2。此外,这些纳米团簇是高度生物相容的,并且在人类肝细胞中被主动内化。尽管已开发的牛血清白蛋白纳米粒在细胞中表现出优异的H2O2传感能力,但还需要更多的研究来实现它们的快速摄取、在细胞质中的长时间停留以及对单个自由基暴露的反应。
FENG等[25]的研究利用四氧化三铁磁性纳米颗粒(Fe3O4MNPs)自身的类过氧化物酶性质,建立了以苯甲酸(BA)为指标的过氧化氢荧光测定方法。以共沉淀法制备的Fe3O4MNPs为过氧化物模拟酶,弱荧光BA可被Fe3O4MNPs所氧化,形成强荧光的羟基苯甲酸,产物羟基苯甲酸的荧光强度(Ex294nm,Em411nm)与过氧化氢的浓度成正比。在优化的条件下,该系统线性范围为0.5~12.5 μmol/L,检出限为0.122 μmol/L,样品的相对标准偏差为4.86% (n=6);实际样品检测中,一次性筷子中H2O2的平均含量为(2.321±0.32) mg/kg。以Fe3O4MNPs为模拟酶的荧光检测法具有良好的重复性、精密度和回收率,可用于各种样品中痕量H2O2的检测。因此该H2O2测定方法在食品[26]和农业[27]中具有很大的价值。
2.2 葡萄糖的检测
血糖水平通常作为糖尿病的临床指标[28]。检测血液中以及食品中的葡萄糖存在诸多方法如荧光分析法[29]、比色法[30-31]和电化学法[32]等。在这些方法中,荧光分析法因其操作简单、响应速度快、成本低而备受关注。
现如今,由于很难控制反应物中金属盐前驱体的还原和成核过程,大多数金属纳米材料的合成都需要非常严格的条件,NIE等[33]通过一种简单的方法直接在水溶液中一步合成了PdCuAu纳米粒子(PdCuAu NPs),合成的PdCuAu NPs具有优异的温度传感器性质和过氧化物模拟酶的催化性能。由于其独特的荧光性质,其荧光强度与温度变化(4~95 ℃)具有良好的线性关系及灵敏度,可用于生物环境的热成像。基于其过氧化物酶样性质,可利用比色法检测H2O2和葡萄糖。该方法简单、快速,为H2O2和葡萄糖的检测开辟了新的道路,同时,这种基于PdCuAu NPs的传感器在生物化学领域具有广阔的应用前景。
银纳米粒子(AgNPs)作为典型的金属纳米粒子,具有特征性的表面等离子体共振和高消光系数,银纳米粒子的结构可以被H2O2破坏,PCN-224作为一种基于卟啉的金属框架,由于其较大的开放通道、良好的生物相容性、优异的生理稳定性和潜在的催化活性中心而被DU等[34]选择作为银纳米粒子的载体,通过酶催化反应高特异性和灵敏度检测H2O2。AgNPs既可以淬灭PCN-224的荧光,又充当H2O2识别剂。由于葡萄糖氧化过程中产生H2O2,AgNPs模拟过氧化物酶与H2O2反应,可以有效地蚀刻成银离子并从PCN-224中释放出来,从而恢复PCN-224的荧光。此传感平台被进一步扩展到监测人血清样本中的葡萄糖,表明其在诊断目的方面具有良好的潜力。
2.3 碱性磷酸酶的检测
碱性磷酸酶(ALP)是蛋白质、核酸和其他小分子磷酸盐代谢的关键水解酶,广泛分布于哺乳动物体液和组织中,碱性磷酸酶在不同的生物过程中起着重要的作用。然而,碱性磷酸酶的异常水平通常与引发多种疾病,如肝功能障碍、骨病、癌症和糖尿病[35]。因此,迫切需要开发简单、准确、高灵敏度的ALP检测方法。
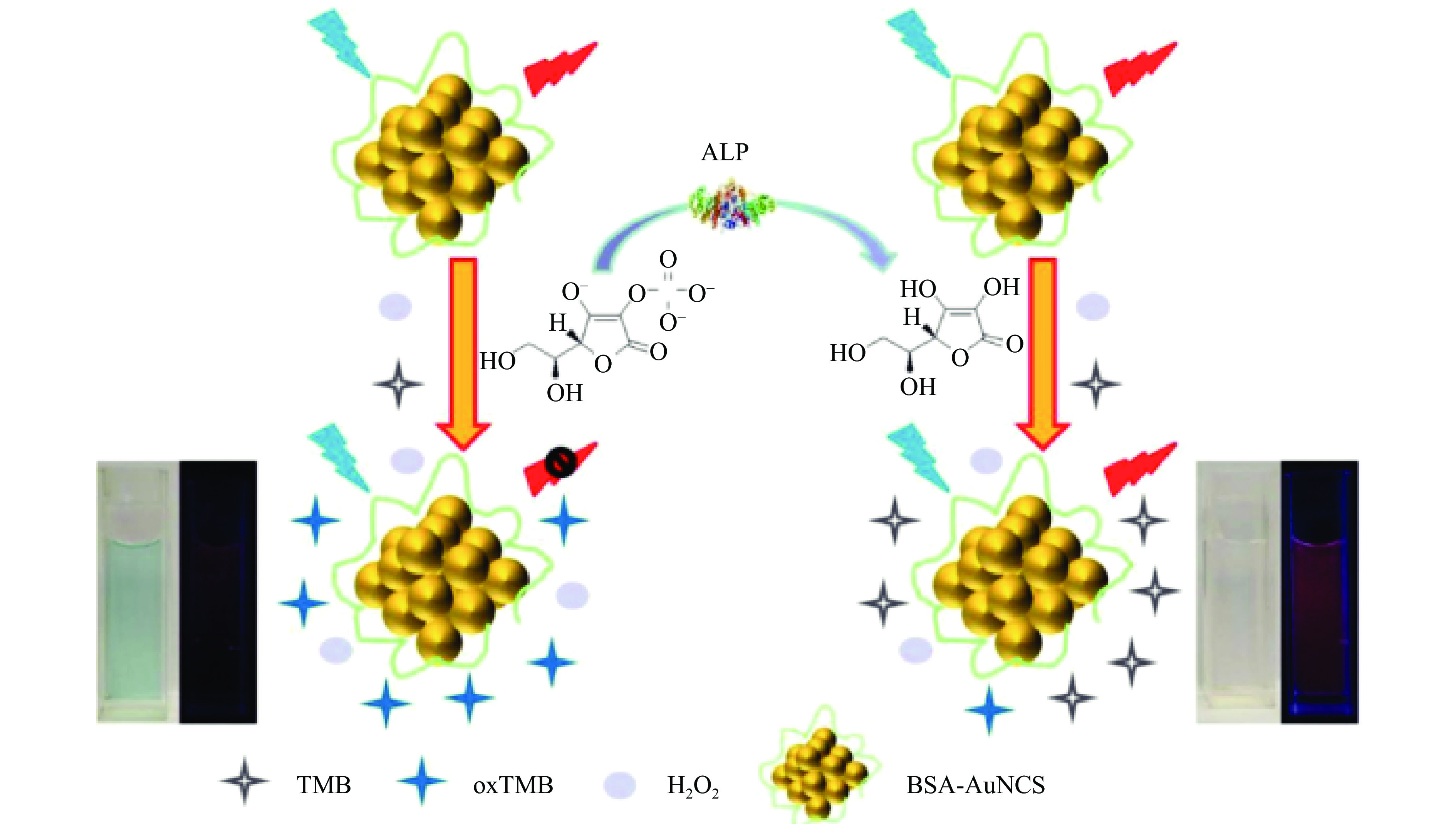
NI等[36]利用牛血清白蛋白结合的金纳米团簇(BSA-AuNCs),基于其过氧化物酶活性和荧光特性,建立了一种比色和荧光双通道检测ALP活性的方法。BSA-AuNCs能够催化H2O2将无色TMB氧化为蓝色的ox-TMB,同时导致BSA-AuNCs的荧光猝灭。抗坏血酸是由ALP催化L-抗坏血酸-2-磷酸水解得到的,能抑制TMB的氧化,从而诱导ox-TMB的脱色和BSA-AuNCs的荧光恢复(如图1)。比色法和荧光法的检测限分别可达0.26和0.16 mUmL−1。此外,该方法已成功应用于人血清样品中ALP的检测。该方法不仅为简单、灵敏、准确地检测ALP活性提供了新思路,而且拓宽了BSA-AuNCs在生物分析中的应用。
2.4 胆固醇的检测
GUAN等[37]通过自组装的方式制备金纳米粒子,该金纳米粒子可以通过H2O2催化氧化ABTS产生绿色产物,结合胆固醇氧化酶与胆固醇反应生成H2O2的原理实现胆固醇的检测。结果表明,合成的金纳米粒子对胆固醇具有良好的选择性和抗干扰性,并成功应用于鸡蛋样品中胆固醇的检测。
3. 多功能纳米复合材料作为模拟酶在生化分析中的应用
3.1 H2O2的检测
PRATSINIS等[38]制备了具有独特的荧光性质和过氧化物酶活性的Eu3+掺杂的氧化铈纳米粒子在研究其模拟过氧化氢酶的抗氧化活性时,表现为水溶液中H2O2的催化分解,H2O2中的活性氧与氧化铈纳米颗粒表面的活性位点发生强相互作用,使纳米颗粒发生显著的荧光淬灭,从而测定了H2O2的浓度,该检测体系的灵敏度低至0.15 μmol/L。基于多功能纳米复合材料可进行复杂的体外试验,实现对疾病生物标志物的高灵敏度检测。此方法为H2O2的检测提供了新的思路。
MATHIVANAN等[39]合成了具有荧光性质的双发射氮/锌掺杂碳点(N/Zn-CDs)对H2O2进行检测,在不同浓度范围的H2O2存在下,测量了合成的N/Zn-CDs的荧光响应,结果表明,当H2O2浓度增加时,N/Zn-CDs发生显著的荧光淬灭,荧光信号的强度逐渐降低,并在H2O2不同浓度范围(1~3 μmol/L)显示良好的线性关系,H2O2的检出限为0.27 μmol/L。双发射复合碳点作为模拟酶和荧光探针传感系统,为实际样品中H2O2的检测提供了新的平台。
3.2 葡萄糖的检测
近年来,人们探索出许多方法来高精度地测定葡萄糖浓度,其中,比色和荧光法因其简单、成本低、灵敏度高、便于携带和可颜色识别而引起了极大的关注。另一方面,许多研究是基于单信号测定(比色测定或荧光测定),单个信号测定可能会受到外部条件的影响,因此,需要一种双信号检测葡萄糖的方法。
YEN等[40]开发了基于比色和荧光法的双传感器,将合成的具有类过氧化物酶活性的氮掺杂碳点金属氧化物杂化物(MFNCDs),用于定量测定H2O2和葡萄糖的浓度,基于比色法的H2O2和葡萄糖的检测限分别低至84 nmol/L和0.41 μmol/L。相比之下,在H2O2的存在下,通过内过滤效应(IFE)和系统中各元件之间的电子转移,MFNCDs/TMB在405 nm处的荧光被淬灭。利用上述特性,开发了基于比色和荧光方法的双传感器,用于定量测定H2O2和葡萄糖的浓度。基于荧光方法的H2O2和葡萄糖的检测限分别低至97 nmol/L和0.85 μmol/L。此外,这种双传感器可用于检测真实血清中的葡萄糖,结果非常准确,该双传感体系检测方法克服了传统单因素检测物质对环境条件要求高的缺陷,并且还具有较高的灵敏度及选择性是生物传感器应用的良好选择。
3.3 尿酸的检测
尿酸(Uric acid,UA)是人体内必不可少的生物分子,也是嘌呤的最终代谢产物[41]。到目前为止,已经建立了几种检测尿酸的分析技术,包括电化学检测[42]、荧光光谱法[43]、毛细管电泳[44]、高效液相色谱法[45]、比色法[46]。已经证明,血清中尿酸浓度过高与许多代谢紊乱密切相关。极低浓度的尿酸会导致氧化应激或多发性硬化等症状。因此,尿酸的定量检测显得尤为必要。
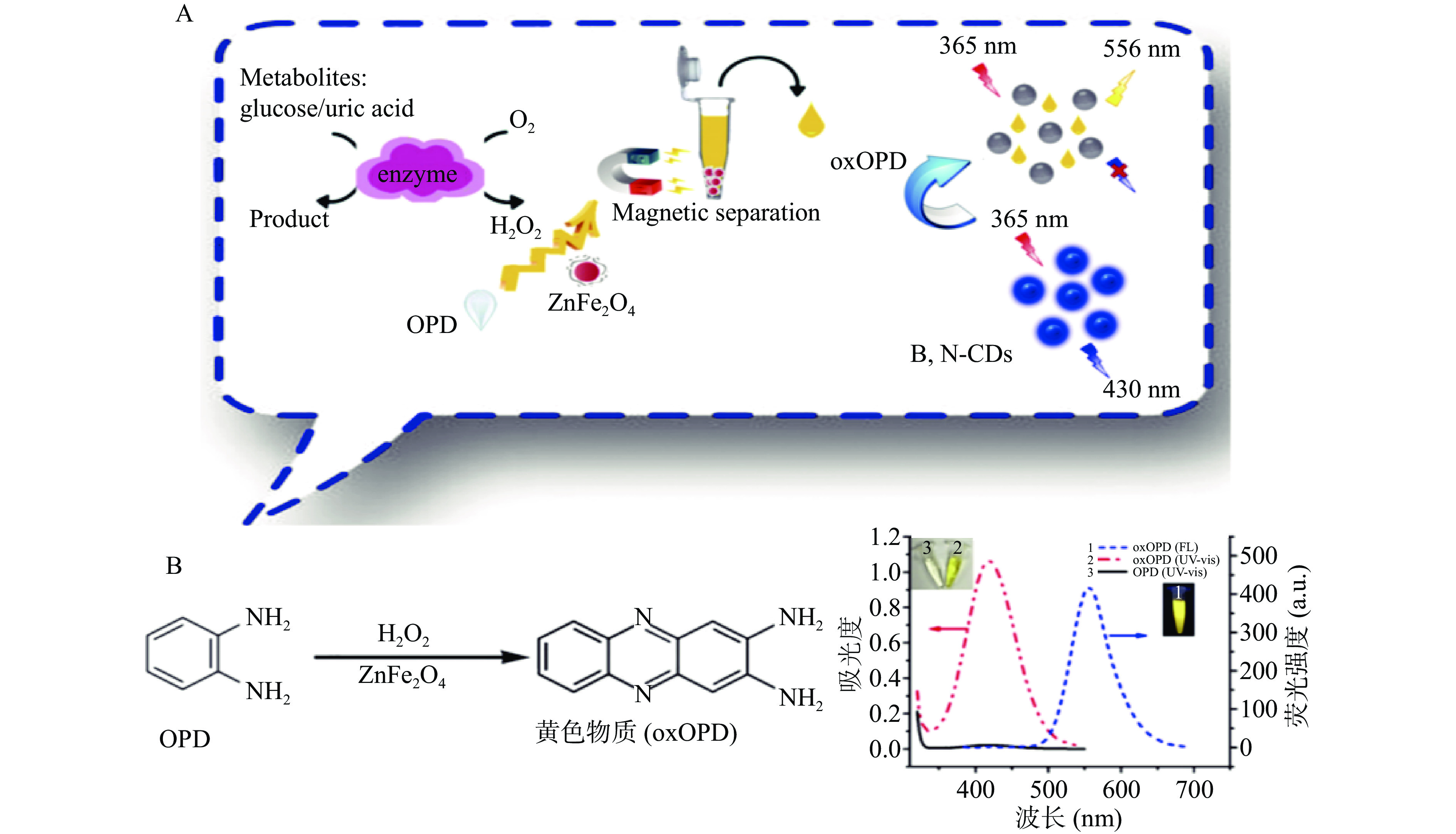
XIAO等[47]使用唯一的前体3-APBA·H2O作为氮、碳和硼源通过水热法合成B,N-CDs,基于银纳米簇和CDs独特的荧光性质,将B,N-CDs和ZnFe2O4磁性微球结合构建了比色和荧光比率的双重读出传感器,该传感器以ZnFe2O4磁性微球为过氧化物酶模拟物,在H2O2存在下催化氧化邻苯二胺(OPD),生成典型的黄色物质(oxOPD),oxOPD可以通过内滤光效应显著淬灭B,N-CDs在430 nm处的荧光,并在556 nm处产生新的荧光发射峰(如图2)。因此,荧光强度比(I556/I430)可用于定量分析H2O2和H2O2相关代谢物即葡萄糖和尿酸的浓度。基于溶液颜色变化也可用于确定H2O2、葡萄糖和UA水平。基于比色检测的H2O2、葡萄糖和UA的检测限分别为0.09、0.9和0.9 μmol/L,使用比率荧光检测的检测限分别为0.1、8和1 μmol/L。此外,该策略还可以检测人血清中的葡萄糖和尿酸。该方法在H2O2及相关代谢物检测中具有潜在的应用价值。
3.4 有机化合物的检测
邻苯二胺(OPD)是一种重要的化学中间体,也是许多杂环化合物的前体。此外,OPD的工业用途非常广泛,特别是制造农药、感光资源、聚合物、染料等[48]。在人体内发现的大量OPD可能会影响消化系统和呼吸功能,有时还可能容易致癌。OPD的快速准确测定是生物分析、食品安全和环境保护等众多领域的重要任务之一。
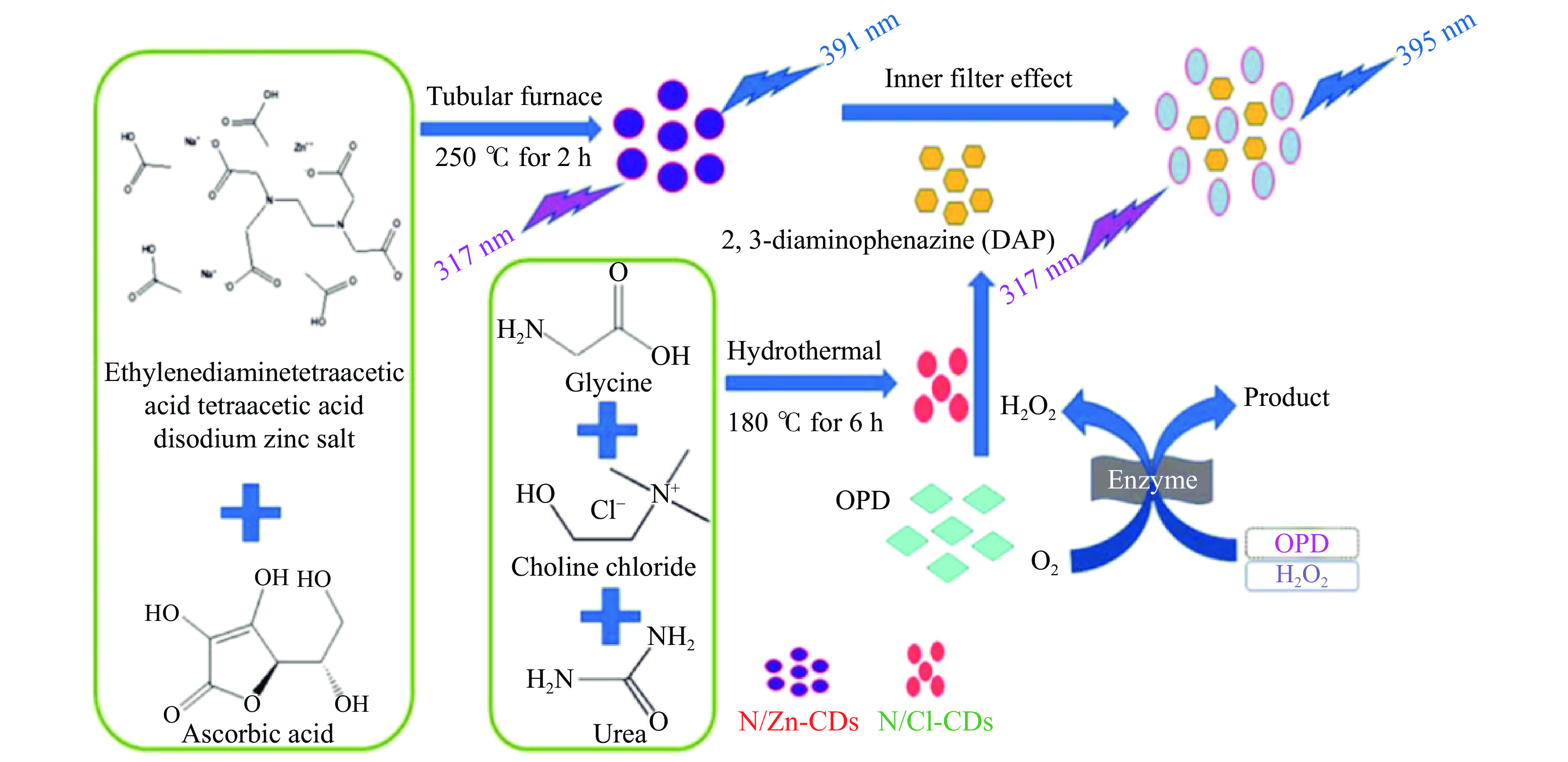
MATHIVANAN等[39]首次用甘氨酸、氯化胆碱和尿素合成了氮/氯掺杂碳点(N/Cl-CDs);同时,以乙二胺四乙酸二钠锌盐和抗坏血酸为前驱体,合成了氮/锌掺杂碳点(N/Zn-CDs);合成的CDs被用作模拟酶和荧光探针,该双碳点体系用于识别OPD和H2O2;N/Cl-CDs由于其过氧化物酶活性,在H2O2存在下氧化无色的OPD生成黄色的2,3-二氨基吩嗪(DAP)。随后,生成的DAP猝灭了N/Zn-CDs的荧光,实现了对OPD以及H2O2的检测(如图3)。该双碳点体系展示出碳点功能的多样性,为碳点的后续发展奠定了基础。
对苯二酚是一种苯的两个对位氢被羟基取代形成的有机化合物,分子式为C6H6O2,为白色结晶,又叫氢醌(H2Q),是一种剧毒有机化合物,主要应用于各种染料的制备以及许多大规模的工业和生物方面[49]。目前,已经报道了许多测定H2Q的方法,如荧光法[50]、电化学方法[51]和高效液相色谱[52]。
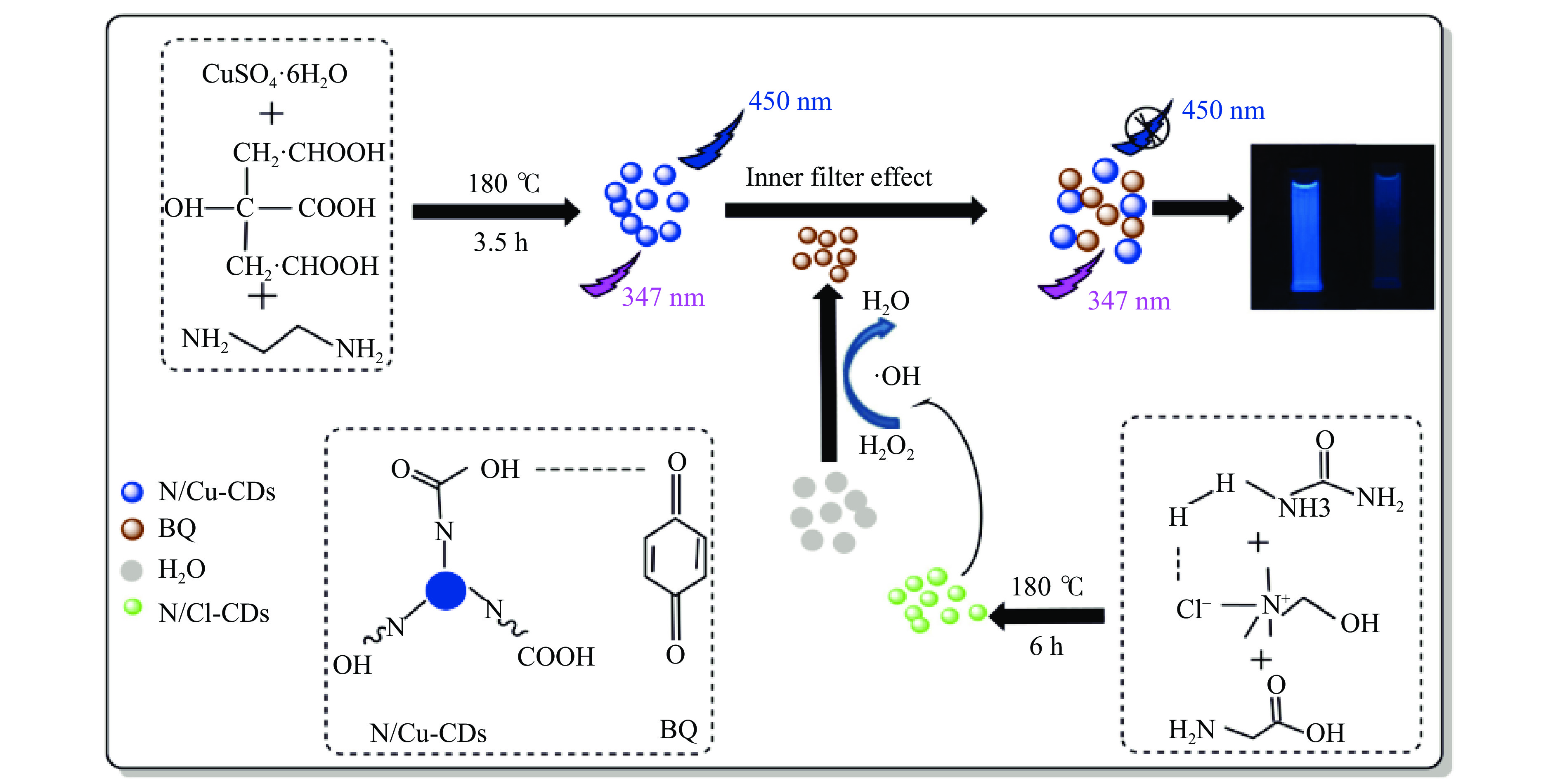
WANG等[53]利用水热法合成了氮/氯掺杂碳点(N/Cl-CDs)和氮/锌掺杂碳点(N/Cu-CDs);合成的CDs被用作模拟酶和荧光探针,该双碳点体系用于识别痕量H2Q。N/Cl-CDs由于其过氧化物酶活性,在H2O2存在下氧化灰色的H2Q生成棕色对苯醌(BQ);随后,生成的BQ猝灭了N/Cu-CDs的荧光,实现了对H2Q的检测(如图4)。
3.5 超痕量K+的检测
纳米复合材料作为模拟酶的应用范围极其广泛,不仅可以应用于常量物质的检测,还可应用于超痕量物质的检测。LI等[54]以玉米淀粉、乙二胺和氯金酸为原料,通过微波辐射快速制备了高催化活性且高稳定性的氮、金共掺杂碳点(CDN/Au),CDN/Au在TMB-H2O2指示剂反应中表现出很强的催化作用,生成了氧化产物ox-TMB,并发生荧光淬灭效应。将纳米酶反应与钾离子适体-血红素的脱氧核酶反应相结合,建立了一种双酶催化荧光/吸收双模式方法来检测超痕量K+。此方法具有良好的选择性和灵敏度,并且这一新方法也被用于其他形成G-四链体和血红素的脱氧核酶的适体反应
4. 金属有机框架作为模拟酶在生化分析中的应用
金属有机框架(MOFs)是一种结构可调、具有模拟酶性质的功能性荧光纳米材料。目前研究最多的是用于对对胆碱及乙酰胆碱的检测。
胆碱作为一种维生素B,是人类的必需营养素,并参与肌肉运动、大脑发育和新陈代谢[55]。此外,它是乙酰胆碱(ACh)的前体,乙酰胆碱是外周和中枢神经系统中的重要神经递质[56]。胆碱和乙酰胆碱的异常水平能够引发多种神经疾病,包括精神分裂症、进行性痴呆、帕金森氏病和阿尔茨海默氏病[57]。因此,灵敏和选择性地检测生物样品中胆碱和乙酰胆碱的水平对于临床分析和相关疾病的早期诊断至关重要。
GUO等[58]合成了一种具有模拟过氧化物酶和荧光发射双重功能的MIL-101(Fe),构建了基于MIL-101(Fe)纳米酶的胆碱和乙酰胆碱无标记荧光传感器;这种荧光传感策略包括乙酰胆碱酯酶催化乙酰胆碱水解为胆碱的反应,胆碱又被胆碱氧化酶氧化生成H2O2,生成的H2O2在MIL-101(Fe)纳米酶的催化下分解为高活性羟基,从而MIL-101(Fe)纳米酶的非荧光有机配体对苯二甲酸被羟基氧化形成高荧光的2-羟基对苯二甲酸;根据这一发现,通过多级酶联反应实现了对胆碱和乙酰胆碱的无标记检测,检测限分别为20.0 和8.9 nmol/L;此外,通过检测牛奶中的胆碱和人血浆中的乙酰胆碱,成功地验证了所开发的基于双功能MIL-101(Fe)的传感策略的实用性。该方法不仅对胆碱和乙酰胆碱具有较高的灵敏度和选择性,而且简化了传感系统,降低了检测成本,避免了荧光试剂带来的潜在风险,为复杂生物样品的分析开辟了一条绿色通道。
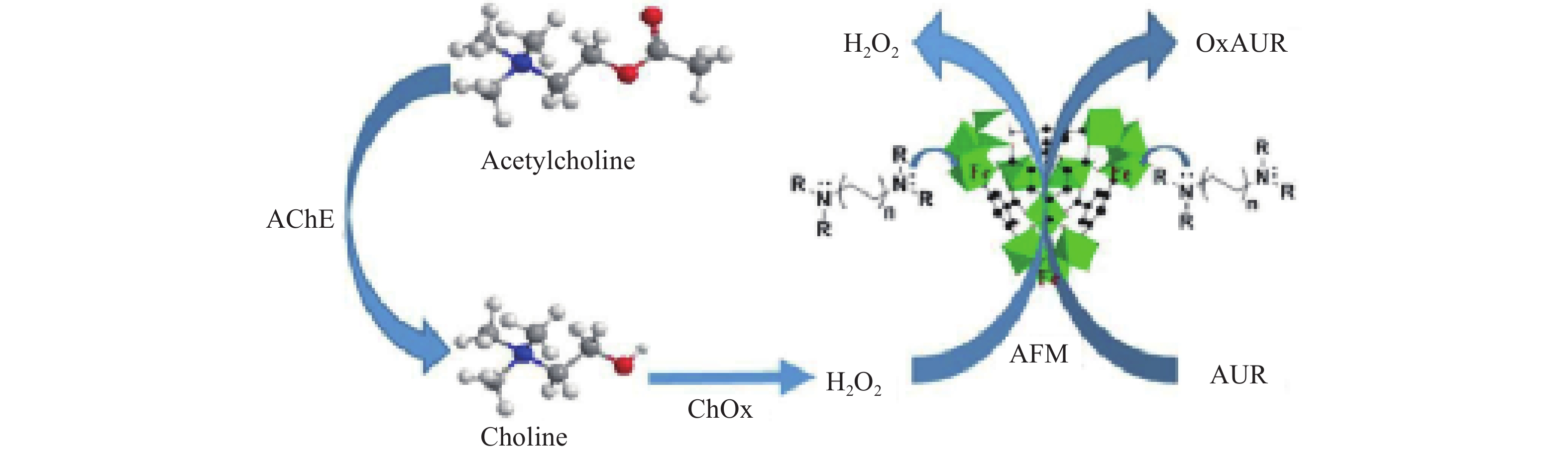
VALEKAR等[59]合成了一种具有过氧化物酶活性和荧光特性双重功能的N,N,N’,N’-四甲基-1,4-丁二胺(TMBDA)官能化MIL-100(Fe) (TMBDA-MIL-100(Fe)),用于荧光定量检测Cho和ACh,通过乙酰胆碱的连续催化氧化产生H2O2,激活胺官能化的TMBDA-MIL-100(Fe),将选定的底物AUR转化为高荧光产物(oxAUR)(如图5);基于TMBDA-MIL-100(Fe)优异的过氧化物酶活性检测胆碱和乙酰胆碱,检出限分别为0.027和0.036 μmol/L。此外,通过分别检测牛奶和血清加标样品中的胆碱和乙酰胆碱,成功证明了该方法的实用性。
5. 结语与展望
近年来,随着荧光分析技术的发展,纳米荧光材料已经被广泛应用于各个研究领域。本文总结了现阶段基于荧光纳米材料作为模拟酶在生化分析中应用的研究进展。基于荧光纳米材料的模拟酶活性,实现了对维生素、葡萄糖、活性分子、代谢产物等物质以及酶活性的检测,并且在医学领域,如免疫分析、肿瘤诊断以及癌细胞的检验和靶向治疗中均表现出较好的检测效果。但是荧光纳米材料作为模拟酶材料的应用和发展仍有很多问题需要解决,例如,缺少一种通用而有效的方法,合成的荧光纳米材料仅局限于一种或很少几种待测物的检测,容易造成材料浪费、检测成本加大、检测效率低等问题。此外,目前基于荧光纳米材料的荧光传感较多情况下采用单一荧光强度作为响应信号,容易受到仪器误差、溶剂等实验因素的影响。与单一信号的荧光传感器不同,比率型荧光传感器可以在很大程度上减少上述干扰,通过两种荧光强度的自校准实现更高的分析准确度,并且比率型荧光法多伴随肉眼可见的颜色变化,可用于快速的可视化识别检测。荧光纳米材料在未来的发展中应着重于开发可视化便携式检测技术,并且实现同时对不同离子进行检测。因此,未来基于荧光纳米材料作为模拟酶在生化分析中的应用研究仍具有广阔的研究空间。
-
-
[1] 翁文婷, 王思玉, 庄君阳. 聚多巴胺原位还原银纳米增强碳点荧光自组装纳米复合膜用于检测葛根素研究[J]. 光谱学与光谱分析,2021,41(1):168−176. [WENG W T, WANG S Y, ZHUANG J Y. Self-Assembled nanocomposite film of AgN in-situ grown on polydopamine with enhanced fluorescence of CDs for detection of puerarin[J]. Spectroscopy and Spectral Analysis,2021,41(1):168−176. WENG W T, WANG S Y, ZHUANG J Y. Self-Assembled nanocomposite film of AgN in-Situ grown on polydopamine with enhanced fluorescence of CDs for detection of puerarin[J]. Spectroscopy and Spectral Analysis, 2021, 41(1): 168-176.
[2] 钟青梅, 黄欣虹, 覃庆敏, 等. 以碳量子点为过氧化物模拟酶的葡萄糖测定方法[J]. 分析化学,2018,46(7):1062−1068. [ZHONG Q M, HUANG X H, QIN Q M, et al. Determination of glucose based on carbon quantum dots as peroxidase mimetic enzyme[J]. Chinese Journal of Analytical Chemistry,2018,46(7):1062−1068. doi: 10.11895/j.issn.0253-3820.171396 ZHONG Q M, HUANG X H, QIN Q M, et al. Determination of glucose based on carbon quantum dots as peroxidase mimetic enzyme[J]. Chinese Journal of Analytical Chemistry, 2018, 46(7): 1062-1068. doi: 10.11895/j.issn.0253-3820.171396
[3] YAO X, LIU T, XIE Y, et al. In situ-forming magnetic Fe3O4nanoroses on defect-controllable mesoporous graphene oxide for enzyme-mimic sensing[J]. Industrial & Engineering Chemistry Research,2020,59(40):17934−17943.
[4] SONG H, MA C, WANG L, et al. Platinum nanoparticle-deposited multi-walled carbon nanotubes as a NADH oxidase mimic: characterization and applications[J]. Nanoscale,2020,12(37):19284−19292. doi: 10.1039/D0NR04060F
[5] FARNOOSH A, MAHSA G S, BEHNAM R, et al. Nanozymes with intrinsic peroxidase-like activities[J]. Journal of Molecular Liquids,2019,278:130−144. doi: 10.1016/j.molliq.2018.12.011
[6] XIN Q, JIA X, NAWAZ A, et al. Mimicking peroxidase active site microenvironment by functionalized graphene quantum dots[J]. Nano Research,2020,13(5):1427−1433. doi: 10.1007/s12274-020-2678-z
[7] SURENDRAN P, LAKSHMANAN A, PRIYA S S, et al. Fluorescent carbon quantum dots from Ananas comosus waste peels: A promising material for NLO behaviour, antibacterial, and antioxidant activities[J]. Inorganic Chemistry Communications,2021,124:108397. doi: 10.1016/j.inoche.2020.108397
[8] CHAUDHARY S, KUMARI M, CHAUHAN P, et al. Upcycling of plastic waste into fluorescent carbon dots: An environmentally viable transformation to biocompatible C-dots with potential prospective in analytical applications[J]. Waste Management,2021,120:675−686. doi: 10.1016/j.wasman.2020.10.038
[9] HUANG G, LIU Y, CHEN H, et al. A novel grafting-template method to prepare three-dimensional hierarchical porous carbon with high surface area and electrical conductivity for superior-performance supercapacitors[J]. Journal of Power Sources,2021,482:228922. doi: 10.1016/j.jpowsour.2020.228922
[10] PAN M, XIE X, LIU K, et al. Fluorescent carbon quantum dots—synthesis, functionalization and sensing application in food analysis[J]. Nanomaterials,2020,10(5):930. doi: 10.3390/nano10050930
[11] YUE X Y, ZHOU Z J, WU Y M, et al. Application progress of fluorescent carbon quantum dots in food analysis[J]. Chinese Journal of Analytical Chemistry,2020,48(10):1288−1296. doi: 10.1016/S1872-2040(20)60049-4
[12] SOBIECH M, LULIŃSKI P, WIECZOREK P P, et al. Quantum and carbon dots conjugated molecularly imprinted polymers as advanced nanomaterials for selective recognition of analytes in environmental, food and biomedical applications[J]. TrAC Trends in Analytical Chemistry,2021,142:116306. doi: 10.1016/j.trac.2021.116306
[13] CILINGIR E K, SEVEN E S, ZHOU Y, et al. Metformin derived carbon dots: Highly biocompatible fluorescent nanomaterials as mitochondrial targeting and blood-brain barrier penetrating biomarkers[J]. Journal of Colloid and Interface Science,2021,592:485−497. doi: 10.1016/j.jcis.2021.02.058
[14] GAVIRIA-ARROYAVE M I, CANO J B, PEÑUELA G A. Nanomaterial-based fluorescent biosensors for monitoring environmental pollutants: A critical review[J]. Talanta Open,2020,2:100006. doi: 10.1016/j.talo.2020.100006
[15] 李姚, 王健. 藏红花素抑制过氧化氢诱导的视网膜色素上皮细胞凋亡[J]. 中国中医眼科杂志,2019,29(5):347−350. [LI Y, WANG J. Crocin inhibits the retinal pigment epithelial cell apoptosis induced by H2O2[J]. China Journal of Chinese Ophthalmology,2019,29(5):347−350. LI Y, WANG J. Crocin inhibits the retinal pigment epithelial cell apoptosis induced by H2O2 [J]. China Journal of Chinese Ophthalmology, 2019, 29(5): 347-350.
[16] REN H, LIU X, YAN L, et al. Ocean green tide derived hierarchical porous carbon with bi-enzyme mimic activities and their application for sensitive colorimetric and fluorescent biosensing[J]. Sensors and Actuators B Chemical,2020,312:127979. doi: 10.1016/j.snb.2020.127979
[17] SIDDIQUI A S, HAYAT A, NAWAZ M H, et al. Effect of sulfur doping on graphene oxide towards amplified fluorescence quenching based ultrasensitive detection of hydrogen peroxide[J]. Applied Surface Science,2020,509:144695. doi: 10.1016/j.apsusc.2019.144695
[18] LI L H, DUTKIEWICZ E P, HUANG Y C, et al. Analytical methods for cholesterol quantification[J]. Journal of Food and Drug Analysis,2019,27(2):375−386. doi: 10.1016/j.jfda.2018.09.001
[19] PRIYADARSHINI E, RAWAT K. Au@carbon dot nanoconjugates as a dual mode enzyme-free sensing platform for cholesterol[J]. Journal of Materials Chemistry B,2017,5(27):5425−5432. doi: 10.1039/C7TB01345K
[20] HASSANZADEH J, KHATAEE A. Ultrasensitive chemiluminescent biosensor for the detection of cholesterol based on synergetic peroxidase-like activity of MoS2 and graphene quantum dots[J]. Talanta,2017,178:992−1000.
[21] ARYAL K P, EKANAYAKA T K, GILBERT S, et al. Fluorescent detection of cholesterol using p-Sulfonatocalix [4] arene functionalized carbon nanotubes and thermally reduced graphite oxide composites[J]. Chemical Physics Letters,2020,738:136856. doi: 10.1016/j.cplett.2019.136856
[22] HU X, LIU X, ZHANG X, et al. One-pot synthesis of the CuNCs/ZIF-8 nanocomposites for sensitively detecting H2O2 and screening of oxidase activity[J]. Biosensors & Bioelectronics,2018,105:65−70.
[23] BENAVIDES J, QUIJADA-GARRIDO I, GARCÍA O. The synthesis of switch-off fluorescent water-stable copper nanocluster Hg2+ sensors via a simple one-pot approach by anin situ metal reduction strategy in the presence of a thiolated polymer ligand template[J]. Nanoscale,2020,12(2):944−955. doi: 10.1039/C9NR08439H
[24] JAIN V, BHAGAT S, SINGH S. Bovine serum albumin decorated gold nanoclusters: A fluorescence-based nanoprobe for detection of intracellular hydrogen peroxide[J]. Sensors and Actuators B:Chemical,2021,327:128886. doi: 10.1016/j.snb.2020.128886
[25] FENG X, YANG J, WU S, et al. Fluorometric determination of hydrogen peroxide using Fe3O4 magnetic nanoparticles as a mimetic enzyme[J]. Digest Journal of Nanomaterials and Biostructures,2020,15(3):931−942.
[26] NING K, XIANG G, WANG C, et al. ‘Turn-on’fluorescence sensing of hydrogen peroxide in marine food samples using a carbon dots–MnO2 probe[J]. Luminescence,2020,35(6):897−902. doi: 10.1002/bio.3799
[27] SU D, LI H, YAN X, et al. Biosensors based on fluorescence carbon nanomaterials for detection of pesticides[J]. TrAC Trends in Analytical Chemistry,2020,134:116126.
[28] HABADI M I, ALRASHIDI M M, MUTAKI I F, et al. Diagnosis of dysglycemia in diabetic patients in primary health care[J]. Journal of Pharmaceutical Research International,2021:14−19.
[29] LU Q, HUANG T, ZHOU J, et al. Limitation-induced fluorescence enhancement of carbon nanoparticles and their application for glucose detection[J]. Spectrochimica Acta Part A:Molecular and Biomolecular Spectroscopy,2021,244:118893. doi: 10.1016/j.saa.2020.118893
[30] MERCAN Ö B, KILIÇ V, ŞEN M. Machine learning-based colorimetric determination of glucose in artificial saliva with different reagents using a smartphone coupled μPAD[J]. Sensors and Actuators B:Chemical,2021,329:129037. doi: 10.1016/j.snb.2020.129037
[31] ALLE M, PARK S C, BANDI R, et al. Rapid in-situ growth of gold nanoparticles on cationic cellulose nanofibrils: Recyclable nanozyme for the colorimetric glucose detection[J]. Carbohydrate Polymers,2021,253:117239. doi: 10.1016/j.carbpol.2020.117239
[32] GAO J, HE S, NAG A. Electrochemical detection of glucose molecules using laser-induced graphene sensors: A review[J]. Sensors,2021,21(8):2818. doi: 10.3390/s21082818
[33] NIE F, GA L, AI J, et al. TrimetallicPdCuAunanoparticles for temperature sensing and fluorescence detection of H2O2 and glucose[J]. Frontiers in Chemistry,2020,8:244. doi: 10.3389/fchem.2020.00244
[34] DU P, NIU Q, CHEN J, et al. “Switch-On” fluorescence detection of glucose with high specificity and sensitivity based on silver nanoparticles supported on porphyrin metal–organic frameworks[J]. Analytical chemistry,2020,92(11):7980−7986. doi: 10.1021/acs.analchem.0c01651
[35] LIU Y, DONG P, JIANG Q, et al. Assembly-enhanced fluorescence from metal nanoclusters and quantum dots for highly sensitive biosensing[J]. Sensors and Actuators B:Chemical,2019,279:334−341. doi: 10.1016/j.snb.2018.10.016
[36] NI P, CHEN C, JIANG Y, et al. Gold nanoclusters-based dual-channel assay for colorimetric and turn-on fluorescent sensing of alkaline phosphatase[J]. Sensors and Actuators B Chemical,2019,301:127080. doi: 10.1016/j.snb.2019.127080
[37] GUAN H, SONG Y, HAN B, et al. Colorimetric detection of cholesterol based on peroxidase mimetic activity of GoldMag nanocomposites[J]. Spectrochimica Acta Part A:Molecular and Biomolecular Spectroscopy,2020,241:118675. doi: 10.1016/j.saa.2020.118675
[38] PRATSINIS A, KELESIDIS G A, ZUERCHER S, et al. Enzyme-mimetic antioxidant luminescent nanoparticles for highly sensitive hydrogen peroxide biosensing[J]. Acs Nano,2017,11(12):12210−12218. doi: 10.1021/acsnano.7b05518
[39] MATHIVANAN D, TAMMINA S K, WANG X, et al. Dual emission carbon dots as enzyme mimics and fluorescent probes for the determination of o-phenylenediamine and hydrogen peroxide[J]. Microchimica Acta,2020,187(5):1−9.
[40] NGO Y L T, NGUYEN P L, JANA J, et al. Simple paper-based colorimetric and fluorescent glucose sensor using N-doped carbon dots and metal oxide hybrid structures[J]. Analytica Chimica Acta,2021,1147:187−198. doi: 10.1016/j.aca.2020.11.023
[41] HSIEH M W, CHEN H Y, TSAI C C. Screening and evaluation of purine-nucleoside-degrading lactic acid bacteria isolated from winemaking byproductsin vitro and their uric acid-lowering effects in vivo[J]. Fermentation,2021,7(2):74. doi: 10.3390/fermentation7020074
[42] MAZZARA F, PATELLA B, AIELLO G, et al. Electrochemical detection of uric acid and ascorbic acid using r-GO/NPs based sensors[J]. Electrochimica Acta,2021,388:138652. doi: 10.1016/j.electacta.2021.138652
[43] HAN L J, KONG Y J, HOU G Z, et al. A europium-based MOF fluorescent probe for efficiently detecting malachite green and uric acid[J]. Inorganic Chemistry,2020,59(10):7181−7187. doi: 10.1021/acs.inorgchem.0c00620
[44] ÖZçELIK S, ÖZTEKIN N, KIYKIM E, et al. Capillary electrophoresis with capacitively coupled contactless conductivity detection for the determination of urinary ethylmalonic acid for the diagnosis of ethylmalonic aciduria[J]. Journal of Separation Science,2020,43(7):1365−1371. doi: 10.1002/jssc.201901044
[45] VLASSA M, FILIP M, DRAGOMIR C. Simultaneous quantifications of four purine derivatives biomarkers in cow milk by SPE HPLC-DAD[J]. Czech Journal of Food Sciences,2021,39(2):122−130. doi: 10.17221/297/2020-CJFS
[46] SHI R, QIN X, YUAN C L, et al. Colorimetric determination of uric acid with molybdenum disulfide nanosheets as peroxidase mimetic enzyme[J]. Chinese Journal of Analytical Chemistry,2021,49(3):397−406.
[47] XIAO N, LIU S G, MO S, et al. B, N-carbon dots-based ratiometric fluorescent and colorimetric dual-readout sensor for H2O2 and H2O2-involved metabolites detection using ZnFe2O4 magnetic microspheres as peroxidase mimics[J]. Sensors and Actuators,2018,273:1735−1743. doi: 10.1016/j.snb.2018.07.097
[48] ZHANG S, LIN F, YUAN Q, et al. Robust magnetic laccase-mimicking nanozyme for oxidizing o-phenylenediamine and removing phenolic pollutants[J]. Journal of Environmental Sciences,2020,88:103−111. doi: 10.1016/j.jes.2019.07.008
[49] PU H, SUN Q, TANG P, et al. Characterization and antioxidant activity of the complexes of tertiary butylhydroquinone with β-cyclodextrin and its derivatives[J]. Food Chemistry,2018,260:183−192. doi: 10.1016/j.foodchem.2018.04.008
[50] WANG Y, YUE Q, TAO L, et al. Fluorometric determination of hydroquinone by using blue emitting N/S/P-codoped carbon dots[J]. Microchimica Acta,2018,185(12):1−9.
[51] BULEDI J A, AMEEN S, KHAND N H, et al. CuO nanostructures based electrochemical sensor for simultaneous determination of hydroquinone and ascorbic acid[J]. Electroanalysis,2020,32(7):1600−1607. doi: 10.1002/elan.202000083
[52] TSUTAHARA R, NISHIHARA M, OSUMI Y. Simultaneous determination of arbutin and hydroquinone in dried bearberry leaf extracts by HPLC[J]. BUNSEKI KAGAKU,2020,69(7-8):357−362. doi: 10.2116/bunsekikagaku.69.357
[53] WANG X, CHENG Z, ZHOU Y, et al. A double carbon dot system composed of N, Cl-doped carbon dots and N, Cu-doped carbon dots as peroxidase mimics and as fluorescent probes for the determination of hydroquinone by fluorescence[J]. Microchimica Acta,2020,187(6):1−8.
[54] LI C, LIU Q, WANG X, et al. An ultrasensitive K+ fluorescence/absorption di-mode assay based on highly co-catalysiscarbon dot nanozyme and DNAzyme[J]. Microchemical Journal,2020,159:105508. doi: 10.1016/j.microc.2020.105508
[55] GUO J, WANG Y, ZHAO M. Target-directed functionalized ferrous phosphate-carbon dots fluorescent nanostructures as peroxidase mimetics for cancer cell detection and ROS-mediated therapy[J]. Sensors and Actuators B:Chemical,2019,297:126739. doi: 10.1016/j.snb.2019.126739
[56] AKHTAR M H, HUSSAIN K K, GURUDATT N G, et al. Detection of Ca2+-induced acetylcholine released from leukemic T-cells using an amperometric microfluidic sensor[J]. Biosensors and Bioelectronics,2017,98:364−370. doi: 10.1016/j.bios.2017.07.003
[57] MATHEW M S, BAKSI A, PRADEEP T, et al. Choline-induced selective fluorescence quenching of acetylcholinesterase conjugated Au@ BSA clusters[J]. Biosensors and Bioelectronics,2016,81:68−74. doi: 10.1016/j.bios.2016.02.048
[58] GUO J, WU S, WANG Y, et al. A label-free fluorescence biosensor based on a bifunctional MIL-101(Fe) nanozyme for sensitive detection of choline and acetylcholine at nanomolar level[J]. Sensors and Actuators B Chemical,2020,312:128021. doi: 10.1016/j.snb.2020.128021
[59] VALEKAR A H, BATULE B S, KIM M I, et al. Novel amine-functionalized iron trimesates with enhanced peroxidase-like activity and their applications for the fluorescent assay of choline and acetylcholine[J]. Biosensors & Bioelectronics,2017:161−168.





 下载:
下载:
 下载:
下载:
