Study of the Removal Chlorpyrifos in Apples and the Degradation Pathway
-
摘要: 目的:通过研究不同条件下的酸性电解水对苹果表面毒死蜱的降解效果以及分析毒死蜱的降解途径,为苹果生产加工行业提供理论支持。方法:使用毒死蜱模拟污染苹果表面,在不同有效氯浓度(10、50、100 mg/L)和pH(pH为2.80和5.80)的酸性电解水条件下,采取浸泡处理或振荡清洗苹果的清洗方法,用气相色谱和气质联用方法测定毒死蜱残留和降解产物。结果:通过强酸性电解水降解苹果表面的毒死蜱实验,发现其降解效率与反应时间、有效氯浓度有直接关系,随着反应时间的延长或有效氯浓度的增加,降解效率也增加。当有效氯浓度达到50 mg/L时,浸泡15 min会降解55%以上的毒死蜱残留,并且与对照组自来水浸泡有极显著差异(P<0.01)。当有效氯浓度为100 mg/L时对毒死蜱的降解率超过了70%。在相同条件下强酸性电解水与微酸性电解水在降解毒死蜱的效果上无显著差异(P>0.05),并且浸泡处理和振荡处理对实验结果没有显著影响(P>0.05)。酸性电解水处理对苹果主要品质指标没有显著影响(P>0.05)。经GC-MS分析,毒死蜱被强酸性电解水降解后,在降解产物中发现毒死蜱氧化物(CPO)和3, 5, 6-三氯吡啶-2-醇(TCP)。其可能的降解途径为毒死蜱→CPO→TCP→小分子有机物→无机物。结论:该研究结果对苹果加工产业在消除农药残留方面提供一种新方法。Abstract: Objective: Through experiments and analysis of the degradation effect of chlorpyrifos on the surface of apples by acidic electrolyzed oxidizing water (EOW) under different conditions, a degradation pathway of chlorpyrifos was proposed to provide theoretical support for apple producing and processing industries. Methods: The specific experimental method used in this research was to use chlorpyrifos to simulate the pollution of the surface of apples at first, then to degrade the chlorpyrifos by soaking and shaking the apples in EOW with different ACC (10, 50, 100 mg/L) and pH (2.80, 5.80). The experiment used gas chromatography and GC-MS to analyze the residual amount of chlorpyrifos and degradation pathway. Results: The experimental results showed that the degradation efficiency of chlorpyrifos on the surface of apples was directly related to the reaction time and the concentration of available chlorine (ACC) when it was treated by strong acid electrolyzed oxidizing water (AcEW). As reaction time increased or the ACC increased, the degradation efficiency also increased. When the available chlorine concentration reached 50 mg/L with the immersion time reached 15 min, the degradation rate of chlorpyrifos reached more than 55%, which significantly differed with the control group in which apple was immersed in tap water (P<0.01). When the ACC was 100 mg/L, the degradation rate of chlorpyrifos exceeds 70%. Under same conditions, there was no significant difference between the AcEW and the slightly acidic electrolyzed water (SAEW) in the degradation effect of chlorpyrifos (P>0.05), and there was no significant difference between the immersion treatment and shaking treatment as it showed in experimental results (P>0.05). The surface treated with EOW had no effect on the main quality indicators of the apple itself (P>0.05). According to GC-MS analysis, the degradation products produced by the degradation of chlorpyrifosbys AcEW included chlorpyrifos oxide (CPO) and 3, 5, 6-trichloropyridin-2-ol (TCP). The possible degradation pathway, as we propose, is chlorpyrifos→CPO→TCP→small molecule organic matter→inorganic matter. Conclusion: This results may provide a new method for the apple processing industries in eliminating pesticide residues.
-
Keywords:
- electrolyzed oxidizing water /
- chlorpyrifos /
- apples /
- degradation /
- degradation pathway /
- GS-MS
-
苹果是世界四大水果之一,中国已成为世界最大的苹果生产国和消费国,也是苹果产品出口大国。2019年中国苹果园面积为197.81万公顷,苹果产量达到4242.54万吨[1]。为了保证产量和质量,不可避免地会使用大量的农药来控制病虫害,这往往会诱发苹果中的农药残留,从而增加对人类健康的潜在危害。
毒死蜱(Chlorpyrifos,CP)是一种硫代磷酸酯类广谱性杀虫剂[2],具有触杀和胃毒的作用[3],是果树生产上少数允许使用的有机磷农药之一[4],广泛应用于苹果种植过程中[5]。尽管毒死蜱在农业上对控制虫害有利,但在食品和环境中暴露毒死蜱残留物仍引起健康问题。越来越多的证据表明毒死蜱和其他有机磷对儿童具有神经毒性[6-8]。例如,Bouchard等[6]进行了一项7岁儿童出生队列研究(n=329),报告称与对照组相比接触高水平毒死蜱的儿童智商较低。在国内外,经常在苹果或其它果蔬中发生毒死蜱检出和超标问题[9-10]。因此,探索有效、可行、低成本的降解果蔬中农药残留方法成为实际生产中亟待解决的问题。
大多数蔬菜和水果在收获后通常用清水冲洗,以去除表面的污垢,在食用前通常要再洗一遍。清洗是大多数加工方法中的第一步,也是去除蔬菜和水果中农药残留研究最多的一步。近几年,酸性电解水(Electrolyzed oxidizing water, EOW)作为一种新型消毒剂已广泛应用于农业、牙科、医疗以及食品工业上[11]。EOW一般分为强酸性电解水(Strong acidic electrolyzed water,AcEW, pH<3.0)和微酸性电解水(Slightly acidic electrolyzed water,SAEW,pH为5.0~6.5)。EOW因容易制备、生产成本低、对人体和环境无害等优点[12],在消除降解果蔬农药残留领域,具有广阔的应用前景。尽管大量的研究结果证实了EOW具有降解农药的效果[13-14],但对苹果中毒死蜱的降解实验及降解产物分析未见报道。因此,本文使用EOW清洗处理苹果,研究了毒死蜱的降解效果及对其品质的影响,并分析了毒死蜱的降解产物和途径,为苹果加工产业提供消除农药残留的新方法。
1. 材料与方法
1.1 材料与仪器
红富士(Malus pumila Mill)苹果 摘自北京市海淀区聂各庄果园,挑选新鲜饱满, 成熟度和大小均匀, 无病虫害, 无机械损伤的苹果作为实验材料;毒死蜱 40%,惠州市中讯化工有限公司;毒死蜱标准品 1.0 mg/mL,中国计量科学研究院;乙腈、甲醇、二氯甲烷、丙酮 分析纯,DIKMA公司。
CE-7001强酸性电解水发生装置 广州赛爱环境保护技术开发有限公司;微酸性电解水装置 实验室自制设备;GC/MS-QP2010气质联用色谱仪 日本岛津公司;CNWBOND HC-C18固相萃取柱(500 mg/3mL) 德国CNW科技公司;HP-5MSUI色谱柱 美国惠普公司;Agilent 6890N气相色谱仪 美国安捷伦科技有限公司;Thermo Orion 5 star型pH/电导率/ORP综合测试仪 美国Thermo 公司;RE-52AA 旋转蒸发器 上海振捷实验设备有限公司;PAL-1糖度计 日本Atago公司;794 Basic Titrino酸碱电位滴定仪 瑞士Metrohm公司。
1.2 实验方法
1.2.1 EOW的制备
EOW的制备方法参照乌云达来等[13]的方法,稍作改进。在不同发生条件下从电解水发生器产生的强酸性电解水(AcEW)和微酸性电解水(SAEW),使用稀HCl调节pH达到所需pH,通过蒸馏水稀释方法获得实验所需的有效氯浓度(Available Chlorine Concentration,ACC)。EOW的理化指标如表1所示。
表 1 不同EOW的理化指标Table 1. Physical and chemical indicators of different EOWEOW ACC(mg/L) pH AcEW 10 2.80 50 2.80 100 2.80 SAEW 50 5.80 100 5.80 1.2.2 苹果样品前处理
实验前将苹果浸泡在浓度为100 mg/L 的毒死蜱溶液中, 充分浸泡2 h, 捞出后在 25 ℃的室温下晾干后备用。每次实验(重复)使用4个苹果,每颗苹果约90 g。
1.2.3 EOW降解苹果表面毒死蜱残留的研究
1.2.3.1 不同ACC的AcEW对苹果表面毒死蜱的降解效果影响
为了研究不同ACC的AcEW对苹果表面毒死蜱的降解效果的影响,设计了pH相同(pH 2.80),而ACC不同的AcEW及自来水进行了浸泡实验。将3.0 L AcEW倒入体积为6 L的塑料圆桶内,放入4只苹果,用不锈钢网压住苹果,保证苹果完全浸入水里;在室温环境(23±1)℃下静置浸泡处理15 min。处理结束后取出苹果,切碎,匀浆,保存在−40 ℃,然后提取、净化、GC测定其农药含量。实验分五个处理,每个处理设3个重复:无浸泡处理;自来水处理;AcEW处理:ACC 10 mg/L;AcEW处理:ACC 50 mg/L;AcEW处理:ACC 100 mg/L。降解效果以农药残留率(%)或农药降解率(%)表示。
1.2.3.2 AcEW的处理时间对苹果表面毒死蜱的降解效果影响
选择ACC为50 mg/L、pH为2.80的AcEW,取3.0 L倒入6 L塑料圆桶内,放入4只苹果,用不锈钢网压住,从而保证苹果完全浸入水里,然后在(23±1)℃下静置浸泡指定反应时间。实验分五个处理:无浸泡处理;AcEW浸泡5 min;AcEW浸泡10 min;AcEW浸泡15 min;AcEW浸泡30 min。处理结束后取出苹果,切碎,匀浆,保存在−40 ℃,然后提取、净化、经GC测定其农药含量。
1.2.3.3 不同的清洗方法对AcEW降解苹果表面毒死蜱的影响
为了研究不同的清洗方法对AcEW降解毒死蜱效果的影响,本实验设计了不同的两种清洗方法,即静置浸泡和振荡处理。每个处理方法随机取出4只苹果,放入含有2.0 L AcEW(ACC 50 mg/L,pH 2.80)的体积为3 L的塑料盒内,盖上盖,密封。实验分两个处理,每个处理重复三次:AcEW静置浸泡15 min;AcEW振荡处理(120 r/min,15 min)。处理结束后取出苹果,切碎,匀浆,保存在-40 ℃,然后提取、净化、经GC测定其农药含量。
1.2.3.4 AcEW和SAEW的毒死蜱降解效果比较
为了比较AcEW和SAEW对毒死蜱的降解效果,实验设计了ACC为50 mg/L的AcEW(pH 2.80)和SAEW(pH5.80)进行浸泡处理苹果。实验取不同的EOW 3.0 L倒入10 L塑料圆桶内,放入4只苹果,用不锈钢网压住苹果,然后在(23±1)℃下静置浸泡15 min。实验分2个处理,重复3次:AcEW浸泡15 min;SAEW浸泡15 min。处理结束后取出苹果,切碎,匀浆,保存在−40 ℃,然后提取、净化、经GC测定其农药含量。
1.2.4 EOW处理对苹果品质变化的影响
取实验用水3.0 L倒入6 L塑料圆桶内,放入苹果,用不锈钢网压住苹果,目的是保证苹果完全浸入水里,然后在(23 ± 1)℃下静置浸泡指定反应时间。实验分六个处理:无浸泡处理;自来水处理15 min;ACC为50 mg/L的AcEW(pH 2.80)浸泡15 min;ACC为50 mg/L的SAEW(pH 5.80)浸泡15 min;ACC为100 mg/L的AcEW(pH 2.80)浸泡15 min;ACC为100 mg/L的AcEW(pH 5.80)浸泡30 min。处理结束后取出苹果,分别测定其Vc、总酚、花青素、可溶性固形物以及可滴定酸含量。
1.2.5 AcEW降解毒死蜱产物分析
取5.0 mL AcEW(pH 2.80、ACC 10 mg/L),加入100 µL毒死蜱(100.0 mg/L),使溶液中的最终农药达到约2.0 mg/L,在漩涡振荡器中漩涡振荡5 s,静置至指定反应时间(1 min和10 min),然后立即加入0.5 mmol/L的硫代硫酸钠100 µL,振荡30 s,终止其降解反应。降解实验结束后经固相萃取提取、净化,通过GC-MS分析降解产物。
1.2.6 从苹果中提取与检测毒死蜱
参考农业标准NY/T 761-2008,并略作改进。将样品切碎,匀浆2 min。准确称取20.0 g样本匀浆置于200 mL具塞三角瓶中,加50.0 mL乙腈进入样品中,震荡提取20 min。过滤,将滤液收集到装有7.0 g NaCl的100 mL 具塞量瓶中,盖上塞子剧烈振荡1 min,室温下静置10 min,是乙腈和水相分层。吸取10.0 mL乙腈相溶液,40 ℃下浓缩至近干,用1.00 mL丙酮定容,用GC-FPD检测。
气相色谱检测条件为:色谱柱30 m×0.32 mm×0.25 µm,柱温100 ℃,进样口温度250 ℃,FPD检测器温度:250 ℃;升温程序:100 ℃初温保持1 min,以20.0 ℃/min的速度升至180 ℃,保持 1 min,再以10.0 ℃/min的速度升至230 ℃,然后以20.0 ℃/min的速度升至250 ℃;气流条件:载气(N2)流速:1.5 mL/min;氢气(H2)流速:80 mL/min;助燃气(Air)流速:120 mL/min; 进氧量:1 µL;进样方式:不分流进样。定量方式:峰面积法。
对毒死蜱残留率及降解率的计算方法:
1.2.7 浸泡处理液中毒死蜱的提取与检测
在毒死蜱的降解产物分析实验中,苹果浸泡液中毒死蜱的提取和净化采取固相萃取方法。参照NY/T 761-2008以及Yao等[15]的方法,并略作改进。CNWBOND HC-C18固相萃取柱(500 mg/3mL),依次用5.0 mL乙腈、5.0 mL甲醇和10.0 mL水预处理,将样品用0.1 mol/L HCl调节pH到2.0,取样品溶液过固相萃取柱,过完柱后真空干燥柱30 min,用5 mL的甲醇洗脱2次,收集洗脱液。洗脱液减压浓缩,用二氯甲烷定容至1.0 mL作为供试品溶液。
气相色谱检测条件为:色谱柱HP-5MSUI(长度30 m,直径0.25 mm,壁厚0.25 µm);载气:高纯氦气(99.999%);柱流量:1.5 mL/min,采用恒压控制模式;进样量:1.0 µL,进样方式:不分流进样;进样口温度230 ℃;色谱柱升温程序:35 ℃初温保持1 min,8.0 ℃/min的速度升至190 ℃,再2.0 ℃/min的速度升至220 ℃,20 ℃/min的速度到280 ℃,保持1.63 min。质谱条件:电子轰击离子源(EI),单四级杆质量分析器,离子源温度200 ℃,接口温度250 ℃;检测方式:全扫描,扫描质量范围40~400 m/z。
1.2.8 指标测定
AcEW样品的pH和氧化还原电位(oxidation reduction potential,ORP)采用Thermo Orion 5 star型pH/电导率/ORP综合测试仪(Thermo 公司)进行测定;ACC 采用碘量法进行测定[16];果实蔬菜维生素C含量测定采用2,6-二氯酚靛酚滴定法[17];总酚(TPC)含量的测定采用福林-肖卡法[18];花青素含量的测定采用示差法[19];苹果可溶性固形物含量采用糖度计(PAL-1, Atago, Japan)测定;可滴定酸含量采用酸碱电位滴定仪测定。
1.3 数据处理
数据处理采用SPSS 16.0 软件(Statistical Product and Service Solutions,SPSS)。每组实验重复三次,结果以平均值±标准差表示。处理间差异采用邓肯氏(Duncan’s test)多重比较,显著性水平为P<0.05。
2. 结果与分析
2.1 EOW对苹果表面毒死蜱消除效果
2.1.1 不同ACC的AcEW对毒死蜱的降解效果影响
设计了不同ACC的AcEW浸泡苹果15 min。图1表示不同的处理方法对毒死蜱的降解效果的影响。未清洗处理组(无处理组)的苹果经检测含有968 µg/kg毒死蜱;经自来水浸泡15 min后降解了17.2%的毒死蜱(残留率为82.85%);AcEW处理组中随着ACC的增加,毒死蜱的降解效果也显著提高,ACC 10 mg/L时降解了27.1%(残留率为72.9%),ACC 50 mg/L时降解了56.4%(残留率为43.6%),ACC为100 mg/L时降解了72.3%(残留率为27.7%)。方差分析表明,各处理组之间有显著性差异(P<0.05)。苹果表面的毒死蜱残留量随着AcEW的有效氯浓度的增加而降低,当ACC为50 mg/L时毒死蜱的降解效果可达极显著水平(P<0.01)。
2.1.2 AcEW的处理时间对毒死蜱的降解效果的影响
使用ACC为50 mg/L的AcEW(pH 2.80),在不同的处理时间浸泡苹果。其结果如表2所示。由表2可以看出,未浸泡处理苹果表面毒死蜱含量为(968±63)µg/kg(100%);苹果表面的毒死蜱残留随着AcEW作用时间的延长有所降低,在浸泡时间达到5 min时,降解效果可达显著水平(P<0.05)。在清洗处理30 min时AcEW的对毒死蜱的降解率达到69%以上(残留率31%以下)。实验结果说明AcEW降解苹果表面毒死蜱的过程是一个化学反应的过程,随着时间的延长,反应能够充分进行,降解效果会更好。
2.1.3 不同清洗方法对毒死蜱降解效果的影响
AcEW浸泡处理和震荡处理对降解苹果表面毒死蜱残留的效果进行了比较,实验结果如图2所示。从图2中可以看出,使用pH2.80,ACC 50 mg/L的AcEW静置浸泡和振荡处理15 min,对苹果毒死蜱消除效果差别不大,无显著性差异(P<0.05)。出现这种情况的原因,可能是由EOW的理化性质所决定的。当储藏于开口容器中,并伴随搅拌和透光时,有效氯浓度的损失最大。当储藏容器处于开口状态,氯的损失符合一级动力学规律,但光照对氯的影响并不显著[20]。在密闭避光的条件下EOW的储藏稳定性最高,而且SAEW的储藏稳定性要好于AcEW[20]。虽然震荡处理可以使EOW与苹果表面的接触更加充分,但是由于AcEW的化学性质都不是很稳定,与空气的充分接触容易使其理化性质发生改变,从而可能影响其对农药残留的降解效果。
2.1.4 不同EOW对毒死蜱降解效果的影响
研究了AcEW和SAEW对毒死蜱的降解效果,实验结果显示(图3),在相同的ACC(50 mg/L)下总体上表现出AcEW降解效果比SAEW好的趋势。毒死蜱在AcEW和SAEW的残留率分别为33.6%和36.6%,但无显著性差异(P>0.05)。
2.2 EOW处理对苹果品质变化的影响
研究了EOW浸泡处理苹果后对苹果的品质变化的影响,实验结果显示(表2),在ACC为50 mg/L的AcEW和SAEW浸泡处理苹果15 min,对苹果的Vc、总酚、花青素、可溶性固形物、可滴定酸的含量没有影响,数据之间无显著性差异(P>0.05)。在ACC为100 mg/L的AcEW分别浸泡15 min和30 min后,处理没有对苹果的Vc、总酚、花青素、可溶性固形物、可滴定酸等引起变化(表4),数据之间无显著性差异(P>0.05)。因此使用ACC为100 mg/L范围内的AcEW浸泡处理30 min以内,不会引起苹果品质变化。
表 3 不同的EOW对苹果品质变化的影响Table 3. Effects of EOW treatments on qualities of apple苹果品质参数 无处理 自来水 AcEW SAEW Vc含量(mg/100 g FW) 4.42±0.34a 4.57±0.27a 5.05±0.38a 4.64±0.26a 总酚(mg/100 g FW) 43.28±2.29a 46.71±2.14a 46.55±2.37a 46.75±0.39a 花青素(mg/100 g FW) 0.63±0.08a 0.64±0.04a 0.53±0.06a 0.56±0.08a 可溶性固形物(%) 11.9±2.7a 11.2±1.6a 12.2±1.4a 12.1±0.4a 可滴定酸(%) 0.137±0.016a 0.141±0.004a 0.138±0.019a 0.146±0.008a 表 4 AcEW的不同处理时间对苹果品质变化的影响Table 4. Effects of treatment time of AcEW on qualities of apple苹果品质参数 无处理 AcEW(15 min) AcEW(30 min) Vc含量
(mg/100 g FW)4.42±0.34a 4.65±0.13a 5.30±0.35a 总酚含量
(mg/100 g FW)43.28±2.29a 43.76±0.09a 47.00±2.74a 花青素含量
(mg/100 g FW)0.63±0.08a 0.46±0.07a 0.50±0.12a 可溶性固形物含量(%) 11.9±2.7a 13.3±2.3a 11.7±1.3a 可滴定酸含量(%) 0.137±0.016a 0.157±0.005a 0.140±0.006a 2.3 毒死蜱在EOW中的降解产物分析
使用AcEW(pH2.8、ACC 10 mg/L)对初始浓度为2 mg/L的毒死蜱进行了降解实验,并在反应时间为1 min和10 min时取样,进行GC-MS分析。在反应时间1 min时候,在总离子流图(Total ion chromatogram, 简称TIC)中除了毒死蜱(Chlorpyrifos; 简称CP),还发现了降解产物毒死蜱氧化物(Chlorpyrifosoxon; Phosphoric acid, diethyl 3,5,6-trichloro-2-pyridyl ester; 简称CPO)和3,5,6-三氯吡啶-2-醇(3,5,6-trichloro-2-pyridinol; 简称TCP)。从图4看出,TCP的保留时间为17.360 min,CPO的保留时间26.641 min,CP的保留时间为26.897 min。图5、图6、图7分别表示CP、TCP、CPO的质谱图和NIST 05质谱库检索结果(匹配度>90%)。
在反应时间为10 min时,总离子流图里没有发现毒死蜱,而继续发现了TCP和CPO(图8)。TCP和CPO的保留时间分别为17.347 min和26.599 min,经NIST 05 库验证确定为TCP和CPO(匹配度>90%)。从图4和图8中可以看出,毒死蜱在通过pH2.8、ACC 10 mg/L的AcEW降解后,其反应时间1 min时还有毒死蜱的色谱峰,但反应时间10 min时,毒死蜱全部已降解;而降解产物TCP和CPO的色谱峰高度在10 min时明显高于1 min,说明降解率随着时间的延长而增加。
关于毒死蜱在各种降解方法中产生的降解产物TCP和CPO的报道很多。其中,Wu等[20]在研究毒死蜱在次氯酸盐里的降解规律时,发现TCP和CPO是毒死蜱的主要降解产物。Zhang等[21]在使用超声波处理苹果浓缩汁里的毒死蜱时也认为毒死蜱的主要降解产物是CPO。张庆芳等[22]使用γ射线辐射毒死蜱研究其辐射效果及产物分析,毒死蜱经辐射处理后发现4种降解产物,其中就有TCP和CPO,TCP也是毒死蜱环境微生物降解产物[23]。因此可以认为,TCP和CPO是毒死蜱氧化和水解过程中常有的中间产物,本实验的结果也证明了这一点。
农药的降解过程是很复杂的化学反应过程,本实验的总离子流图里发现了很多降解产物,但某些成分因无法确定其化学结构,未能在本论文里进行详细讨论。有些降解产物可能在提取过程中因不易溶于提取溶剂或在其它提取过程中被流失,从而在质谱分析中可能会出现应值较低或没有相应。
2.4 AcEW降解毒死蜱降解途径分析
在本研究中,AcEW降解毒死蜱后发现了降解产物CPO和TCP。AcEW的主要有效成分为HOCl,HOCl具有很强的氧化性和亲电子性质[24-25]。
光催化降解有机磷农药过程中·OH攻击有机磷农药的P=S键而把原来的P=S键转换成P=O键,这是光催化降解有机磷农药的一个反应特性[26]。Mahmod等[27]在纳米材料光催化降解毒死蜱的研究中认为其降解产物CPO和TCP是由·OH、-O2·引起的。在AcEW降解农药是个复杂的化学反应过程,作者认为pH2.8的低pH值下毒死蜱降解成CPO和TCP可能与HOCl和·OH共同参与的结果。如下为毒死蜱在AcEW中降解途径的假设(图9)。
从毒死蜱到CPO,可能有两种途径;一是从(1)→(2)→(4)→(5),即HOCl攻击(1)的P=S键,-H加到S上,-OCl加到P上,然后产生中间产物(4),中间产物(4)丢失S而产生产物(5)。第二种可能途径是从(1)→(3)→(4)→(5),即·OH攻击(1)的p=S键,-OH加到P上,S被活化,产生中间产物(3),中间产物(3)进一步脱氢,转换为中间产物(4),中间产物(4)脱硫产生产物(5)。
从CPO到TCP,·OH攻击(5)的-P=O旁边的P-O键,导致产生产物(6)和含有OH-P=S结构的产物(7);或者·OH攻击(5)的-P=O旁边的P-O键,导致产生产物(6)和含有H-P=S结构的产物(8)。
从降解产物(6)、(7)、(8)在HOCl和·OH的作用下进一步降解成更小的小分子物质,最终降解成CO2、
3. 结论
采用模拟污染苹果方法,制备表面含有毒死蜱的苹果样品。通过强酸性电解水降解苹果表面的毒死蜱实验,发现其降解效率与反应时间、有效氯浓度有直接关系,随着反应时间的延长或有效氯浓度的增加,降解效率也增加。当有效氯浓度达到50 mg/L时,浸泡15 min会降解55%以上的毒死蜱残留,并且与对照组自来水浸泡有极显著差异(P<0.01)。当有效氯浓度为100 mg/L时对毒死蜱的降解率超过了70%。在相同条件下强酸性电解与水微酸性电解水在降解毒死蜱的效果上无显著差异,并且振荡处理和浸泡处理对实验结果没有明显影响。使用ACC为100 mg/L范围内的AcEW浸泡处理30 min以内,不会引起苹果品质变化。
经GC-MS分析,毒死蜱被强酸性电解水降解后,在降解产物中发现3,5,6-三氯吡啶-2-醇(TCP)和毒死蜱氧化物(CPO)。其可能的降解途径认为是毒死蜱被HOCl和·OH共同作用后,毒死蜱→毒死蜱氧化物→3,5,6-三氯吡啶-2-醇→小分子有机物→无机物。本研究证明通过酸性电解水浸泡清洗苹果能够有效消除苹果表面的毒死蜱残留,为苹果种植及加工产业提供参考。
-
表 1 不同EOW的理化指标
Table 1 Physical and chemical indicators of different EOW
EOW ACC(mg/L) pH AcEW 10 2.80 50 2.80 100 2.80 SAEW 50 5.80 100 5.80 表 2 AcEW浸泡后的苹果毒死蜱农药残留
Table 2 The residues chlorpyrifos in apple after AcEW treatment
表 3 不同的EOW对苹果品质变化的影响
Table 3 Effects of EOW treatments on qualities of apple
苹果品质参数 无处理 自来水 AcEW SAEW Vc含量(mg/100 g FW) 4.42±0.34a 4.57±0.27a 5.05±0.38a 4.64±0.26a 总酚(mg/100 g FW) 43.28±2.29a 46.71±2.14a 46.55±2.37a 46.75±0.39a 花青素(mg/100 g FW) 0.63±0.08a 0.64±0.04a 0.53±0.06a 0.56±0.08a 可溶性固形物(%) 11.9±2.7a 11.2±1.6a 12.2±1.4a 12.1±0.4a 可滴定酸(%) 0.137±0.016a 0.141±0.004a 0.138±0.019a 0.146±0.008a 表 4 AcEW的不同处理时间对苹果品质变化的影响
Table 4 Effects of treatment time of AcEW on qualities of apple
苹果品质参数 无处理 AcEW(15 min) AcEW(30 min) Vc含量
(mg/100 g FW)4.42±0.34a 4.65±0.13a 5.30±0.35a 总酚含量
(mg/100 g FW)43.28±2.29a 43.76±0.09a 47.00±2.74a 花青素含量
(mg/100 g FW)0.63±0.08a 0.46±0.07a 0.50±0.12a 可溶性固形物含量(%) 11.9±2.7a 13.3±2.3a 11.7±1.3a 可滴定酸含量(%) 0.137±0.016a 0.157±0.005a 0.140±0.006a -
[1] 中华人民共和国国家统计局[EB/OL]. (2021−04−03). https: //data.stats.gov.cn/easyquery.htm?cn=C01. National bureau of statistics of china[EB/OL]. (2021−04−03). https: //data.stats.gov.cn/easyquery.htm?cn=C01.
[2] 刘腾飞, 董明辉, 杨代凤, 等. 毒死蜱在茶叶上的残留消解动态与使用安全性[J]. 食品安全质量检测学报,2017,8(4):1383−1388. [LIU TengFei, DONG MingHui, YANG DaiFeng, et al. Residual degradation dynamics and safety of chlorpyrifos used in tea[J]. Journal of Food and Quality,2017,8(4):1383−1388. [3] 姜莉莉, 武玉国. 毒死蜱环境安全性进展[J]. 农药科学与管理,2014,35(1):29−34. [Jiang Lili, Wu Yuguo. Research progress on environmental safety of chlorpyrifos[J]. Pesticide Science and Administration,2014,35(1):29−34. doi: 10.3969/j.issn.1002-5480.2014.01.008 [4] 吴静娜, 杨秀娟, 韦璐阳, 等. 覆膜栽培方式下毒死蜱、丙溴磷和三唑磷在金桔和土壤中的消解动态[J]. 西南农业学报,2018,31(9):1845−1850. [WU Jingna, YANG Xiujuan, WEI Luyang, et al. Degradation of chlorpyrifos, profenofos and triazophosin plastic-film mulching kumquat and soil[J]. Southwest China Journal of Agricultural Sciences,2018,31(9):1845−1850. [5] J Hoa, R Rosserb, M Hasania, et al. Degradation of chlorpyrifos and inactivation of Escherichia coli O157: H7 and Aspergillus niger on apples using an advanced oxidation process[J]. Food Control,2020,109:106−920.
[6] Bouchard M F, Chevrier J, Harley Kim G, et al. Prenatalexposure to organophosphate pesticides and IQ in 7-year-old children[J]. Environmental Health Perspectives,2011,119(8):1189−1195. doi: 10.1289/ehp.1003185
[7] Rauh VA, Perera FP, Horton M K, et al. Brain anomalies in children exposed prenatally to a common organophosphate pesticide[J]. Proceedings of the National Academy of Sciences,2012,109(20):7871−7876. doi: 10.1073/pnas.1203396109
[8] Trasande L. When enough data are not enough to enact policy: The failure to banchlorpyrifos[J]. PLoS Biology,2017,15(12):e2003671. doi: 10.1371/journal.pbio.2003671
[9] 管鹏, 陈文龙. 2016-2018年贵州省宁县蔬菜水果20种农药残留状况分析[J]. 植物医生,2020,33(5):55−59. [GUAN Peng, CHEN Wenlong. Analysis of 20 pesticide residues in vegetables an fruits in zhenning county of Guizhouprovine from 2016 to 2018[J]. Plant Doctor,2020,33(5):55−59. [10] El Hawari K, MokhSamia, AI Iskandarani, et al. Pesticide residues in Lebanese apples and health risk assessment[J]. Food Addittives & Contaminants. Part B Surveillance,2019,12:81−89.
[11] Antonio I, Annamaria M, Antony S, et al. Electrolyzed water as a potential agentfor controlling postharvest decay of fruitsand vegetables[M]. Postharvest Pathology-Next Generation Solutions to Reducing Losses and Enhancing Safety, Springer, 2021: 181−197.
[12] Ding T, Oh D H, Liu D H. Electrolyzed water in food fundamentals and application[M]. Hangzhou: Zhejiang University Press, Springer, 2019: 1−2.
[13] 乌云达来, 梁铎, 郝建雄, 等. 强酸性电解水降解对硫磷动力学模型及降解产物[J]. 食品工业科技,2018,39(12):63−68. [WUYUN Dalai, LIANG Duo, HAO Jianxiong, et al. Kinetic model and pathway of parathion degraded by electrolyzed oxidizing water[J]. Science and Technology of Food Industry,2018,39(12):63−68. [14] Wang J, Han R. Removal of pesticide on food by electrolyzed water. In: Electrolyzed water in food: fundamentals and applications[M]. Springer, Singapore, 2019: 39−65.
[15] Yao J J, Gao N Y, Deng Y, et al. Sonolytic degradation of parathion and the formation of byproducts[J]. Ultrasonics Sonochemistry,2010,17:802−809. doi: 10.1016/j.ultsonch.2010.01.016
[16] 张铁垣. 化验员手册(第2版)[M]. 北京: 中国电力出版社, 1996: 133−136. ZHANG Tieheng. Laboratory technician manual (2rd)[M]. Beijing: China Electric Power Press, 1996: 133−136.
[17] 曹健康, 姜微波, 赵玉梅. 果蔬采后生理生化实验指导[M]. 北京: 中国轻工业出版社, 2007: 34−37. CAO Jiankang, JIANG Weibo, ZHAO Yumei. Physiological and biochemical experiment guidance for fruits and vegetables after harvest[M]. Beijing: China Light Industry Press, 2007: 34−37.
[18] 田树革, 魏玉龙, 刘宏炳. Folin-Ciocalteu比色法测定石榴不同部位总多酚的含量[J]. 光谱实验室,2009,26(2):341−344. [TIAN Shuge, WEI Yulong, LIU Hongbing. Determination of total polyphenol in the different places of Punica granatum L by folin-ciocalteu colorimetry[J]. Chinese Journal of Spectroscopy Laboratory,2009,26(2):341−344. doi: 10.3969/j.issn.1004-8138.2009.02.045 [19] 杨兆艳. pH 示差法测定桑椹红色素中花青素含量的研究[J]. 食品科技,2007,32(4):201−203. [YANG Zhaoyan. Anthocyanin content in mulberry red pigment bypH- differential spectrophotometry[J]. Food Science and Technology,2007,32(4):201−203. doi: 10.3969/j.issn.1005-9989.2007.04.060 [20] Wu J, Laird D A. Abiotic transformation of chlorpyrifos to chlorpyrifosoxon in chlorination water[J]. Environmental Toxicology and Chemistry,2003,22:261−264. doi: 10.1002/etc.5620220204
[21] Zhang Y Y, Xiao Z, Chen F, et al. Degradation behavior and products of malathion and chlorpyrifos spiked in apple juice by ultrasonic treatment[J]. Ultrasonics Sonochemistry,2010,17:72−77. doi: 10.1016/j.ultsonch.2009.06.003
[22] 张庆芳, 王锋, 哈益明. 毒死蜱和氯氰菊酯的辐射降解及产物特性研究[J]. 中国农业科学,2010,43(5):1041−1049. [ZHANG Qingfang, WANG Feng, HA Yiming. Research on irradiation degradation and products characteristics of chlorpyrifos and cypermethrin[J]. Scientia Agricultura Sinica,2010,43(5):1041−1049. doi: 10.3864/j.issn.0578-1752.2010.05.020 [23] Y H Huang, W P Zhang, S M Pang, et al. Insights into the microbial degradation and catalytic mechanisms of chlorpyrifos[J]. Enviromental Research,2020,194:110660.
[24] 胡建英, 谢国红, 相泽贵子. 4-壬基酚在氯消毒过程中的氧化途径[J]. 环境化学,2002:254−257. [HU Jianying, XIE Guohong, AizawaTakako. Aqueous chlorination pathways of 4-nonylphenol[J]. Enviromental Chemistry,2002:254−257. doi: 10.3321/j.issn:0254-6108.2002.03.009 [25] White G C. Handbook of chlorination and alternative disinfectant, 3rd[M]. Van Nostrand-Reinhold Publishers, New York, NY. USA. 1992: 184−191.
[26] Devi L G, Murthy B N, Kumar S G. Photocatalytic activity of V5+, Mo6+and Th4+ doped polycrystalline TiO2 for the degradation under UV/solar light[J]. Journal of Molecular Catalysis A: Chemical,2009,308:174−181. doi: 10.1016/j.molcata.2009.04.007
[27] Mahmod S, Mona G, Ibrahim, et al. Innovative photocatalytic reactor for the degradation of chlorpyrifos using acoated composite of ZrV2O7 and graphenenano-platelets[J]. Chemical Engineering Journal, 2020: 395: 124974.





 下载:
下载:
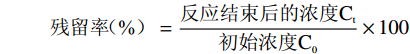
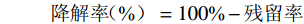










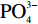
 下载:
下载:
