Protective Effect of Caffeic Acid on CCl4-Induced Injury of BRL Hepatocyte
-
摘要: 采用体外四氯化碳(carbon tetrachloride,CCl4)诱导BRL大鼠肝细胞损伤模型,研究咖啡酸(caffeic acid,CA)对CCl4诱导BRL大鼠肝细胞损伤的保护作用。实验分为对照组、CCl4模型组(100 mmol/L CCl4 损伤3 h)和CA干预组(含0.2、0.4和0.8 mg/mL CA的DMEM溶液预处理4 h,再行CCl4暴露3 h),采用全自动生化分析仪检测天冬氨酸氨基转移酶(aspartate aminotransferase,AST)、丙氨酸氨基转移酶(alanine aminotransferase,ALT)和乳酸脱氢酶(lactate dehydrogenase,LDH)活力,试剂盒测定胞内活性氧(reactive oxygen species,ROS)、细胞质中细胞色素C(cytochrome C,Cyt c)和8-羟基脱氧鸟苷(8-hydroxydeoxyguanosine,8-OHdG)水平, qRT-PCR检测核因子E2相关因子2(nuclearfactor erythroid-2-related factor 2,Nrf2)、谷胱甘肽还原酶(glutathione reductase,GSR)、醌氧化还原酶1(quinine oxidoreductase,NQO1)和超氧化物歧化酶(superoxide dismutase,SOD)的表达水平。结果显示,CA对CCl4所致细胞培养液中AST、ALT和LDH活力以及胞内ROS、细胞质中Cyt c 和8-OHdG水平的异常升高均具有显著的抑制作用(P<0.05);与对照组相比,模型组细胞中Nrf2、GSR、NQO1和SOD基因的mRNA表达水平无显著差异(P>0.05),而CA干预组中各检测基因的mRNA表达水平显著升高(P<0.05),且具有剂量依赖效应。结果表明,CCl4暴露可使BRL大鼠肝细胞发生氧化应激,而CA可激活Nrf2/ARE信号通路、上调抗氧化基因的mRNA水平,从而有效抑制CCl4对肝细胞的损伤。Abstract: This work aimed to investigate protective effect of caffeic acid on CCl4-induced BRL hepatocyte injury. The experiment was divided into control group, CCl4 model group (100 mmol/L CCl4 injury for 3 hours) and CA pretreated group (pretreated with 0.2, 0.4 and 0.8 mg/mL CA in DMEM for 4 hours, followed by CCl4 exposure for 3 hours). The activities of aspartate aminotransferase (AST), alanine aminotransferase (ALT) and lactate dehydrogenase (LDH) were detected by automatic biochemical analyzer. The levels of reactive oxygen species (ROS), cytochrome C (Cyt c) and 8-hydroxydeoxyguanosine (8-OHdG) were measured by the kit. The expression levels of nuclear factor E2-related factor 2 (Nrf2), glutathione reductase (GSR), quinine oxidoreductase (NQO1) and superoxide dismutase (SOD) were detected by qRT-PCR. Significant inhibitory effects of CA were observed on the CCl4-induced elevation of AST, ALT, LDH, ROS, Cyt c and 8-OHdG in culture medium (P<0.05). Compared with the control group, no significant differences of the mRNA expression levels of Nrf2, GSR, NQO1 and SOD gene were found in the model group (P>0.05). However, the mRNA expression levels of all detected genes were significantly increased in CA-treated group compared with the control group and a dose-dependent manner was observed. In conclusion, CCl4 exposure induced oxidative stress in BRL hepatocytes and CA inhibited the CCl4-induced BRL hepatocyte damage by activating the Nrf2/ARE signaling pathway and up-regulating the mRNA levels of antioxidant genes.
-
Keywords:
- caffeic acid /
- carbon tetrachloride /
- BRL hepatocyte /
- live injury /
- oxidative stress /
- protective effect
-
肝脏是机体最主要的代谢、排泄和解毒器官,具有分泌胆汁、解毒、凝血、免疫等重要生理功能[1-3]。外环境中的药物、酒精、病毒、化学试剂等极易导致肝损伤的发生,且各种因素导致的肝损伤常伴有氧化应激、炎症反应和细胞凋亡等[4-7]。四氯化碳(carbon tetrachloride,CCl4)所致肝损伤的表现及发展与许多人类肝脏疾病类似,常被用于肝损伤的病理研究和保肝药物的开发[8]。
咖啡酸(caffeic acid,CA)广泛存在于植物中,是一种安全、无毒害的天然化合物,具有抗氧化、抗炎、抗肿瘤、抑菌、抗病毒、免疫调节等多种药理活性,在降低细菌致病力和抗药性等方面也有很高的应用价值[9-12]。已有研究表明,CA的抗氧化活性主要源于其强大的还原能力和淬灭自由基的能力,它可通过抑制肝细胞氧化应激来改善肝微循环障碍和肝细胞损伤[13-14]。氧化应激与肝损伤的病理进程密切关联,而Nrf2/ARE是重要的抗氧化应激信号通路,激活该信号通路的传导对抑制肝损伤的发展具有重要作用[15-16],但CA在CCl4肝细胞损伤模型中对抗氧化通路激活作用的研究鲜有报道。
采用CCl4诱导BRL大鼠肝细胞损伤模型,以CA进行干预,测定大鼠肝细胞的生化指标、活性氧(ROS)、细胞色素C(Cyt c)、8-羟基脱氧鸟苷(8-OHdG)水平和部分抗氧化基因的mRNA表达情况,从氧化应激和激活Nrf2/ARE信号通路的角度探讨CA对CCl4损伤BRL大鼠肝细胞的保护作用及机制,为肝损伤的靶向治疗提供分子基础。
1. 材料与方法
1.1 材料与仪器
BRL大鼠肝细胞 购自中国科学院细胞库;咖啡酸标准品(纯度≥99%) 上海阿拉丁生化科技股份有限公司;DMEM高糖培养液、胎牛血清(FBS) 美国Gibco公司;青霉素-链霉素溶液(100×)、胰酶细胞消化液、杜氏磷酸盐缓冲液(D-PBS) 上海碧云天生物技术有限公司;四氯化碳 分析纯,山东佰仟化工有限公司;活性氧(ROS)试剂盒、细胞色素C(Cyt c)和8-羟基脱氧鸟苷(8-OHdG)酶联免疫检测试剂盒 南京建成生物工程研究所;Trizol A+总RNA提取试剂盒 天根生化科技(北京)有限公司;iScript™ Select cDNA合成试剂盒、Ssoadvanced™ SYBR® Green Supermix 美国Bio-rad公司。
MDF-382E(N) 超低温冰箱 日本SANYO公司;RCO3000T-5-VBC型二氧化碳培养箱 美国REVCO公司;ClassⅡType A2生物安全柜 美国LABCONCO公司;CKX41SF 倒置显微镜、BX53倒置荧光显微镜 日本Olympus公司;SP-Max3500FL多功能荧光酶标仪 上海闪谱生物科技有限公司;7180全自动生化分析仪 日本Hitachi公司;Micro 21R台式高速冷冻离心机 美国 Thermo Fisher 公司;高通量组织研磨仪 美国MP Biomedicals公司;NP80 Touch 超微量核酸蛋白测定仪 德国Implen公司;CFX96 Touch荧光定量PCR仪 美国Bio-rad公司。
1.2 实验方法
1.2.1 细胞培养及分组
以DMEM完全培养液(10% 胎牛血清+1% 双抗)培养BRL大鼠肝细胞,选取对数生长期的细胞进行实验。实验组分为对照组、CCl4模型组(100 mmol/L CCl4损伤3 h)和CA干预组(含0.2、0.4和0.8 mg/mL CA的DMEM溶液预处理4 h,再行CCl4暴露3 h)。
1.2.2 CA对CCl4所致BRL大鼠肝细胞损伤AST、ALT和LDH活力的测定
以5×104/mL的细胞密度接种于24孔培养板,每孔500 μL,于37 ℃、5% CO2培养箱中培养24 h后,样品干预组每孔加入750 μL浓度为0.2、0.4和0.8 mg/mL 的CA溶液,对照组和模型组每孔加入等体积的完全培养液代替样品溶液。置于CO2培养箱中培养4 h后,模型组和样品干预组每孔加入CCl4 染毒液200 μL,对照组加入等体积的完全培养液,继续培养3 h。收集各组细胞培养液上清,采用全自动生化分析仪测定AST、ALT和LDH的活力。
1.2.3 CA对CCl4所致BRL大鼠肝细胞损伤ROS、Cyt c和8-OHdG水平的测定
以5×104/mL的细胞密度接种于6孔培养板,每孔2 mL,于37 ℃、5% CO2培养箱中培养24~48 h后,样品干预组每孔加入3 mL 浓度为0.2、0.4和0.8 mg/mL 的样品工作液,对照组和模型组每孔加入等体积的完全培养液代替样品溶液。于CO2培养箱中培养4 h后,模型组和CA干预组每孔加入CCl4染毒液800 μL,对照组加入等体积的完全培养液,继续培养3 h。
将ROS各处理组的其中一个培养板于倒置荧光显微镜下观察拍照,另一个细胞培养板参照ROS试剂盒说明书,收集并重悬细胞,稀释调整细胞浓度,加入DCFH-DA探针、孵育、洗涤、重悬,使用多功能荧光酶标仪测定OD值(激发波长500 nm,发射波长525 nm),结果以对照组为1(对照组OD值/对照组OD值),其他组用相对比值表示(处理组OD值/对照组OD值)。
各处理组细胞培养结束后,弃上清液,收集细胞,通过反复冻融法裂解细胞[17-18],离心取上清液。按照Cyt c和8-OHdG酶联免疫检测剂盒说明书测定OD值,结果以各组OD值与对照组OD值的相对比值表示。运用ELISAcalc软件,选择Logistic曲线(四参数)拟合模型,得Cyt c标准曲线四参数拟合方程为Y=(A−D)/[1 + (X/C)B]+D,A=1.1690,B=1.6028,C=251.7827,D=0.0387,R2=0.9983;8-OHdG标准曲线四参数拟合方程为Y=(A−D)/[1+(X/C)B]+D,A=1.1579,B=0.6719,C=10.3982,D=−0.3350,R2=0.9998。
1.2.4 损伤抗氧化基因mRNA水平检测
细胞处理同1.2.3,采用试剂盒提取不同实验组BRL大鼠肝细胞的总RNA,RNA纯度=A260/A280,范围在1.8~2.1之间说明RNA纯度较高,可以进行逆转录[19-20]。根据Bio-radiScript Select cDNA合成试剂盒说明书进行反转录,设计引物及合成(见表1)。使用Bio-radSsoadvancedTM SYBR Green Supermix试剂盒进行实时荧光定量PCR测定,程序为:95 ℃ 3 min →(95 ℃ 10 s → 60 ℃ 30 s)×40个循环。以β-actin作为内参对照,根据各基因的Ct值,按2−∆∆Ct法计算mRNA相对表达量[21-22]。
表 1 qRT-PCR 引物序列Table 1. qRT-PCR primer sequences基因 Primer名称 引物序列 (5' → 3') 产物大小(bp) β-actin ac615F GAGGGAAATCGTGCGTGAC 212 ac827R TCATGGATGCCACAGGATT Nrf2 Nr1305F AGACAAACATTCAAGCCGATTA 204 Nr1509R AGCGGCAACTTTATTCTTCC GSR G786F CGATGTCTGTGGGAAAGCA 129 G915R GCTGAAGACCACGGTAGGG NQO1 NQ452F GCAGCGGCTCCATGTACTCT 202 NQ654R CTCCTCCCAGACAGTCTCCA SOD S219F CGGTCCAGCGGATGAAGAG 174 S393R TCCACCTTTGCCCAAGTCA 1.3 数据处理
运用SPSS 17.0统计软件和ELISAcalc软件对实验数据进行处理,实验结果用平均值±标准差(
2. 结果与分析
2.1 CA对CCl4损伤BRL大鼠肝细胞培养液上清中AST、ALT和LDH活力的影响
由表2可知,CCl4模型组BRL大鼠肝细胞培养液上清中的AST、ALT和LDH活力较对照组分别升高了277.18%、99.40% 和100.82%(P<0.01)。与模型组相比,随着CA预处理浓度的升高,BRL大鼠肝细胞培养液上清中AST活力下降了19.64%~35.90%,ALT活力下降了15.02%~45.05%,LDH活力下降了14.09%~27.99%。这表明CA能够有效抑制CCl4所致的AST、ALT和LDH活力的异常升高,保护CCl4所致肝细胞损伤的发生,且随着CA浓度的提高,保护作用增强。
表 2 咖啡酸对CCl4损伤BRL大鼠肝细胞培养液上清中AST、ALT和LDH活力的影响Table 2. Effect of caffeic acid on the AST, ALT and LDH activities in the supernatant of BRL hepatocyte injured by CC14组别 浓度(mg/mL) AST(U/L) ALT(U/L) LDH(U/L) 对照组 − 5.17±0.75 1.67±0.52 81.83±2.71 CCl4模型组 − 19.50±1.05## 3.33±0.52## 164.33±2.42## 0.2 15.67±1.21 2.83±0.41 141.17±1.72 CA干预组 0.4 13.83±0.75* 2.33±0.52* 135.33±2.16* 0.8 12.50±1.05** 1.83±0.41** 118.33±2.66 ** 注:“−”表示以不含咖啡酸的完全培养液处理;与对照组相比,# P<0.05,## P<0.01;与模型组相比,* P<0.05,** P<0.01。 2.2 CA对CCl4损伤BRL大鼠肝细胞内ROS水平的影响
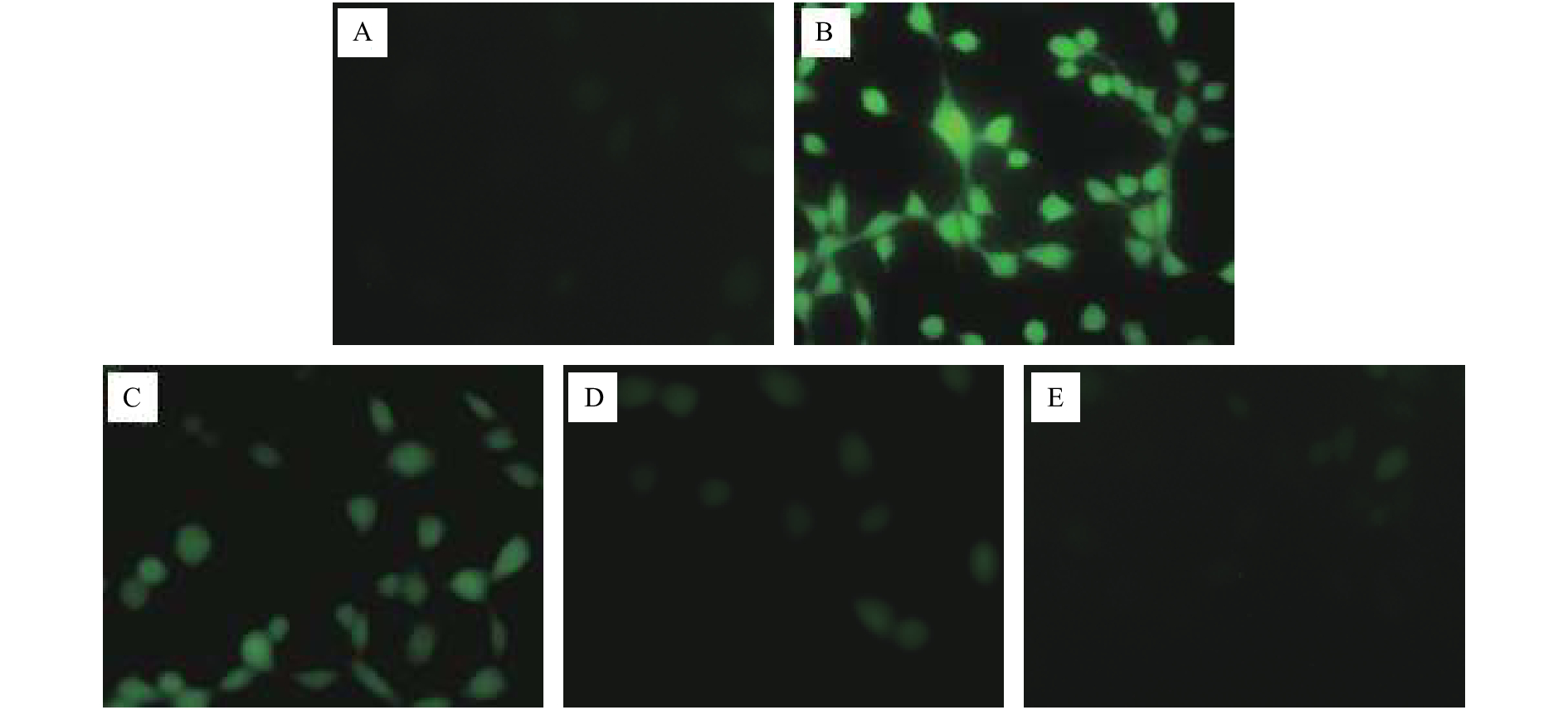
如图1所示,与对照组相比,CCl4处理组大鼠肝细胞中绿色荧光显著增强,说明细胞中ROS水平明显升高。与模型组相比,各干预组细胞中二氯荧光黄(dichlorofluorescein,DCF)荧光强度明显减弱。由图2可知,CCl4处理组大鼠肝细胞中ROS水平是对照组的132.33倍,差异具有统计学意义(P<0.01);而经CA预处理后再行CCl4暴露的细胞中ROS水平较模型组均显著降低(P<0.01),且随着CA干预浓度的升高分别降低了47.28%、93.84% 和97.75%。
2.3 CA对CCl4损伤BRL大鼠肝细胞细胞质中Cyt c水平的影响
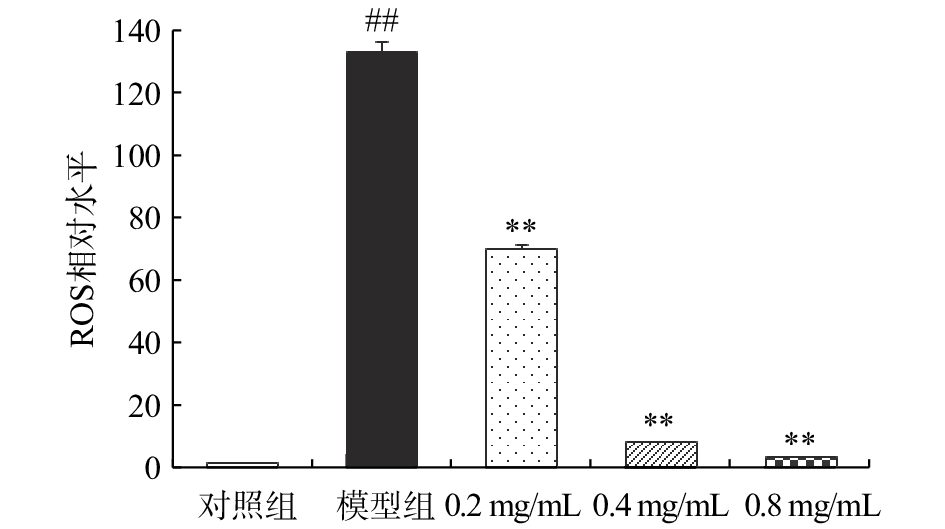
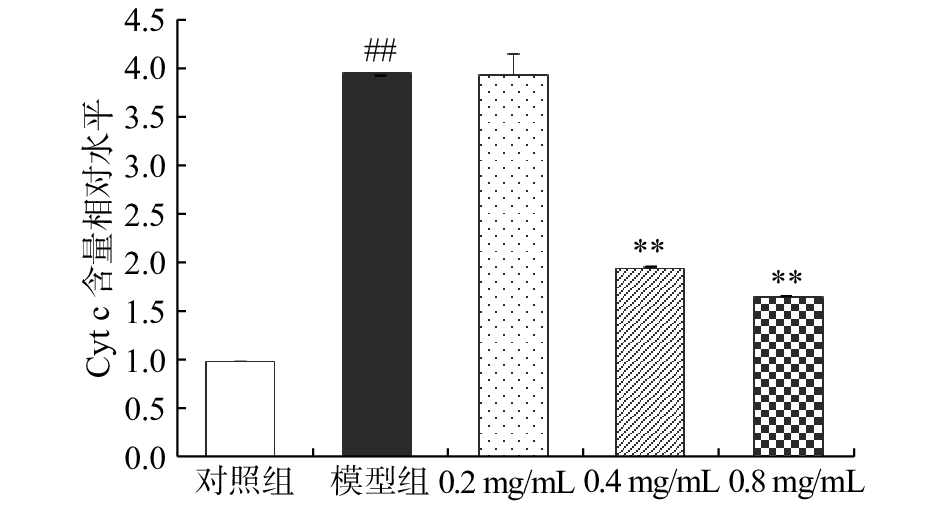
如图3所示,CCl4模型组的大鼠肝细胞细胞质中Cyt c含量是对照组的3.92倍,差异有统计学意义(P<0.01);相较于CCl4模型组,0.2 mg/mL的CA溶液干预效果不显著(P>0.05),而0.4 mg/mL和0.8 mg/mL CA干预组BRL大鼠肝细胞细胞质中Cyt c含量分别下降了50.52%和57.99%(P<0.01)。
Cyt c可直接参与介导细胞凋亡,也可通过扰乱呼吸链中的电子传递、促进ROS生成和阻断能量合成等途径在细胞凋亡过程中发挥作用[23]。正常状态下,Cyt c在线粒体的内膜和外膜之间,不会透过外膜进入到胞浆中。当细胞受到不良刺激时,ROS的过量产生可使线粒体通透性增加,同时膜电位的崩溃以及线粒体肿胀、破裂的发生都将促使Cyt c释放进入细胞质[24]。
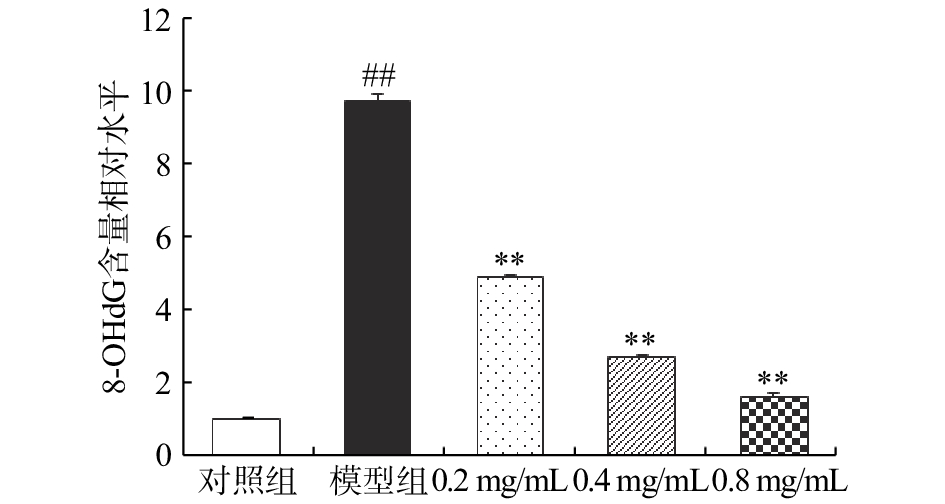
2.4 CA对CCl4损伤BRL大鼠肝细胞质中8-OHdG含量的影响
如图4所示,CCl4模型组的大鼠肝细胞中8-OHdG含量是对照组的9.64倍,差异性显著(P<0.01),表明在CCl4的损伤作用下,大鼠肝细胞发生了明显的氧化损伤。相较于CCl4模型组,0.2、0.4和0.8 mg/mL CA样品干预组的细胞中8-OHdG含量分别降低了49.79%、72.20% 和83.20%(P<0.01)。
8-OHdG与多种氧化损伤疾病具有关联性,是最常采用的氧化应激敏感指标和DNA损伤标志物[25]。正常条件下机体可对DNA氧化损伤进行修复,然而当损伤超出自身修复能力或修复机制异常时,就会导致8-OHdG堆积,进而引发致畸、致癌、致突变等损伤效应[26]。
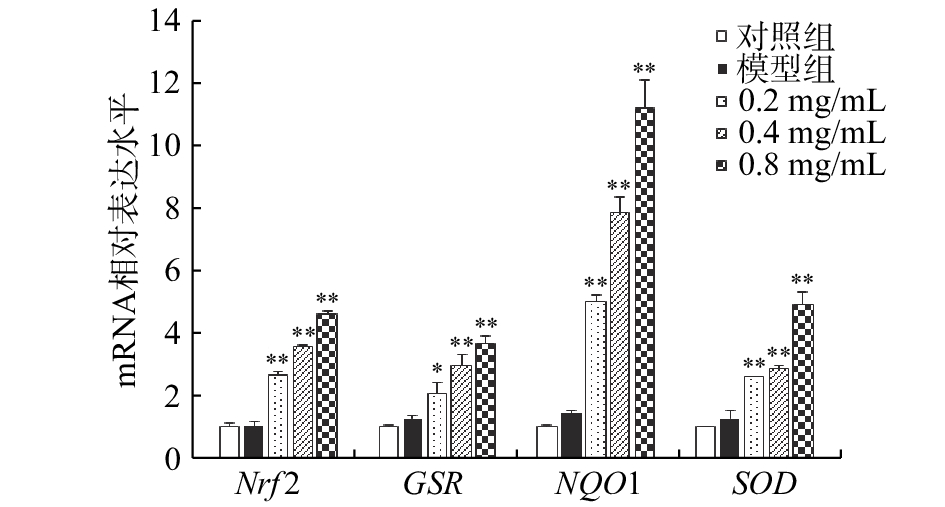
2.5 CA对CCl4损伤BRL大鼠肝细胞抗氧化基因mRNA水平的影响
如图5所示,与对照组细胞相比,CCl4模型组细胞中Nrf2、GSR、NQO1和SOD基因的mRNA表达水平无显著变化(P>0.05)。经0.2、0.4和0.8 mg/mL的CA预处理后再行CCl4暴露的各组细胞中Nrf2、GSR、NQO1和SOD的mRNA表达水平较模型组显著升高(P<0.05)。随着CA预处理浓度的升高,Nrf2
的mRNA表达水平分别为模型组的2.61、3.51倍和4.52倍;GSR的mRNA表达水平分别为模型组的1.69、2.41倍和2.98倍;NQO1 的mRNA表达水平分别为模型组的3.57、5.58倍和8.01倍;SOD的mRNA表达水平分别为模型组的2.12、2.31倍和4.04倍。且各基因的mRNA表达水平随CA预处理浓度的增加而逐渐上升。 Nrf2
是机体重要的抗氧化调节因子,活化的Nrf2能够促进抗氧化酶的表达,清除细胞内过量的ROS,调节细胞凋亡[27-28]。大量研究表明,Nrf2/ARE通路是机体抗氧化应激的重要通路,在抗炎、抗凋亡、抗细胞损伤等方面也发挥着重要作用[29]。本研究结果显示,CCl4损伤的大鼠肝细胞中Nrf2 水平并未提高,而经CA预处理后再行CCl4染毒的各组细胞中Nrf2、GSR、NQO1和SOD基因的mRNA表达水平均显著升高,表明CA对BRL大鼠肝细胞损伤的保护作用与激活Nrf2/ARE信号通路有关。 3. 讨论与结论
CCl4所致的肝细胞损伤与氧化应激密切相关,而CA可有效抑制CCl4损伤的BRL大鼠肝细胞培养液中AST、ALT和LDH活力的升高,抑制细胞内ROS、Cyt c和8-OHdG水平的异常升高,上调Nrf2、GSR、NQO1
和SOD 基因表达。其作用机制可能是通过直接增强大鼠肝细胞清除自由基的能力或上调细胞中Nrf2 的表达水平,激活Nrf2/ARE抗氧化通路,调节多个抗氧化基因的表达,在转录水平上提高细胞的抗氧化防御能力,从而减少氧化损伤。这与SU等[30-33]的研究结果一致,即酚类化合物可通过激活Nrf2/ARE信号通路启动抗氧化机制,从而提高抗氧化基因或蛋白的表达,发挥抗氧化作用。该研究结果为CA的保肝作用机制提供了一定的理论依据,但抗氧化相关蛋白表达情况以及Nrf2通路的激活机制仍需进一步研究。 -
表 1 qRT-PCR 引物序列
Table 1 qRT-PCR primer sequences
基因 Primer名称 引物序列 (5' → 3') 产物大小(bp) β-actin ac615F GAGGGAAATCGTGCGTGAC 212 ac827R TCATGGATGCCACAGGATT Nrf2 Nr1305F AGACAAACATTCAAGCCGATTA 204 Nr1509R AGCGGCAACTTTATTCTTCC GSR G786F CGATGTCTGTGGGAAAGCA 129 G915R GCTGAAGACCACGGTAGGG NQO1 NQ452F GCAGCGGCTCCATGTACTCT 202 NQ654R CTCCTCCCAGACAGTCTCCA SOD S219F CGGTCCAGCGGATGAAGAG 174 S393R TCCACCTTTGCCCAAGTCA 表 2 咖啡酸对CCl4损伤BRL大鼠肝细胞培养液上清中AST、ALT和LDH活力的影响
Table 2 Effect of caffeic acid on the AST, ALT and LDH activities in the supernatant of BRL hepatocyte injured by CC14
组别 浓度(mg/mL) AST(U/L) ALT(U/L) LDH(U/L) 对照组 − 5.17±0.75 1.67±0.52 81.83±2.71 CCl4模型组 − 19.50±1.05## 3.33±0.52## 164.33±2.42## 0.2 15.67±1.21 2.83±0.41 141.17±1.72 CA干预组 0.4 13.83±0.75* 2.33±0.52* 135.33±2.16* 0.8 12.50±1.05** 1.83±0.41** 118.33±2.66 ** 注:“−”表示以不含咖啡酸的完全培养液处理;与对照组相比,# P<0.05,## P<0.01;与模型组相比,* P<0.05,** P<0.01。 -
[1] YE D, ZHANG T B, LOU G H. Role of mir-223 in the pathophysiology of liver diseases[J]. Experimental & Molecular Medicine,2018,50(9):128.
[2] 张君, 吴凤鸣, 郭凯, 等. 水飞蓟素对于急性肝损伤修复的抗氧化作用研究[J]. 江西畜牧兽医杂志,2019,189(1):19−22. [ZHANG J, WU F M, GUO K, et al. Antioxidant effects of silymarin on the repair of acute liver injury[J]. Jiangxi Journal of Animal Husbandry & Veterinary Medicine,2019,189(1):19−22. [3] DAWID P, AGNIESZKA W, EWA H, et al. Liver failure impairs the intrahepatic elimination of interleukin-6, tumor necrosis factor-alpha, hepatocyte growth factor, and transforming growth factor-beta[J]. BioMed Research International,2015,2015:1−7.
[4] 陈美岑, 吕黄华, 农小欣, 等. 激活Nrf2/ARE信号通路减轻肝损伤的中药研究进展[J]. 世界科学技术-中医药现代化,2020,22(4):1102−1107. [CHEN M C, LV H H, NONG X X, et al. Research progress in traditional chinese medicine for activating Nrf2/ARE signaling pathway to reduce liver injury[J]. Modernization of Traditional Chinese Medicine and Materia Medica-World Science and Technology,2020,22(4):1102−1107. [5] 梁丽, 毕倩, 董金材, 等. 具有保肝作用的天然药物开发进展[J]. 生物资源,2018,40(2):148−158. [LIANG L, BI Q, DONG J C, et al. Progress on the development of natural medicines with hepatoprotective effects[J]. Biotic Resources,2018,40(2):148−158. [6] WANG Y, HAN T, XUE L M, et al. Hepatotoxicity of kaurene glycosides from Xanthium strumarium L. fruits in mice[J]. Pharmazie,2011,66(6):445−449.
[7] LUEDDE T, KAPLOWITZ N, SCHWABE R F. Cell death and cell death responses in liver disease: Mechanisms and clinical relevance[J]. Gastroenterology,2014,147(4):765−783.
[8] 梁佩诗, 周旺, 江振洲, 等. 补骨脂素通过延缓肝再生加重四氯化碳所致肝毒性的机制研究[J]. 中国中药杂志,2020,45(12):2916−2923. [LIANG P S, ZHOU W, JIANG Z Z, et al. Mechanism of psoralen in aggravating hepatotoxicity induced by CCl4 by delaying liver regeneration[J]. China Journal of Chinese Materia Medica,2020,45(12):2916−2923. [9] 兰星, 李钊文. 不同产地海金沙藤咖啡酸含量研究[J]. 大众科技,2020,22(1):29−31. [LAN X, LI Z W. Study on the content of caffeic acid in lygodiumjaponicum from different areas[J]. Popular Science & Technology,2020,22(1):29−31. [10] DZIEDZIC A, KUBINA R, KABALA-DZIK A, et al. Caffeic acid reduces the viability and migration rate of oral carcinoma cells(scc-25) exposed to low concentrations of ethanol[J]. International Journal of Molecular Sciences,2014,15(10):18725−18741.
[11] HOOSHMAND S, KUMAR A, ZHANG J Y, et al. Evidence for anti-inflammatory and antioxidative properties of dried plum polyphenols in macrophage raw 264.7 cells[J]. Food & Function,2015,6(5):1719−1725.
[12] 于福浩, 娄在祥, 王洪新等. 咖啡酸对铜绿假单胞菌群体感应的抑制及毒力因子降低的研究[J]. 食品与生物技术学报,2019,38(6):56−63. [YU F H, LOU Z X, WANG H X, et al. Effect of caffeic acid on quorum sensing and virulence factors of Pseudomonas aeruginosa[J]. Journal of Food Science and Biotechnology,2019,38(6):56−63. [13] 范金波, 蔡茜彤, 冯叙桥, 等. 咖啡酸体外抗氧化活性的研究[J]. 中国食品学报,2015,15(3):65−73. [FAN J B, CAI Q T, FENG X Q, et al. Studies on the antioxidant activity in vitro of caffeic acid[J]. Journal of Chinese Institute of Food Science and Technology,2015,15(3):65−73. [14] 韩晶岩. 咖啡酸抑制肝微循环障碍和肝损伤的作用机制[J]. 中国病理生理杂志,2015,31(10):1873. [HAN J Y. The mechanism of caffeic acid in inhibiting hepatic microcirculation disturbance and liver injury[J]. Chinese Journal of Pathophysiology,2015,31(10):1873. [15] CHEN D, TAVANA O. ARF-NRF2: A new checkpoint for oxidative stress responses?[J]. Molecular & Cellular Oncology,2018,5(3).
[16] XU D, XU M, JEONG S, et al. The role of Nrf2 in liver disease: Novel molecular mechanisms and therapeutic approaches[J]. Frontiers in Pharmacology,2019,9:1428.
[17] 曹若琼. N-乙酰半胱氨酸与抗结核药物协同功能的研究[D]. 保定: 河北大学, 2018. CAO R Q. Synergistic effects of nac and anti-TB antibiotics [D]. Baoding: Hebei University, 2018.
[18] 许炳华, 徐健, 鲍传庆, 等. 热休克凋亡和冻融裂解人胃癌细胞株抗原负载树突状细胞体外刺激细胞毒T细胞活性比较[J]. 现代肿瘤医学,2011,19(6):1093−1096. [XU B H, XU J, BAO C Q, et al. Comparison of cytotoxic T lymphocyte activity stimulated in vitro by dendritic cells loaded with heat-shocked and freeze-thawed gastric cancer cell strain[J]. Journal of Modern Oncology,2011,19(6):1093−1096. [19] 薛婵. 齐墩果酸经CoQ10/UCP2/ROS/Cyto-C通路抑制大鼠血管平滑肌细胞增殖[D]. 青岛: 青岛大学, 2017. XUE C. Oleanolic acid regulats the cells proliferation of rat artery vascular smooth muscle via CoQ10/UCP2/ROS/Cyto-C signaling pathways[D]. Qingdao: Qingdao University, 2017.
[20] 刘凤超. 抑制PIK3C3和PI3K通路对肝癌干细胞自我更新的影响及机制研究[D]. 重庆: 重庆医科大学, 2019. LIU F C. Study on the effect and mechanism of inhibition of PIK3C3 and PI3K pathways on the self-renewal of liver cancer stem cells [D]. Chongqing: Chongqing Medical University, 2019.
[21] 吕丽. 基于PI3K/Akt/NF-κb信号通路槲皮素抗动脉粥样硬化作用研究[D]. 长春: 吉林大学, 2017. LV L. Protective effects of quercetin on atherosclerosis via PI3K/Akt/NF-κb signaling pathway[D]. Changchun: Jilin University, 2017.
[22] 张倩. 金丝桃苷对Nrf2-ARE途径的影响及其对肝细胞氧化应激损伤的保护作用[D]. 重庆: 西南大学, 2014. ZHANG Q. Effect of hyperoside on Nrf2-ARE pathway and its protective effect on oxidative stress-induced L02 cell damage[D]. Chongqing: Southwest University, 2014.
[23] 龚瑜林, 王玉鑫, 赵振群, 等. 细胞色素C与Caspase-9在激素性股骨头缺血坏死中的作用[J]. 中国组织工程研究,2018,22(16):2526−2531. [GONG Y L, WANG Y X, ZHAO Z Q, et al. Roles of cytochrome C and caspase-9 in steroid-induced avascular necrosis of the femoral head[J]. Chinese Journal of Tissue Engineering Research,2018,22(16):2526−2531. [24] CHATTERJEE S, KUNDU S, BHATTACHARYYA A. Mechanism of cadmium induced apoptosis in the immunocyte[J]. Toxicology Letters,2008,177(2):83−89.
[25] 邱月, 安莉莎, 曹小芳, 等. 8-羟基脱氧鸟苷高特异性ELISA检测方法的建立及其用于妊娠期糖尿病的对比研究[J]. 中国计划生育学杂志,2019,27(7):851−853,857. [QIU Y, AN L S, CAO X F, et al. The establishment of 8 hydroxydeoxyguanosine detection by a high specificity ELISA assay, and the comparative study of its used in gestational diabetes mellitus[J]. Chinese Journal of Family Planning,2019,27(7):851−853,857. [26] 唐毅, 刘丽丽, 唐耘天. 8-羟基脱氧鸟苷在原发性肝癌中的研究现状[J]. 中国临床新医学,2013,6(3):273−276. [TANG Y, LIU L L, TANG Y T. Advances of 8-hydroxy-2’-deoxyguanosine expression in primary hepatocellular carcinoma[J]. Chinese Journal of New Clinical Medicine,2013,6(3):273−276. [27] 覃斐章, 董敏, 秦秋华等. 玉郎伞查尔酮激活Nrf2/ARE信号通路减轻缺氧/复氧所致的H9c2细胞凋亡及氧化应激损伤[J]. 天然产物研究与开发,2020,32(6):1038−1044. [TAN F Z, DONG M, QIN Q H, et al. 17-Methoxyl-7-hydroxyl-benzofuran chalcone activates Nrf2/ARE pathway to protect H9c2 cells against apoptosis and oxidative stress induced by hypoxia/reoxygenation[J]. Natural Product Research and Development,2020,32(6):1038−1044. [28] DESHMUKH P, UNNI S, KRISHNAPPA G. The Keap1-Nrf2 pathway: Promising therapeutic target to counteract ros-mediated damage in cancers and neurodegenerative diseases[J]. Biophy Rev,2017,9(1):41−56.
[29] 周秋丽, 周燕. Nrf2/ARE 信号通路在氧化应激性疾病的作用研究进展[J]. 世界最新医学信息文摘,2020,20(26):104−105. [ZHOU Q L, ZHOU Y. Research progress on the role of Nrf2/ARE signaling pathway in oxidative stress diseases[J]. World Latest Medicine Information,2020,20(26):104−105. [30] SU C, XIA X, SHI Q. Neohesperidindihydrochalcone against CCl4-induced hepatic injury through different mechanisms: The implication of free radical scavenging and Nrf2 activation[J]. Journal of Agricultural and Food Chemistry,2015,63(22):5468−5475.
[31] SHI HT, SHI A, Dong L, et al. Chlorogenic acid facilitates Nrf2-mediated antioxidant gene and protects against CCl4-induced liver injury[J]. Gastroenterology,2016,150(4):S1066.
[32] LIN Y, KUANG Y, LI K, et al. Nrf2 activators from glycyrrhizainflata and their hepatoprotective activities against CCl4-induced liver injury in mice[J]. Bioorganic and Medicinal Chemistry,2017,25(20):5522−5530.
[33] PALL M L, LEVINE S. Nrf2, a master regulator of detoxification and also antioxidant, anti-inflammatory and other cytoprotective mechanisms, is raised by health promoting factors[J]. Acta Physiologica Sinica,2015,67(1):1−18.





 下载:
下载:
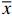
 下载:
下载:
