Optimization of Extraction Process of Flavonoids from Lycium ruthenicum Murr. by Plackett-Burnman with Response Surface Methodology and Its Antioxidation Activity
-
摘要: Plackett-Burnman(PB)联合响应面法优化黑果枸杞黄酮提取工艺并评价其抗氧化性。依次通过PB实验设计、最陡爬坡实验设计研究了5种影响因素对提取率的影响,确定了显著性影响因素及响应面中心,采用Box-Behnken(BB)实验设计优化了提取工艺;采用FRAP法及ABTS、DPPH法评价了黑果枸杞黄酮的抗氧化性,并与抗坏血酸进行了平行比较。结果表明,最佳提取工艺参数为:51%乙醇(体积分数)与原料之比为30:1(mL/g),62 ℃、240 W超声辅助提取42 min,提取率可达42.0974 mg/g(原料),与理论预测值的相对标准偏差为3.24%;FRAP法及ABTS、DPPH法均表明,黑果枸杞总黄酮还原力强于抗坏血酸,其对ABTS、DPPH自由基清除的IC50分别为0.0252、0.0272 mg/mL,均较抗坏血酸强,且二者抗氧化性均与浓度呈量效关系,为开发黑果枸杞资源、拉长其产业链提供了一定的理论基础。Abstract: To optimize the extraction conditions of flavonoids from Lycium ruthenicum by Plackett-Burnman combined with response surface methodology and evaluate its antioxidant activity. The factors with significant influence and response surface center were determined by investigating the effects of five factors on extraction rate based on Plackett-Burnman design test and the steepest ascent serach experiment. Meanwhile, the extraction technology was optimized by Box-Behnken response surface methodology. The antioxidant activity of flavonoids from Lycium ruthenicum Murr. was evaluated by using FRAP, ABTS and DPPH, which was then compared with that of ascorbic acid in parallel. Results indicated that the optimized process conditions were as follows: Ethanol volume fraction 51%, liquid to solid ratio 30:1, extraction temperature 62 ℃, extraction time 42 min, ultrasonic power 240 W, the extraction rate was up to 42.0974 mg/g(raw material) and the RSD with the theoretical value was 3.24%. The antioxidant activity tests revealed that the ferric reducing capacity of flavonoids from Lycium ruthenicum Murr. was stronger than that of ascorbic acid, the IC50of ABTS and DPPH radical scavenging activities of Lycium ruthenicum Murr. flavonoids were 0.0252 and 0.0272 mg/mL, respectively, which were higher than those of ascorbic acid, and the antioxidant activity of flavonoids followed a dose-dependent manner at all the tested concentrations. This study would provide a theoretical basis for the further development of Lycium ruthenicum Murr. resources and the extension its industrial production chain.
-
Keywords:
- Lycium ruthenicum Murr. /
- flavonoids /
- extraction process /
- optimization /
- antioxidant property
-
黑果枸杞具有抗炎[1]、增强肠道屏障功能[2]、抗氧化[3-6]、抗疲劳[7-8]、防痛风性关节炎[9]、抗动脉粥样硬化[10]、防治心脑血管疾病[11]等功效,富含花青素、多糖、多酚、黄酮等多种天然有效成分,主产于我国新疆、甘肃、青海、宁夏等地[12]。黄酮类化合物(Flavonoids)是一类植物次生代谢产物,其抗氧化性是化学合成抗氧化剂的3~5倍,天然无毒,极具开发前景[13]。李淑珍[14]以新疆产黑果枸杞叶为原料,测定了其总黄酮含量并优化了提取工艺,使总黄酮提取率达到了0.23%。段亚云等[15]、韩爱芝等[16]分别采用响应面技术优化了超声波-微波协同提取、超声辅助提取黑果枸杞叶总黄酮的工艺条件,提取率分别达到了0.997%和1.62%。古丽巴哈尔·卡吾力等[17]以新疆塔里木盆地产黑果枸杞为原料,采用水提法,通过单因素实验与响应面法优化了黑果枸杞黄酮提取工艺,总黄酮提取量达到了69.02 μg/mL。同时,相关研究发现黑果枸杞黄酮具有明显的体外抗氧化性[17-18]、降血脂功效[19-20]、抑制Hep G-2肝癌细胞增殖作用[21-22]。综上所述,关于黑果枸杞总黄酮提取及生物活性研究,多见于新疆产黑果枸杞叶中的黄酮类化合物,其它主产区数据尚缺,从黑果枸杞果实中提取黄酮化合物的报道也较为少见。
植物有效成分提取中需考虑到多个影响因素,通常的单因素实验结合响应面设计导致工作费时费力且优化工艺具有盲目性、缺乏精准性。Plackett-Burman(PB)是一种近饱和的两水平筛选试验设计方法,能用最少的试验次数快速有效地筛选出显著性影响因子[23],最陡爬坡实验可依据PB实验结果确定爬坡方向,快速聚焦响应面中心区域,Box-Behnken(BB)响应面设计采用多元线性和二次项模型拟合,可较好地体现依赖变量与非依赖变量之间的关系,对回归方程分析寻求最佳工艺参数[24]。
本研究以甘肃产黑果枸杞干果为原料,采用超声辅助提取其总黄酮,通过PB、最陡爬坡实验及BB联合实验设计对提取工艺进行优化,并对其抗氧化性进行了评价,一方面可为黑果枸杞研究填补数据空白,有利于黑果枸杞资源开发利用,另一方面为植物有效成分提取工艺研究提供可供参考的思路和方法。
1. 材料与方法
1.1 材料与仪器
黑果枸杞 2018年6月至8月产自甘肃省民勤县;抗坏血酸(批号Lot.No 1018P032)、DPPH(批号Lot.No 102D021)、ABTS(批号Lot.No 109A021) 北京索莱宝科技有限公司;氢氧化钾、无水乙醇、铁氰化钾、三氯乙酸、三氯化铁、过硫酸钾 均为分析纯。
FZ102微型植物试样粉碎机 北京中兴伟业仪器有限公司;SB-5200DTD型超声波清洗机 宁波新芝生物科技有限公司;7230G可见分光光度计 上海精密科学仪器有限公司;PHS-3C酸度计 上海仪电科学仪器股份有限公司。
1.2 实验方法
1.2.1 黑果枸杞黄酮提取方法
黑果枸杞原料经30 ℃鼓风干燥48 h、粉碎,取100目标准筛筛下物,干燥器中−5 ℃保存。准确称取0.5 g,置于装有15 mL 51%乙醇的锥形瓶中,62 ℃下提取42 min,超声功率240 W,冷却至室温后离心分离,取上层清液于25 mL容量瓶中,蒸馏水定容。
1.2.2 单因素实验
以黑果枸杞总黄酮提取率(Total flavonoids content,TFC)为评价指标,各因素考察参数及固定水平如表1所示。
表 1 单因素实验各因素考察参数及固定水平Table 1. Parameters and fixed level of each factor in single factor experiments因素 考察参数 固定水平 乙醇体积分数(%) 40、50、60、70、80、90 50 提取时间(min) 30、40、50、60、70 40 提取温度(℃) 40、50、60、70、80、90 70 液料比(mL/g) 15:1、20:1、25:1、30:1、35:1、40:1 30:1 超声功率(W) 150、180、210、240、270、300 240 1.2.3 PB实验-最陡爬坡试验
根据单因素实验结果,分别对每个影响因子取高低两水平通过Minitab17.1.0软件进行PB筛选试验设计,选取的因素及水平见表2。其次,在PB试验的基础上,分析实验所得一次多项式及各因素的正负效应,确定爬坡方向和步长,进行最陡爬坡试验设计。
表 2 PB实验设计中的因素及水平Table 2. Factors and levels tested in PB design序号 因素 低水平(−1) 高水平(+1) A 乙醇体积分数(%) 50 75 B 提取时间(min) 25 40 C 提取温度(℃) 45 70 D 液料比(mL/g) 20:1 30:1 E 超声功率(W) 160 240 1.2.4 响应面试验
根据最陡爬坡试验结果,聚焦响应面中心区域,选取显著性因素及水平,非显著性影响因素保持单因素实验中最高提取率对应值,液料比30:1 mL/g,超声功率240 W,见表3,采用Design-Expert 8.0.6软件进行响应面设计及优化分析。
表 3 响应面因素及水平Table 3. Factors and levels in response surface design因素及水平 乙醇体积分数
(A,%)提取温度
(B,℃)提取时间
(C,min)−1 30 50 25 0 50 65 40 1 70 80 55 1.2.5 总黄酮提取率测定
将提取液稀释适当倍数作为测试液。参照课题组前期研究成果中的方法测定总黄酮浓度,并根据式(1)计算黄酮提取率,提取率以mg/g(原料)表示,后面简写为mg/g[25]。
(1) 式中:ρ:总黄酮提取率,mg/g;C:测试液总黄酮浓度,μg/mL;DF:稀释倍数,50;m:原料质量,g;V:提取液体积,25 mL;1000:单位换算系数。
1.2.6 黑果枸杞黄酮抗氧化性测定
参考Pavlić等[26]与Sarikurkcy等[27]的方法并根据实验经验稍作修改。抗坏血酸与黄酮保持相同浓度和方法做平行对比。
1.2.6.1 FRAP实验
将黑果枸杞黄酮提取液稀释至浓度分别为0.01、0.02、0.04、0.06、0.08、0.10、0.15、0.20 mg/mL的样品测试液。2.5 mL磷酸缓冲液(pH=6.6)及1%铁氰化钾溶液加入1 mL测试液中,混合、50 ℃水浴中保持20 min后,常温下加入2.5 mL 10%三氯乙酸溶液,离心分离、取上层清液2.5 mL,与2.5 mL蒸馏水与0.1%氯化铁溶液混合,静置,测定700 nm的吸光度。
1.2.6.2 ABTS实验
将黑果枸杞黄酮提取液稀释至浓度分别为0.005、0.01、0.02、0.03、0.04、0.05 mg/mL的样品测试液。将7 mmol ABTS与140 mmol过硫酸钾按5 mL:88 μL混合,室温下暗处放置12~16 h,形成ABTS自由基储备液,避光保存,使用时稀释为A734 nm在0.695~0.705范围即可。测定时,取300 μL配制好的样品溶液或抗坏血酸溶液与3.7 mL ABTS自由基稀释液,混合、静置,测定734 nm的吸光度。
1.2.6.3 DPPH实验
将黑果枸杞黄酮提取液稀释至浓度分别为0.01、0.02、0.03、0.04、0.05、0.06、0.08、0.10 mg/mL的样品测试液。取0.5 mL测试液及4.0 mL DPPH无水乙醇溶液(0.15 mmol/L)于带刻度具塞试管中,用无水乙醇稀释至6 mL,混匀、避光放置一定时间,测定517 nm的吸光度。采用相同的方法分别测定用无水乙醇代替DPPH溶液和4.0 mL DPPH溶液与2.0 mL无水乙醇的混合液在517 nm的吸光度。同法评价抗坏血酸DPPH自由基清除能力。
ABTS与DPPH自由基清除率均采用式(2)计算。
(2) 式中:S为清除率;Ai为测试液吸光度;Aj为样品溶液吸光度;A0为未加样品对照液吸光度。
1.3 数据处理
采用Origin 8.0软件作图、Mintab 17.1.0软件进行Plackett-Burman实验设计与数据处理与统计差异比较、Design-Expert 8.0.6软件进行响应面设计及优化分析与统计差异比较,每组实验重复3次。
2. 结果与分析
2.1 黑果枸杞黄酮提取工艺的优化
2.1.1 单因素实验结果
由图1可以看出,50%乙醇溶液对黑果枸杞黄酮的提取率最高,推测其与黑果枸杞黄酮极性最相似;提取时间40 min时,黄酮提取率不再增加,继续延长提取时间提取率变化不大;提取温度太低不利于传质,太高则会破坏黄酮结构、降低其生物活性,70 ℃较佳;当液料比达到30:1(mL/g)时,黑果枸杞黄酮溶出量最大,再增大溶剂用量,会导致溶出杂质增多,降低总黄酮在溶出物中的比例而使其纯度下降;超声功率240 W时提取效果较佳。因此,较佳的提取工艺为:乙醇体积分数50%、提取时间40 min、提取温度70 ℃、液料比30:1 mL/g、超声功率240 W,以其为参考值进行后续实验设计。
2.1.2 PB实验设计及结果
按前述方法进行PB实验设计,各组实验提取率如表4所示。
表 4 PB实验设计及结果Table 4. PB experimental design and results实验
号A B C D E TFC
(mg/g)1 +1 +1 −1 +1 −1 27.22 2 +1 +1 −1 +1 +1 27.61 3 +1 +1 +1 −1 +1 31.17 4 −1 +1 +1 +1 −1 36.35 5 −1 −1 −1 −1 −1 34.94 6 −1 −1 +1 +1 +1 41.27 7 −1 +1 −1 −1 −1 27.63 8 −1 +1 +1 −1 +1 34.87 9 −1 −1 −1 +1 +1 35.34 10 +1 −1 +1 −1 −1 36.66 11 +1 −1 +1 +1 −1 36.51 12 +1 −1 −1 −1 +1 32.66 采用Minitab 17.1.0软件对PB实验结果分析与模型拟合,结果见表5。
表 5 PB实验方差分析Table 5. Variance analysis results of PB design方差来源 自由度 平方和 均方 F值 P值 显著性 模型 5 203.708 40.742 41.53 0.000 *** 截距 5 203.708 40.742 41.53 0.000 *** A 1 28.737 28.737 29.29 0.002 *** B 1 88.183 88.183 89.89 0.000 *** C 1 82.320 82.320 83.91 0.000 *** D 1 3.381 3.381 3.45 0.113 E 1 1.086 1.086 1.11 0.333 误差 6 5.886 0.9811 总数 11 209.595 S 0.990487 R-sq(adjusted) 0.9485 R-sq 0.9719 R-sq(predicte) 0.8877 注:*表示P<0.05;**表示P<0.01;***表示P<0.001;表9同。 由表5可知,模型的“P<0.001”、F=41.53,说明实验拟合模型达到了0.1%显著水平;从相关系数来看,R2=0.9719,R2(predicted)=0.8877,R2(adjusted)=0.9485均与1接近,说明拟合得到的一次多项式Y=31.519−1.548A−2.711B+2.619C+0.531D+0.301E与实验基本相符,可用来判别各种影响因素的显著性。表6为各因素的正负效应系数、显著性数值及影响排名。
表 6 各因素的正负效应及显著性Table 6. Positive and negative effects and significance of each factor因素 效应系数 显著性数值 影响大小排名 乙醇体积分数 −1.548 0.002 3 提取温度 2.619 0.000 2 提取时间 −2.711 0.000 1 液料比 0.531 0.113 4 超声功率 0.301 0.333 5 注:各影响大小排名以升序排列,排名序号越小,影响越大。 2.1.3 最陡爬坡试验
由表7可知,第5组提取率最高,所以以第5组实验对应的显著性影响参数为响应面中心进行响应面设计。
表 7 最陡爬坡试验设计及结果Table 7. Experimental design and result in steepest ascent method实验
号乙醇体积分数
(%)提取温度
(℃)提取时间
(min)液料比
(mL/g)超声功率
(W)TFC
(mg/g)1 70 45 60 30:1 240 34.46 2 65 50 55 30:1 240 35.63 3 60 55 50 30:1 240 36.60 4 55 60 45 30:1 240 38.57 5 50 65 40 30:1 240 40.38 6 45 70 35 30:1 240 38.01 7 40 75 30 30:1 240 36.28 2.1.4 响应面试验
依据实验结果,采用Design expert 8.0.6软件进行多元回归拟合,得到二次多项式TFC=40.98+0.17A−0.29B+0.20C+0.40AB+0.28AC−0.95BC−1.57A2−1.03B2−1.38C2,统计分析结果见表8和表9。
表 8 Box-Behnken试验设计及结果Table 8. Experimental design and results in Box-Behnken实验号 A B C D E TFC(mg/g) 1 −1 0 +1 30:1 240 37.85 2 +1 0 −1 30:1 240 37.62 3 +1 −1 0 30:1 240 38.61 4 0 +1 +1 30:1 240 37.61 5 0 +1 −1 30:1 240 39.02 6 −1 +1 0 30:1 240 37.32 7 0 0 0 30:1 240 41.11 8 −1 0 −1 30:1 240 38.09 9 −1 −1 0 30:1 240 38.82 10 0 0 0 30:1 240 41.31 11 0 −1 −1 30:1 240 37.62 12 +1 +1 0 30:1 240 38.73 13 0 −1 +1 30:1 240 39.99 14 +1 0 +1 30:1 240 38.51 15 0 0 0 30:1 240 40.85 16 0 0 0 30:1 240 41.05 17 0 0 0 30:1 240 40.56 表 9 Box-Behnken实验结果方差分析Table 9. ANOVA results of Box-Behnken design方差来源 平方和 自由度 均方 F值 P值 显著性 模型 31.39 9 3.49 50.50 <0.0001 *** A 0.24 1 0.24 3.50 0.1037 B 0.70 1 0.70 10.08 0.0156 * C 0.32 1 0.32 4.69 0.0670 AB 0.66 1 0.66 9.50 0.0178 * AC 0.32 1 0.32 4.62 0.0686 BC 3.57 1 3.57 51.72 0.0002 *** A2 10.43 1 10.43 151.09 <0.0001 *** B2 4.48 1 4.48 64.90 <0.0001 *** C2 8.07 1 8.07 116.82 <0.0001 *** 残差 0.48 7 0.069 失拟性 0.16 3 0.053 0.66 0.6199 纯误差 0.32 4 0.081 总差 31.87 16 R2=0.9848 R2adj=0.9653 R2pred=0.9040 由表9可知,模型F=50.50,P<0.0001,说明模型达到了0.1%显著水平,并且R2=0.9848,R2adj=0.9653,R2pred=0.9040、失拟项P=0.6199>0.05,说明模型预测性良好且失拟程度不显著,具有统计学意义。另外,各项显著性因素统计分析表明,其显著性大小顺序为:B>C>A,这与Plackett-Burnman试验分析结果一致,结论相互佐证,说明实验过程误差小,并且B,AB达到了5%显著性水平,BC,A2,B2,C2等二次项达到了0.1%显著性水平。
依据数据模拟结果,绘制3D响应面图,见图2。由图2可知,所形成的响应曲面均中心凸起四周下降,说明通过最陡爬坡实验选取的响应面中心准确,实验中选取各因素水平范围覆盖了最高提取率的工艺条件,通过模型预测的最佳提取工艺是科学合理的。
2.1.5 最优条件及验证
解析所得二次多项式,并根据仪器实际操作精确度做近似处理,得到超声辅助提取黑果枸杞黄酮的最佳工艺条件为:乙醇体积分数51%,提取温度62 ℃,提取时间42 min,液料比30:1,超声功率240 W,并进行三次验证实验,平均提取率为42.0974 mg/g,与预测值的相对标准偏差为3.24%,说明该拟合模型可靠、最佳工艺条件准确。
2.2 黑果枸杞黄酮抗氧化性
2.2.1 FRAP还原力
由图3可知,随着黑果枸杞黄酮样品与抗坏血酸浓度增大,吸光度逐渐增大,说明其还原力增强,并且黑果枸杞黄酮的还原力强于抗坏血酸,与李进等[18]报道的黑果枸杞叶黄酮还原力实验结果基本一致,但吸光度整体偏小,可能由于黑果枸杞黄酮来自不同地域的植物和植物不同部位而表现出差异,同时推测黑果枸杞黄酮是良好的电子供应者。
2.2.2 ABTS总抗氧化力
由图4可知,黑果枸杞总黄酮与抗坏血酸对ABTS+自由基的清除率均随自身浓度增大而增大,在0.05 mg/mL时,黑果枸杞黄酮与抗坏血酸的清除率分别达到96.68%和93.63%,说明黑果枸杞黄酮与抗坏血酸均具有很强的ABTS+自由基清除能力,IC50分别为0.0252 、0.0279 mg/mL,说明黑果枸杞黄酮的ABTS+自由基清除力略强于抗坏血酸。原因可能是黄酮类化合物具有多羟基,黄酮类化合物结构中的3-OH,5-OH,2、3位双键,B环中的4'-OH,3',4'邻位双羟基是抗氧化的有效基团,能与自由基反应,形成共振稳定的半醌式自由基,共振半醌式自由基的稳定性越大,黄酮类化合物的抗氧活性越强[28]。
2.2.3 DPPH自由基清除能力
稳定自由基DPPH的乙醇溶液呈紫色,在517 nm处有最大吸收,抗氧化剂具有递电子或递质子的能力,对DPPH自由基的清除作用是抗氧化剂将电子或质子传递给DPPH自由基,从而生成稳定的分子态的结果[29]。由图5可知,黑果枸杞黄酮与抗坏血酸清除DPPH自由基作用均较强,IC50分别为0.0272、0.0287 mg/mL。浓度0.01~0.06 mg/mL时,两者对DPPH自由基清除率随浓度增大急剧上升,达到0.06 mg/mL时,两者的清除率都大于90%并趋于稳定,此后清除作用增加不明显,整个过程二者对DPPH自由基的清除率无明显差异,本实验中的黄酮样品对DPPH自由基的清除能力低于古丽巴哈尔·卡吾力等[17]报道的新疆黑果枸杞黄酮,与李兆君等[30]报道的宁夏黑果枸杞黄酮清除能力基本一致。
3. 结论
本研究以甘肃产黑果枸杞为原料,采用PB实验设计联合最陡爬坡实验与BB实验设计进行黄酮提取工艺优化,最佳提取工艺条件为:以51%乙醇(体积分数)为提取剂,加入与原料比30:1(mL/g)的量,62 ℃、240 W提取42 min,提取率可达42.0974 mg/g。
同时,以抗坏血酸为阳性对照,较全面地评价了黑果枸杞黄酮的抗氧化性,得出黑果枸杞黄酮具有较强的还原力,对ABTS+自由基、DPPH自由基的清除作用表明,其IC50分别为0.0252、0.0272 mg/mL均略强于抗坏血酸的0.0279、0.0287 mg/mL,抗氧化能力与浓度正相关。实验中对抗氧化性考察的实验项目有限,本课题组会在后续研究中继续探索黑果枸杞黄酮对其它自由基的清除作用,采用HPLC或MS对提取物黄酮单体化合物进行定性定量研究。
综上所述,黑果枸杞黄酮可作为一种安全的天然抗氧化物,具有较高的应用价值和潜在经济效益,本文研究成果可为黑果枸杞开发应用、深加工、精加工提供一定的理论依据。
-
表 1 单因素实验各因素考察参数及固定水平
Table 1 Parameters and fixed level of each factor in single factor experiments
因素 考察参数 固定水平 乙醇体积分数(%) 40、50、60、70、80、90 50 提取时间(min) 30、40、50、60、70 40 提取温度(℃) 40、50、60、70、80、90 70 液料比(mL/g) 15:1、20:1、25:1、30:1、35:1、40:1 30:1 超声功率(W) 150、180、210、240、270、300 240 表 2 PB实验设计中的因素及水平
Table 2 Factors and levels tested in PB design
序号 因素 低水平(−1) 高水平(+1) A 乙醇体积分数(%) 50 75 B 提取时间(min) 25 40 C 提取温度(℃) 45 70 D 液料比(mL/g) 20:1 30:1 E 超声功率(W) 160 240 表 3 响应面因素及水平
Table 3 Factors and levels in response surface design
因素及水平 乙醇体积分数
(A,%)提取温度
(B,℃)提取时间
(C,min)−1 30 50 25 0 50 65 40 1 70 80 55 表 4 PB实验设计及结果
Table 4 PB experimental design and results
实验
号A B C D E TFC
(mg/g)1 +1 +1 −1 +1 −1 27.22 2 +1 +1 −1 +1 +1 27.61 3 +1 +1 +1 −1 +1 31.17 4 −1 +1 +1 +1 −1 36.35 5 −1 −1 −1 −1 −1 34.94 6 −1 −1 +1 +1 +1 41.27 7 −1 +1 −1 −1 −1 27.63 8 −1 +1 +1 −1 +1 34.87 9 −1 −1 −1 +1 +1 35.34 10 +1 −1 +1 −1 −1 36.66 11 +1 −1 +1 +1 −1 36.51 12 +1 −1 −1 −1 +1 32.66 表 5 PB实验方差分析
Table 5 Variance analysis results of PB design
方差来源 自由度 平方和 均方 F值 P值 显著性 模型 5 203.708 40.742 41.53 0.000 *** 截距 5 203.708 40.742 41.53 0.000 *** A 1 28.737 28.737 29.29 0.002 *** B 1 88.183 88.183 89.89 0.000 *** C 1 82.320 82.320 83.91 0.000 *** D 1 3.381 3.381 3.45 0.113 E 1 1.086 1.086 1.11 0.333 误差 6 5.886 0.9811 总数 11 209.595 S 0.990487 R-sq(adjusted) 0.9485 R-sq 0.9719 R-sq(predicte) 0.8877 注:*表示P<0.05;**表示P<0.01;***表示P<0.001;表9同。 表 6 各因素的正负效应及显著性
Table 6 Positive and negative effects and significance of each factor
因素 效应系数 显著性数值 影响大小排名 乙醇体积分数 −1.548 0.002 3 提取温度 2.619 0.000 2 提取时间 −2.711 0.000 1 液料比 0.531 0.113 4 超声功率 0.301 0.333 5 注:各影响大小排名以升序排列,排名序号越小,影响越大。 表 7 最陡爬坡试验设计及结果
Table 7 Experimental design and result in steepest ascent method
实验
号乙醇体积分数
(%)提取温度
(℃)提取时间
(min)液料比
(mL/g)超声功率
(W)TFC
(mg/g)1 70 45 60 30:1 240 34.46 2 65 50 55 30:1 240 35.63 3 60 55 50 30:1 240 36.60 4 55 60 45 30:1 240 38.57 5 50 65 40 30:1 240 40.38 6 45 70 35 30:1 240 38.01 7 40 75 30 30:1 240 36.28 表 8 Box-Behnken试验设计及结果
Table 8 Experimental design and results in Box-Behnken
实验号 A B C D E TFC(mg/g) 1 −1 0 +1 30:1 240 37.85 2 +1 0 −1 30:1 240 37.62 3 +1 −1 0 30:1 240 38.61 4 0 +1 +1 30:1 240 37.61 5 0 +1 −1 30:1 240 39.02 6 −1 +1 0 30:1 240 37.32 7 0 0 0 30:1 240 41.11 8 −1 0 −1 30:1 240 38.09 9 −1 −1 0 30:1 240 38.82 10 0 0 0 30:1 240 41.31 11 0 −1 −1 30:1 240 37.62 12 +1 +1 0 30:1 240 38.73 13 0 −1 +1 30:1 240 39.99 14 +1 0 +1 30:1 240 38.51 15 0 0 0 30:1 240 40.85 16 0 0 0 30:1 240 41.05 17 0 0 0 30:1 240 40.56 表 9 Box-Behnken实验结果方差分析
Table 9 ANOVA results of Box-Behnken design
方差来源 平方和 自由度 均方 F值 P值 显著性 模型 31.39 9 3.49 50.50 <0.0001 *** A 0.24 1 0.24 3.50 0.1037 B 0.70 1 0.70 10.08 0.0156 * C 0.32 1 0.32 4.69 0.0670 AB 0.66 1 0.66 9.50 0.0178 * AC 0.32 1 0.32 4.62 0.0686 BC 3.57 1 3.57 51.72 0.0002 *** A2 10.43 1 10.43 151.09 <0.0001 *** B2 4.48 1 4.48 64.90 <0.0001 *** C2 8.07 1 8.07 116.82 <0.0001 *** 残差 0.48 7 0.069 失拟性 0.16 3 0.053 0.66 0.6199 纯误差 0.32 4 0.081 总差 31.87 16 R2=0.9848 R2adj=0.9653 R2pred=0.9040 -
[1] Peng Y J, Yan Y M, Wan P, et al. Gut microbiota modulation and anti-inflammatory properties of anthocyanins from the fruits of Lycium ruthenicum Murray in dextran sodium sulfate-induced colitis in mice[J]. Free Radical Biology and Medicine,2019,136:96−108. doi: 10.1016/j.freeradbiomed.2019.04.005
[2] Tian B M, Zhao J H, An W, et al. Lycium ruthenicum diet alters the gut microbiota and partially enhances gut barrier function in male C57BL/6 mice[J]. Journal of Functional Foods,2019,52:516−528. doi: 10.1016/j.jff.2018.11.034
[3] 双全, 张海霞, 卢宇, 等. 野生黑果枸杞化学成分及抗氧化活性研究[J]. 食品工业科技,2017,38(4):94−100. [Shuang Q, Zhang H X, Lu Y, et al. The research on chemical componentand antioxidant activity of wild Lycium ruthenicum[J]. Science and Technology of Food Industry,2017,38(4):94−100. [4] 张霞, 张芳, 高晓娟, 等. 不同干燥方法对黑果枸杞中活性成分含量及其抗氧化活性的影响[J]. 中国中药杂志,2017,42(20):3926−3931. [Zhang X, Zhang F, Gao X J, et al. Effects of different drying methods on content of bioactive component andantioxidant activity in Lycium ruthenicum[J]. China Journal of Chinese Materia Medica,2017,42(20):3926−3931. [5] 尹民强, 吴金龙, 王天琦, 等. 黑果枸杞抗氧化能力评价及比较研究[J]. 中国果菜,2019,39(11):52−56. [Yin M Q, Wu J L, Wang T Q, et al. Evaluation and comparative study on antioxidant capacity of Lycium ruthenicum Murr[J]. China Fruit & Vegetable,2019,39(11):52−56. [6] Zhang J T, Dong Y S, Tanzeela N, et al. Effect of superfine-grinding on the physicochemical and antioxidant properties of Lycium ruthenicum Murray powders[J]. Powder Technology,2020,372:68−75. doi: 10.1016/j.powtec.2020.05.097
[7] Ni W H, Gao T T, Wang H L, et al. Anti-fatigue activity of polysaccharides from the fruits of four Tibetan Plateau indigenous medicinal plants[J]. Journal of Ethnopharmacology,2013,150(2):529−535. doi: 10.1016/j.jep.2013.08.055
[8] 曹茸茸. 黑果枸杞抗运动疲劳作用研究[D]. 兰州: 甘肃中医药大学, 2018. Cao R R. Study on the anti-fatigue effects of Lycium ruthenium[J]. Lanzhou: Gansu University of Chinese Medicine, 2018.
[9] Zhang G, Chen S S, Zhou W, et al. Anthocyanin composition of fruit extracts from Lycium ruthenicum and their protective effect for gouty arthritis[J]. Industrial Crops and Products,2019,129:414−423. doi: 10.1016/j.indcrop.2018.12.026
[10] Luo Y, Fang J L, Yuan K, et al. Ameliorative effect of purified anthocyanin from Lycium ruthenicum on atherosclerosis in rats through synergistic modulation of the gut microbiota and NF-κB/SREBP-2 pathways[J]. Journal of Functional Foods,2019,59:223−233. doi: 10.1016/j.jff.2019.05.038
[11] 林丽, 李进, 李永洁, 等. 黑果枸杞花色苷对氧化低密度脂蛋白损伤血管内皮细胞的保护作用[J]. 中国药学杂志,2013,48(8):606−611. [Lin L, Li J, Li Y J, et al. Protective effects of Lycium ruthenicum anthocyanins on the vascular endothelial cells with oxidative injury by oxidized low-density lipoprotein in vitro[J]. Chinese Pharmaceutical Journal,2013,48(8):606−611. [12] Wang H Q, Li J N, Tao W W, et al. Lycium ruthenicum studies: Molecular biology, phytochemistry and pharmacology[J]. Food Chemistry,2018,240:759−766. doi: 10.1016/j.foodchem.2017.08.026
[13] 张媛媛, 管棣, 谢青兰, 等. 黄酮体外抗氧化作用研究[J]. 中成药,2007,29(3):342−345. [Zhang Y Y, Guan D, Xie Q L, et al. Antioxidative effect of xanthones in vitro[J]. Chinese Traditional Patent Medicine,2007,29(3):342−345. doi: 10.3969/j.issn.1001-1528.2007.03.009 [14] 李淑珍. 黑果枸杞总黄酮制备工艺优化和抗氧化、降血脂活性及成分研究[D]. 乌鲁木齐: 新疆师范大学, 2009. Li Shuzhen. Optimization preparating technology and activities of anti-oxidation, hypolipidemic and compositions of the total flavonoids from Lycium ruthenicum[D]. Wulumuqi: Xinjiang Normal University, 2009.
[15] 段亚云, 李建颖, 程瑶, 等. 响应面法优化超声波-微波协同提取黑果枸杞叶总黄酮工艺[J]. 食品研究与开发,2018,39(21):100−105. [Duan Y Y, Li J Y, Cheng Y, et al. Optimization of ultrasonic-microwave synergy extraction of total flavonoids from Lycium ruthenicum leaves by response surface methodology[J]. Food Research and Development,2018,39(21):100−105. doi: 10.3969/j.issn.1005-6521.2018.21.017 [16] 韩爱芝, 白红进, 耿会玲. 响应面法优化超声辅助提取黑果枸杞叶片总黄酮的工艺研究[J]. 西北林学院学报,2013,28(1):114−118. [Han A Z, Bai H J, Geng H L, et al. Optimization of ultrasound-assisted extraction of total flavonoids from Lycium ruthenicum leaves by response surface methodology[J]. Journal of Northwest Forestry University,2013,28(1):114−118. doi: 10.3969/j.issn.1001-7461.2013.01.22 [17] 古丽巴哈尔·卡吾力, 高晓黎, 常占瑛, 等. 黑果枸杞总黄酮提取工艺优化及抗氧化活性[J]. 江苏农业科学,2017,45(22):213−217. [Gulibahaer Kawuli, Gao X L, Chang Z Y, et al. Study on optimization of extraction process of flavonoids from Lycium ruthenicum Murr. and its antioxidation activityxidation activity[J]. Jiangsu Agricultural Sciences,2017,45(22):213−217. [18] 李进, 李淑珍, 冯文娟, 等. 黑果枸杞叶总黄酮的体外抗氧化活性研究[J]. 食品科学,2010,31(13):259−262. [Li J, Li S Z, Feng W J, et al. In vitro antioxidant and free radical scavenging activities of total flavonoids from the leaves of Lycium ruthenicum Murr[J]. Food Science,2010,31(13):259−262. [19] 李淑珍, 李进. 黑果枸杞黄酮降血脂作用[J]. 时珍国医国药,2012,23(5):1072−1074. [Li S Z, Li J. Hypolipidemic activity of the total flavonoids from Lycium ruthenicum Murr[J]. Lishizhen Medicine and Materia Medica Research,2012,23(5):1072−1074. doi: 10.3969/j.issn.1008-0805.2012.05.009 [20] 李淑珍, 李进. 黑果枸杞叶黄酮降血脂及抗氧化活性的研究[J]. 北方药学,2011,8(11):23−24. [Li S Z, Li J. Study on hypolipidemic and antioxidant activity of the total flavonoids from Lycium ruthenicum Murr J]. Journal of North Pharmacy,2011,8(11):23−24.
[21] 艾克山·吾拉木, 谭扬扬, 古丽巴哈尔·卡吾力. 黑果枸杞中总黄酮的降脂活性研究[J]. 新疆医科大学学报,2019,42(8):1063−1067. [Aikeshan Wulamu, Tan Y Y, Gulibahaer Kawuli. Study on the lipid-lowering activity of total flavonoids in Lycium ruthenicum Murr[J]. Journal of Xinjiang Medical University,2019,42(8):1063−1067. doi: 10.3969/j.issn.1009-5551.2019.08.022 [22] 艾克山·吾拉木. 黑果枸杞总黄酮分离纯化及其降脂、抗肝癌活性初步研究[D]. 乌鲁木齐: 新疆医科大学, 2020. Aikeshan Wulamu. Preliminary study on isolation and purification of total flavonoids from Lycium ruthenicum Murr. and its lipid-lowering and antihepatocarcinogenic activity[D]. Wulumuqi: Xinjiang Medical University, 2020.
[23] 唐远江, 余波, 刘镜, 等. 运用Plackett-Burnman设计和Box-Behnken-响应面法优化地榆没食子酸提取工艺[J]. 贵州农业科学,2019,47(4):131−135. [Tang Y J, Yu B, Liu J, et al. Extraction optimization of gallic acid from Sanguisorba officinalis by Plackett-Burnman design and Box-Behnken response surface methodology[J]. Guizhou Agricultural Sciences,2019,47(4):131−135. doi: 10.3969/j.issn.1001-3601.2019.04.029 [24] 管志美, 彭艳梅, 王银, 等. 基于Plackett-Burnman设计和Box-Behnken效应面法优化南宝戒毒清胶囊提取工艺[J]. 中药与临床,2018,9(5):20−24. [Guan Z M, Peng Y M, Wang Y, et al. Study on the extraction technology of Nanbaojieduqing capsule by Plackett-Burman design and Box-Behnken design-response surface methodology[J]. Pharmacy and Clinics of Chinese Materia Medica,2018,9(5):20−24. [25] 武芸, 马世荣, 王春林, 等. 大叶藜叶中总黄酮含量的测定[J]. 安徽农业科学,2015,43(34):164−165. [Wu Y, Ma S R, Wang C L, et al. Determination of total flavone in the leaf of Chenopodium hybridum L doi: 10.3969/j.issn.0517-6611.2015.34.061 J]. Journal of AnhuiAgricultural Sciences,2015,43(34):164−165. doi: 10.3969/j.issn.0517-6611.2015.34.061
[26] Pavlić B, Kaplan M, Bera O, et al. Microwave-assisted extraction of peppermint polyphenols artificial neural networks approach[J]. Food and Bioproducts Processing,2019(118):258−269.
[27] Sarikurkcy C, Tepe B, Semiz D K, et al. Evaluation of metal concentration and antioxidant activity of three edible mushrooms from Mugla, Turkey[J]. Food and Chemical Toxicology,2010(48):1230−1233.
[28] 胡春, 丁霄霖. 黄酮类化合物在不同氧化体系中的抗氧化作用研究[J]. 食品与发酵工业,1996(3):46−53. [Hu C, Ding X L. Anitoxidant effect of flavonoid in different oxidation systems[J]. Food and Ferrnentation Industries,1996(3):46−53. doi: 10.3321/j.issn:0253-990X.1996.03.009 [29] 李铉军, 崔胜云. 抗坏血酸清除DPPH自由基作用机理[J]. 食品科学,2011,32(1):86−90. [Li X J, Cui S Y. DPPH radical scavenging mechanism of ascorbic acid[J]. Food Science,2011,32(1):86−90. [30] 李兆君, 丁润梅. 宁夏枸杞与黑果枸杞总黄酮含量及抗自由基活性的比较研究[J]. 食品研究与开发,2014,35(12):39−41. [Li Z J, Ding R M. Comparative studies the content of total flavonoids and anti-free radical between Ningxia wolfberry and black wolfberry[J]. Food Research and Development,2014,35(12):39−41.





 下载:
下载:

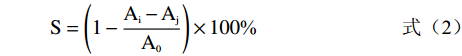





 下载:
下载:
