Optimization of Extraction Process of Total Saponins from Rubus crataegifolius Bunge. Root by Response Surface Methodology and Its Antioxidant Activity
-
摘要: 为进一步开发托盘根的功能性成分和药用价值。本研究以托盘的干燥根为试材,通过考察提取时间、乙醇体积分数、液料比等因素对托盘根总皂苷得率的影响,选用响应面法(RSM)探究托盘根总皂苷的最佳提取工艺,且研究了托盘根总皂苷提取物的体外抗氧化能力。结果表明:托盘根总皂苷的最优提取条件为:提取时间2 h,乙醇体积分数71%,液料比28:1 mL/g,在该条件下测得托盘根总皂苷的得率为3.37%,与预测值3.49%相近。托盘根总皂苷提取物对DPPH·、ABTS+·、
-
托盘(Rubus crataegifolius Bunge.)是蔷薇科悬钩子属植物,别名山楂叶悬钩子、牛迭肚,广泛分布于我国东北、华东和中南部地区[1]。托盘根和果实均为传统中药材,果实酸甜,可生食,也可制作果酱、果羹或酿酒,果实也可入药,具有补肝养肾、固精缩尿的功效。其根在民间多用治疗痛风及肝炎等病症[2-3]。托盘根包含大量酚酸类、芪类、黄酮类、鞣质、萜类、皂苷类和多糖类成分[4-6]。其中三萜类成分在悬钩子属植物中有着含量高、结构丰富的特点[7],从而成为了研究热点。Jung等[8]在托盘根中分离得到一种新的三萜皂苷,命名为crataegioside。魏忠宝等[2]在山楂叶悬钩子的根部中分离获得蔷薇酸、吐曼酸、2α-羟基齐墩果酸和乌苏酸等多种皂苷。李秋叶[9]从山楂叶悬钩子根部的有机溶剂提取物中分离鉴定了10个乌苏烷型皂苷。赵伟等[4]通过有机溶剂萃取和硅胶柱色谱等方法,从托盘根中鉴定得到多个皂苷类化合物,其中有齐墩果酸、熊果酸和蛇莓苷B。
皂苷又名皂苷素,广泛存在于高等植物和一部分海洋生物,是一类较复杂的苷类化合物[10]。皂苷类化合物有多种较强的药理活性,如抗氧化[11]、抗肥胖[12]、抗菌[13]、抗肿瘤[14-15]、肝保护[16]、抗炎[17]、免疫和降血糖等,具有一定的药理价值。较为常见提取皂苷化合物的方法有浸渍法、渗漉法、回流法、酶解法、超声和微波辅助提取法等[18]。其中热回流法有经济、简单、容易操作等优点[19]。同时,RSM被广泛应用于中药化学成分提取技术的研究,是较为常用的实验设计和优化方法之一[20]。目前,还没有关于托盘根皂苷类化合物提取工艺的相关报道,本研究基于单因素的考察,利用Box-Behnken RSM对托盘根总皂苷提取工艺进行优化,并测定托盘根提取物的体外抗氧化活性,为提高托盘根总皂苷的得率和进一步开发为天然抗氧化剂提供科学依据。
1. 材料与方法
1.1 材料与仪器
托盘根 采自吉林市外郊,经长春中医药大学药学院李勇教授鉴定为蔷薇科悬钩子属植物托盘(Rubus crataegifolius Bunge.)的干燥根;香草醛、冰醋酸:天津市科密欧化学试剂有限公司;硫酸、甲醇、无水乙醇 天津市大茂化学试剂厂;齐墩果酸、2,2’-联氨-双-[3-乙基苯并噻唑啉-6-磺酸]-二氨盐(ABTS) 美国Sigma公司;1,1-二苯基-2-三硝基苯肼(DPPH) 阿拉丁生化试剂。
FA1004N电子分析天平 上海菁海仪器有限公司;UV-2000紫外分光光度计 北京普析通用仪器厂;Spectra Max Plus 384酶标仪 美国Molecular Devices公司;DK-98-ll旋转蒸发仪 天津天泰仪器有限公司。
1.2 实验方法
1.2.1 托盘根总皂苷的提取
取适量的托盘根洗净后置于60 ℃烘箱中干燥至恒质量,干燥后的托盘根粉碎,过60目筛,称取粉末3 g,加入250 mL圆底烧瓶中,再加入乙醇,热水回流提取2次。抽滤后合并滤液。滤液浓缩、冻干,制得托盘根总皂苷提取物。
1.2.2 总皂苷含量测定方法
参照文献[21]的试验方法,并稍加改动,标准品为齐墩果酸,绘制标准曲线:A=26.163c−0.006,R2=0.9998,式中:A为吸光度,c为皂苷质量浓度,mg/mL。
含量测定:将制备所得的总皂苷提取物溶于甲醇中,定容至50 mL,配得待测溶液。吸取0.1 mL待测溶液加入10 mL容量瓶,平行3组,按上文方法测定其吸光度,计算托盘根总皂苷得率。
(1) 式中,W为托盘根总皂苷得率(%);c为测定皂苷的浓度(mg/mL);V为供试液的体积(mL);n为稀释倍数;M为托盘根生药材质量(g)。
1.2.3 单因素实验设计
通过研究不同液料比(10:1、15:1、20:1、30:1、40:1 mL/g)、乙醇体积分数(50%、60%、70%、80%、90%)、提取时间(1、1.5、2、2.5、3 h)、提取温度(75、80、85、90、95 ℃)对得率的影响,在研究单因素影响时,选取其余因素中间值为固定提取条件,选择对得率影响显著的因素进行响应面试验设计,试验重复3次。
1.2.4 响应面试验
以单因素实验数据为参考,选择液料比(A)、乙醇体积分数(B)、提取时间(C)3个要素为自变量,以托盘根总皂苷的得率(Y)为响应值,利用Box-Behnken中心组实验法优化热回流提取工艺,用Design-Expert 8.0.6软件对试验数据进行拟合和分析,试验要素与水平如表1所示。
表 1 试验因素与水平Table 1. Experimental factors and levels因素 编码 编码水平 −1 0 1 液料比(mL/g) A 20:1 30:1 40:1 乙醇体积分数(%) B 60 70 80 提取时间(h) C 1.5 2 2.5 1.2.5 抗氧化实验
抗氧化活性测定参照文献[22]的方法并稍加改动。托盘根总皂苷提取物按照上述最佳工艺制得,并溶于80%乙醇溶液中。
DPPH自由基清除能力测定:配制1 mg/mL的样品溶液50 mL,再依次稀释为0.8、0.4、0.2、0.1、0.05、0.025 mg/mL。配制0.1 mg/mL的阳性对照VC溶液50 mL,再依次稀释为0.08、0.04、0.02、0.01、0.005、0.0025 mg/mL。取100 μL样品溶液加入100 μL的0.16 mmol/L DPPH溶液中,常温避光孵育30 min后在波长517 nm处测定吸光度A1,用甲醇代替样品溶液,测定吸光度A2,实验平行三次,计算DPPH·清除率。
(2) ABTS+自由基清除能力测定:将88 μL140 mmol/L的过硫酸钾和5 mL 7 mmol/L的ABTS溶液混合,常温避光孵育16 h,将得到的ABTS用水稀释至在734 nm波长下测得吸光度为0.70±0.02。配制1 mg/mL的样品溶液50 mL,再依次稀释为0.8、0.6、0.4、0.2、0.1、0.05、0.025 mg/mL。配制0.16 mg/mL的阳性对照VC溶液50 mL,再依次稀释为0.08、0.04、0.02、0.01、0.005、0.0025 mg/mL。取10 μL样品溶液加入190 μL的ABTS工作液中,常温避光孵育6 min后在波长734 nm处测定吸光度A1,用甲醇代替样品溶液,测定吸光度A2,计算ABTS+·清除率。
(3) (4) 1.3 数据处理
实验结果均为3次重复实验的平均值,数据处理采用Excel2016和SPSS17.0软件进行统计学分析。响应面实验数据采用Design-Expert 8.0.6软件进行结果和方差分析,显著水平P<0.05。
2. 结果与分析
2.1 单因素实验
2.1.1 液料比对托盘根总皂苷得率的影响
如图1所示,液料比在10:1~30:1 mL/g范围内,总皂苷得率缓慢升高,且在液料比30:1 mL/g时有最大得率2.868%,但随着液料比的继续增加,总皂苷的得率却开始下降。原因可能是提高液料比可以明显提升生药材与溶液的接触面积,让有效成分的扩散速率得到提升。当液料比为30:1 mL/g时,有效成分析出完全,如果液料比继续增加,则会不断溶出更多非皂苷成分,干扰总皂苷得率,增加成本[23-24]。因此选用液料比30:1 mL/g为最佳工艺提取条件。
2.1.2 乙醇体积分数对托盘根总皂苷得率的影响
如图2所示,乙醇浓度在50%~70%范围内,总皂苷得率明显提高,且在乙醇体积分数70%时有最大得率3.115%,但随着乙醇体积分数的继续增加,总皂苷的得率开始下降。可能是因为不同类型皂苷类化合物溶解度不同,而托盘根中的皂苷类化合物在70%的乙醇中溶解度较好,且部分皂苷在较高温度下会分解[25-27]。因此选用乙醇体积分数70%为最佳工艺提取条件。
2.1.3 提取时间对托盘根总皂苷得率的影响
由图3所示,当提取时间在1~2 h范围内时,托盘根总皂苷得率随之升高,当提取时间为2 h时,总皂苷的得率最高,为2.874%,当提取时间继续增加,总皂苷得率开始下降。原因可能是由于提取时间过长,细胞内其他物质溶出阻碍了皂苷溶出通道,导致得率降低[28-29]。因此选用提取时间2 h为最佳工艺提取条件。
2.1.4 提取温度对托盘根总皂苷得率的影响
如图4所示,当提取温度在75~95 ℃范围内时,托盘根总皂苷得率总体呈现上升趋势,当提取温度在80、85和95 ℃时,总皂苷得率分别为2.854%、2.929%和2.972%,其原理可能是提取温度的不同能够影响皂苷分子项提取溶剂扩散的速度,但较高的温度并不会进一步提升皂苷得率,同时考虑成本、资源等多重因素[30-31],采用85 ℃作为最佳提取温度。
2.2 响应面试验结果
使用Design-Expert 8.0软件分析试验数据,根据Box-Behnken设计得到三因素三水平的响应面试验设计方案及结果如表2所示。
表 2 响应面分析试验方案及结果Table 2. Results of response surface experiment实验号 A B C Y总皂苷得率(%) 1 30:1 70 2 3.576 2 20:1 70 1.5 2.508 3 30:1 80 1.5 2.998 4 30:1 80 2.5 3.016 5 30:1 70 2 3.173 6 20:1 60 2 2.937 7 40:1 70 1.5 2.722 8 40:1 70 2.5 3.343 9 20:1 80 2 2.991 10 30:1 60 1.5 2.901 11 30:1 60 2.5 3.113 12 40:1 80 2 3.385 13 40:1 60 2 2.739 14 30:1 70 2 3.40:19 15 30:1 70 2 3.40:13 16 30:1 70 2 3.664 17 20:1 70 2.5 3.095 本试验中,1、5、14、15、16 为五组中心试验,其他均为析因试验,17个试验点中包括析因点和零点,自变量A、B、C对应的三维顶点为析因点,零点试验重复5次,估算试验误差。
对表2数据进行多元回归拟合分析,可得到托盘根总皂苷得率与主要因素间的关系方程为:Y(%)=3.49−0.12A+0.052B−4.250E−0.003C+0.030AB+0.028AC−0.056BC−0.28A2−0.32B2−0.29C2。在试验设计中,一次项的偏回归系数绝对值A>B>C,表明对总皂苷得率的影响最大的是液料比,其次是乙醇体积分数和提取时间。总皂苷得率回归模型方差分析结果见表3。
表 3 回归模型方差分析结果Table 3. Regression model analysis of variance results来源 平方和 自由度 均方 F值 P值 显著性 模型 1.39 9 0.15 14.00 0.0011 ** A 0.11 1 0.11 9.58 0.0174 * B 0.022 1 0.022 1.96 0.2038 C 1.445×10−4 1 1.445×10−4 0.013 0.9122 AB 3.540×10−3 1 3.540×10−3 0.32 0.5894 AC 3.136×10−3 1 3.136×10−3 0.28 0.6110 BC 0.013 1 0.013 1.13 0.3224 A2 0.33 1 0.33 29.43 0.0010 ** B2 0.43 1 0.43 38.50 0.0004 ** C2 0.36 1 0.36 32.97 0.0007 ** 残差 0.077 7 0.011 失拟项 0.018 3 6.037×10−3 0.41 0.7571 纯误差 0.059 4 0.015 总离差 1.47 16 R2 0.9474 R2Adj 0.8797 CV(%) 3.42 注:*表示显著性差异(P<0.05),**表示显著性差异(P<0.01)。 从表3可以看出,对本实验模型和回归系数的方差分析结果显示P=0.0011<0.05,表明该回归模型水平显著;一次项A具有显著影响(P<0.05);在二阶因子中,A2、B2、C2对响应值的影响极显著(P<0.01);失拟项P值>0.05,表明方程对实验的拟合性良好,根据模型确决定系数R2=0.9474,表明测量值和预测值之间吻合度较高,校正RAdj2=0.8797,表明托盘根总皂苷得率有87.97%的程度受这三个因素影响,实验误差小,准确率高。变异系数(CV)反映模型的可信度,本实验的CV值为3.42,显示实验稳定性较好。因此,该模型适用于托盘根总皂苷提取结果的分析预测。
所构建模型的响应面及等高线关系由图5所示,托盘根总皂苷的得率随着各因素水平变化而变化,等高线图的维度可反映相互作用的强弱,在图5中可直观地看出AC、AB、BC即液料比和提取时间、液料比和乙醇体积分数、乙醇体积分数和提取时间的交互项对响应值有一定影响,验证了方差分析表中的结果。
根据所得到的模型,预测托盘根总皂苷的最佳提取工艺为:提取时间1.99 h,乙醇浓度70.74%,液料比27.96:1 mL/g。于此条件,托盘根总皂苷的得率理论上可达3.49%。根据实际工作条件,将其调整为:提取时间2 h,乙醇体积分数71%,液料比28:1 mL/g。于此条件,重复3次实验进行工艺验证,实际所得到的托盘根总皂苷得率为3.37%。
贺红军等[32]采用正交试验法对茅莓总皂苷提取条件进行优化,结果显示,在乙醇浓度80%,提取时间3 h,液料比20:1 mL/g,提取温度80 ℃的条件下,茅莓总皂苷的得率为1.994%,较托盘根总皂苷的得率稍低。通过比较,证明托盘根中含有较为丰富的皂苷类化合物,在同属植物中皂苷得率较高。
2.3 体外抗氧化试验
2.3.1 DPPH·清除试验结果
从图6可以看出,质量浓度在0.025~1 mg/mL之间托盘根提取物的DPPH·清除率(13.82%~91.24%)小于质量浓度在0.0025~0.1 mg/mL之间VC的清除率(14.85%~92.24%)。托盘根提取物DPPH·清除率的IC50值为0.0782 mg/mL,VC清除率的IC50值为0.0051 mg/mL,清除效果均随着质量浓度的增大而增大,当质量浓度在0.00625~0.025 mg/mL之间时,DPPH·清除效果明显提高,当质量浓度大于0.025 mg/mL时,DPPH·清除效果略有提高。韦一飞[33]比较了山莓根总多酚和VC的抗氧化活性,山莓根的DPPH·清除能力稍大于VC。结果表明,托盘根皂苷提取物对DPPH·的清除能力低于VC,且低于同属植物的多酚类化合物。
2.3.2 ABTS+·清除试验结果
从图7可以看出,质量浓度在0.025~1 mg/mL之间托盘根提取物的ABTS+·清除率(19.48%~84.38%)小于质量浓度在0.0025~0.16 mg/mL之间VC的清除率(25.83%~94.89%)。托盘根提取物ABTS+·清除率的IC50值为0.2770 mg/mL,VC清除率的IC50值为0.0053 mg/mL。托盘根提取物清除自由基的能力随质量浓度的增加而增强。汪礼洋[34]比较了树莓中的两种花色苷的ABTS+·清除作用,花色苷RA1和花色苷A2的ABTS+·的清除率均大于VC。说明托盘根提取物对ABTS+·的清除活性低于VC,低于同属其他植物。
2.3.3
从图8可以看出,质量浓度0.025~1.6 mg/mL之间托盘根提取物的
3. 结论
以托盘干燥根为原料,通过乙醇回流法提取总皂苷,在液料比、乙醇体积分数和提取时间等单因素试验的基础上,进行响应面Box-Behnken试验设计,最佳提取条件为:提取时间2 h,乙醇体积分数71%,液料比28:1 mL/g,此条件下托盘根总皂苷得率为3.37%,与预测值相近。体外抗氧化试验表明,托盘根提取物对DPPH·、ABTS+·清除力都较高,但其清除力较VC低;对
-
表 1 试验因素与水平
Table 1 Experimental factors and levels
因素 编码 编码水平 −1 0 1 液料比(mL/g) A 20:1 30:1 40:1 乙醇体积分数(%) B 60 70 80 提取时间(h) C 1.5 2 2.5 表 2 响应面分析试验方案及结果
Table 2 Results of response surface experiment
实验号 A B C Y总皂苷得率(%) 1 30:1 70 2 3.576 2 20:1 70 1.5 2.508 3 30:1 80 1.5 2.998 4 30:1 80 2.5 3.016 5 30:1 70 2 3.173 6 20:1 60 2 2.937 7 40:1 70 1.5 2.722 8 40:1 70 2.5 3.343 9 20:1 80 2 2.991 10 30:1 60 1.5 2.901 11 30:1 60 2.5 3.113 12 40:1 80 2 3.385 13 40:1 60 2 2.739 14 30:1 70 2 3.40:19 15 30:1 70 2 3.40:13 16 30:1 70 2 3.664 17 20:1 70 2.5 3.095 表 3 回归模型方差分析结果
Table 3 Regression model analysis of variance results
来源 平方和 自由度 均方 F值 P值 显著性 模型 1.39 9 0.15 14.00 0.0011 ** A 0.11 1 0.11 9.58 0.0174 * B 0.022 1 0.022 1.96 0.2038 C 1.445×10−4 1 1.445×10−4 0.013 0.9122 AB 3.540×10−3 1 3.540×10−3 0.32 0.5894 AC 3.136×10−3 1 3.136×10−3 0.28 0.6110 BC 0.013 1 0.013 1.13 0.3224 A2 0.33 1 0.33 29.43 0.0010 ** B2 0.43 1 0.43 38.50 0.0004 ** C2 0.36 1 0.36 32.97 0.0007 ** 残差 0.077 7 0.011 失拟项 0.018 3 6.037×10−3 0.41 0.7571 纯误差 0.059 4 0.015 总离差 1.47 16 R2 0.9474 R2Adj 0.8797 CV(%) 3.42 注:*表示显著性差异(P<0.05),**表示显著性差异(P<0.01)。 -
[1] 周繇. 中国长白山植物资源志[M]. 北京: 中国林业出版社, 2010: 11. Zhou Y. Changbai mountain plant resources in China[M]. Beijing: China Forestry Publishing House, 2010: 11.
[2] 魏忠宝, 孙佳明, 李朋飞, 等. 山楂叶悬钩子根抗氧化活性成分研究[J]. 中国中药杂志,2018,44(3):1−7. [Wei Z B, Sun J M, Li P F, et al. Antioxidant activity constituents from root of Rubus crataegifolius[J]. China Journal of Chinese Materia Medica,2018,44(3):1−7. [3] Ni W, Zhang X, Bi H, et al. Preparation of a glucan from the roots of Rubus crataegifolius Bge. and its immunological activity[J]. Carbohydrate Research,2009,344:2512−2518. doi: 10.1016/j.carres.2009.08.042
[4] 赵伟, 李超, 刘利民, 等. 托盘根的化学成分研究[J]. 中国药学杂志,2017,52(3):193−195. [Zhao W, Li C, Liu L M, et al. Chemical constituents from the roots of Rubus crataegifolius Bge J]. Chinese Pharmaceutical Journal,2017,52(3):193−195.
[5] 张萍, 肖新月, 张南平, 等. 蔷薇科根类药材化学成分及药理作用研究进展[J]. 中国药事,2008,22(8):721−726. [Zhang P, Xiao X Y, Zhang N P, et al. Review on research of the chemical constituents and pharmacological activities of plants of Rosaceae[J]. Chinese Pharmaceutical Affairs,2008,22(8):721−726. [6] 张旭, 房金波, 梁忠岩. 托盘根水溶性多糖的分离纯化及初步研究[J]. 特产研究,2005(1):40−42. [Zhang X, Fang J B, Liang Z Y. Purification and initial studies of the water-soluble polysaccharide RCP from the roots of Rubus crataegiflolius Bge doi: 10.3969/j.issn.1001-4721.2005.01.011 J]. Special Wild Economic Animal and Plant Research,2005(1):40−42. doi: 10.3969/j.issn.1001-4721.2005.01.011
[7] Lee J H, Ham Y A, Choi S H, et al. Activity of crude extract of Rubus crataegifolius roots as a potent apoptosis inducer and DNA topoisomerase I inhibitor[J]. Archives of Pharmacal Research,2000,23(4):338−343. doi: 10.1007/BF02975444
[8] Jung S W, Shin M H, Jung J H, et al. A triterpene glucosyl ester from the roots of Rubus crataegifolius[J]. Archives of Pharmacal Research,2001,24(5):412−415. doi: 10.1007/BF02975185
[9] 李秋叶. 山楂叶悬钩子的化学成分及保肝活性研究[D]. 延吉: 延边大学, 2013. Li Q Y. Study of chemical constituent and hepatoprotective activity of Rubus crataegifolius Bunge[D]. Yanji: Yanbian University, 2013.
[10] 闻利威, 张琼琳, 青格乐, 等. 皂苷生物活性及应用研究进展[J]. 畜牧与饲料科学,2020,41(4):90−96. [Wen L W, Zhang Q L, Qing G L, et al. Research advances on biological activities and application of saponins[J]. Animal Husbandry and Feed Science,2020,41(4):90−96. doi: 10.12160/j.issn.1672-5190.2020.04.018 [11] Liu Y, Yang Y, Feng Z, et al. Eight new triterpenoid saponins with antioxidant activity from the roots of Glycyrrhiza uralensis Fisch[J]. Fitoterapia,2019,133:186−192. doi: 10.1016/j.fitote.2019.01.014
[12] Jung M S, Lee S J, Song Y, et al. Rubus crataegifolius Bunge. regulates adipogenesis through Akt and inhibits high-fat diet-induced obesity in rats[J]. Nutrition & Metabolism,2016,13:29.
[13] Zhao Y, Su R, Zhang W, et al. Antibacterial activity of tea saponin from Camellia oleifera shell by novel extraction method[J]. Industrial Crops & Products,2020,153:112604.
[14] Xia C, Chen L, Sun W, et al. Total saponins from Paris forrestii (Takht) H. Li. show the anticancer and RNA expression regulating effects on prostate cancer cells[J]. Biomedicine & Pharmacotherapy,2020,121:109674.
[15] Desai T H, Joshi S V. Anticancer activity of saponin isolated from Albizia lebbeck using various in vitro models[J]. Journal of Ethnopharmacology,2019,231:494−502. doi: 10.1016/j.jep.2018.11.004
[16] Sun Y, Jia L, Huang Z, et al. Hepatoprotective effect against CCl4-induced acute liver damage in mice and high-performance liquid chromatography mass spectrometric method for analysis of the constituents of extract of Rubus crataegifolius[J]. Natural Product Research,2017,31:2695−2699. doi: 10.1080/14786419.2017.1292264
[17] Tian C, Chang Y, Liu X, et al. Anti-inflammatory activity in vitro, extractive process and HPLC-MS characterization of total saponins extract from Tribulus terrestris L. fruits[J]. Industrial Crops & Products,2020,150:112343.
[18] Hadidi M, Ibarz A, Pagan J. Optimisation and kinetic study of the ultrasonic-assisted extraction of total saponins from alfalfa (Medicago sativa) and its bioaccessibility using the response surface methodology[J]. Food Chemistry,2020,309:125786. doi: 10.1016/j.foodchem.2019.125786
[19] 左月明, 王亚芳, 张忠立, 等. 响应面分析法优化回流提取延龄草甾体皂苷工艺研究[J]. 时珍国医国药,2020,31(1):49−51. [Zuo Y M, Wang Y F, Zhang Z L, et al. Optimization of extraction of steroidal saponins from Trillium tschonoskii Maxim. using response surface methodology[J]. Lishizhen Medicine and Materia Medica Research,2020,31(1):49−51. [20] Zivkovic J, Savikin K, Jankovic T, et al. Optimization of ultrasound-assisted extraction of polyphenolic compounds from pomegranate peel using response surface methodology[J]. Separation and Purification Technology,2018,194:40−47. doi: 10.1016/j.seppur.2017.11.032
[21] Hierro J D, Herrera T, Garcia-Risco M R, et al. Ultrasound-assisted extraction and bioaccessibility of saponins from edible seeds: quinoa, lentil, fenugreek, soybean and lupin[J]. Food Research International,2018,109:440−447. doi: 10.1016/j.foodres.2018.04.058
[22] Yang X, Bai Z, Zhang D W, et al. Enrichment of flavonoid-rich extract from Bidens bipinnata L. by macroporous resin using response surface methodology, UHPLC-Q-TOF MS/MS-assisted characterization and comprehensive evaluation of its bioactivities by analytical hierarchy process[J]. Biomedical Chromatography,2020,34(11):e4933.
[23] 胡政宇. 乌拉草多糖的提取纯化、结构表征及生物活性研究[D]. 吉林: 吉林化工学院, 2019. Hu Z. Extraction, purification, structural characterization and biological activity of polysaccharides from Carex meyeriana Kunth[D]. Jilin: Jilin Institute of Chemical and Technology. 2019.
[24] 陈俭清, 高凌飞, 任涌志, 等. 响应面法优化丁香叶总皂苷提取工艺[J]. 食品工业科技,2016,37(10):320−323, 328. [Chen J Q, Gao L F, Ren Y Z, et al. Optimization of extraction process of total saponins from Syringa oblate Lindl. leaves by response surface methodology[J]. Science and Technology of Food Industry,2016,37(10):320−323, 328. [25] 徐士钊, 齐菲, 席雅琳, 等. 响应面法优化辽东楤木总皂苷提取工艺及其抗氧化作用[J]. 江苏农业科学,2020,48(03):204−209. [Xu S Z, Qi F, Xi Y L, et al. Optimization of extraction process of total saponins from Aralia elata (Miq.) Seem by response surface analysis and its antioxidant activity[J]. Jiangsu Agricultural Science,2020,48(03):204−209. [26] Le A V, Parks S E, Nguyen M, et al. Optimisation of the microwave-assisted ethanol extraction of saponins from gac (Momordica cochinchinensis Spreng.) seeds[J]. Medicines,2018,5(3):70. doi: 10.3390/medicines5030070
[27] 姬海刚, 杨秀芳, 惠昱昱, 等. 响应曲面法优化提取柴胡总皂苷的工艺[J]. 应用化工,2020,49(11):2787−2790, 2794. [Ji H G, Yang X F, Hui Y Y, et al. Response surface methodology for optimizing the extraction of total saponins from Bupleurum Chinese DC doi: 10.3969/j.issn.1671-3206.2020.11.025 J]. Applied Chemical Industry,2020,49(11):2787−2790, 2794. doi: 10.3969/j.issn.1671-3206.2020.11.025
[28] 王志娟, 张炜, 田格, 等. 超高压法提取藜麦皂苷的工艺研究[J]. 中国粮油学报,2020,35(6):45−50. [Wang Z J, Zhang W, Tian G, et al. Ultrahigh pressure extraction technology of saponins from quinoa husk[J]. Journal of the Chinese Cereals and Oils Association,2020,35(6):45−50. doi: 10.3969/j.issn.1003-0174.2020.06.007 [29] Huy T B, Phuong N T L, Nga B K, et al. Enzyme-assisted extraction of triterpenoid saponins from Pseuderanthemum palatiferum (Nees) Radlk. dry leaf powder and bioactivities examination of extracts[J]. Chemistry Select,2019,27(4):8129−8134.
[30] 张文婷, 王后玮, 潘金鹏, 等. 响应面法优化油茶壳中茶皂素提取工艺及HPLC验证[J]. 食品工业,2019,40(10):75−79. [Zhang W T, Wang H W, Pan J P, et al. Optimization of extraction process and HPLC verification of tea saponin from oil tea shell by response surface methodology[J]. The Food Industry,2019,40(10):75−79. [31] 许效群, 赵文婷, 苗秀香, 等. 藜麦麸皮总皂苷的提取纯化工艺研究[J]. 食品工业科技,2017,38(18):215−220. [Xu X Q, Zhao W T, Miao X X, et al. Extraction and purification of total saponins from quinoa bran[J]. Science and Technology of Food Industry,2017,38(18):215−220. [32] 贺红军, 邱宗荫. 正交试验优选茅莓总皂苷的提取工艺[J]. 中国药房,2012,23(7):611−613. [He H J, Qiu Z M. Study on the extraction process of the total saponins of Rubus parviflolius[J]. China Pharmacy,2012,23(7):611−613. doi: 10.6039/j.issn.1001-0408.2012.07.12 [33] 韦一飞. 山莓根成分分析及抗肿瘤、抗氧化作用研究[D]. 南宁: 广西中医药大学, 2018. Wei Y F. Component analysis and antitumor and antioxidant effects of Rubus corchorifolius L. f. roots[D]. Nanning: Guangxi University of Chinese Medicine, 2018.
[34] 汪礼洋. 树莓中花色苷的提取、分离、纯化及抗氧化活性研究[D]. 郑州: 河南工业大学, 2016. Wang L Y. Extraction, separation, purification and antioxidant activity of raspberry anthocyanins[D]. Zhengzhou: Henan University of Technology, 2016.
[35] 蔡成林, 黄庭海, 张青峰. 红莓和黑莓叶黄酮类化合物抗氧化活性的比较研究[J]. 生物化工,2020,6(6):33−35. [Cai C L, Huang T H, Zhang Q F. Comparative research on antioxidant activity of flavonoids from raspberry and blackberry leaves[J]. Biological Chemical Engineering,2020,6(6):33−35.






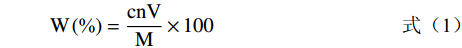
 下载:
下载:
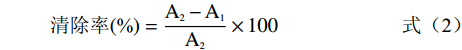
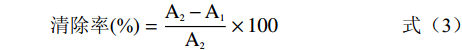
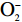

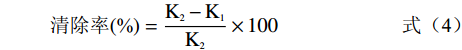







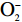
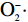
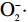
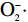
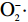

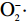
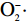
 下载:
下载:

