Extraction, Purification of Taro Globulin and Its Inhibitory Activity on α-Amylase and α-Glucosidase
-
摘要: 目的:探究芋头球蛋白体外调节血糖活性。方法:以磷酸缓冲液提取芋头球蛋白,以蛋白质提取率为指标考察了料液比、温度、时间和次数对蛋白质提取的影响,在此基础上采用响应面优化提取工艺。采用DEAE-52离子纤维素柱层析法纯化粗蛋白,通过高效液相色谱法检测纯化所得球蛋白的纯度,并测定其等电点和分子量。研究了芋头球蛋白对α-淀粉酶和α-葡萄糖苷酶的抑制活性及抑制动力学,以阿卡波糖为阳性对照,评价其体外调节血糖活性。结果:最佳提取条件为:料液比1:16 g/mL、温度41 ℃、时间124 min,此时提取率为36.75%±0.31%,得率0.70%±0.04%,纯度85.72%±0.47%。纯化后的球蛋白经高效液相色谱检测得一主峰,纯度为93.27%,得率为0.20%±0.01%,等电点pI=5.6,分子量为22 kDa左右。芋头球蛋白对两种酶的抑制活性与蛋白浓度存在量效关系,对α-淀粉酶的IC50为0.75±0.10 mg/mL,对α-葡萄糖苷酶的IC50为(2.09±0.19) mg/mL,而阿卡波糖对α-淀粉酶的IC50为(0.61±0.13) mg/mL,对α-葡萄糖苷酶的IC50为(0.69±0.16) mg/mL,说明芋头球蛋白对α-淀粉酶略低于阿卡波糖,而对α-葡萄糖苷酶抑制活性远低于阿卡波糖,二者的抑制类型均为可逆性的非竞争性抑制,对α-淀粉酶抑制的Ki=(0.61±0.05) mg/mL,对α-葡萄糖苷酶抑制的Ki=(0.26±0.02) mmol/L。结论:本研究优化了芋头球蛋白的提取工艺,纯化得到芋头球蛋白,研究发现其有一定的体外调节血糖的活性,对功能食品的研发和芋头产品提高附加值具有一定的指导意义。Abstract: Objective: Exploring taro globulin regulating activity in vitro. Methods: Taro globulin was extracted by phosphate buffer. The effects of solid-liquid ratio, temperature, time and times on protein extraction were investigated with protein extraction rate as an index. Based on the test, response surface methodology was used to optimize the extraction process. The crude protein was purified by DEAE-52 ion cellulose column chromatography. The purity of purified globulin was detected by high performance liquid chromatography, and its isoelectric point and molecular weight were determined. The inhibitory activity and inhibition kinetics of taro globulin on α -amylase and α-glucosidase were studied, and acarbose was used as positive control to evaluate globulin activity of regulating blood glucose in vitro. Results: The optimum extraction conditions were as follows: The solid-to-liquid ratio was 1:16 g/mL, the temperature was 41 ℃, and the time was 124 min. Under these condition, the extraction rate was 36.75%±0.31%, the yield was 0.70%±0.04%, and the purity of the protein was 85.72%±0.47%. The purified globulin was detected by high performance liquid chromatography with a main peak with purity of 93.27%, yield of 0.20%±0.01%, isoelectric point of 5.6 and molecular weight of about 22 kDa. The taro globulin exhibited inhibition on the two enzymes with dose-effect relationship. The IC50 was (0.75±0.10) mg/mL for α-amylase and was (2.09±0.19) mg/mL for α-glucosidase The IC50 of acarbose were (0.61±0.13) mg/mL and (0.69±0.16) mg/mL. The results showed that the inhibitory activity of taro globulin on α-amylase was slightly lower than acarbose, while the inhibitory activity on α-glucosidase was much lower than acarbose. The inhibition type was reversible and uncompetitive inhibitor, with Ki=(0.61±0.05) mg/ml for α-amylase and Ki=(0.26±0.02) mmol/L/L for α-glucosidase. Conclusion: The extraction process of taro globulin was optimized, and taro globulin was purified. It was found that taro globulin has certain activity of regulating blood sugar in vitro, which would have certain guiding significance for the research and development of functional food and the increasing of added value of taro products.
-
Keywords:
- taro /
- globulin /
- extraction /
- purification /
- glucose regulating activity
-
芋头(Colocasia esciclenta (L.)Schott)又称芋魁,俗名芋艿,天南星科魁芋属多年生草本传统药食两用植物[1],世界各地均有种植,其中广西荔浦芋较为出名,荔浦芋又名槟榔芋,个头大、产量高、营养物质丰富。芋头球蛋白分为G1和G2两种,各占可溶性蛋白的40%左右,一种凝集素Tarin,具有独特的碳水化合物结合特性,芋头的很多活性与其相关,另一种为蛋白酶抑制剂的Kunitz家族,氨基酸测序证实其与胰蛋白酶抑制有关[2]。比如研究者发现中国台湾的槟榔芋蛋白经胃蛋白酶酶解后具有抗氧化活性和血管紧张素转换酶抑制作用[3],芋头蛋白具有抗氧化[4]、调节免疫[3]、抗肿瘤和抗菌生长的能力[5]等活性。芋头蛋白提取工艺研究较少,芋头中活性蛋白一般采用含盐缓冲液提取,将芋头40 ℃以下烘干打粉[3]或将新鲜芋头打浆[6],4 ℃提取,硫酸铵盐析即可分离出蛋白质,童晶晶等[7]比较了几种提取溶剂,发现盐提蛋白胰蛋白酶抑制活性最高,黄友如等[8]采用分级提取Osborne分级法芋艿蛋白,其中清蛋白的提取率为43.38%。本文采用0.1 mol/L磷酸缓冲液(含0.3 mol/L NaCl,pH=6.8)的方法提取芋头球蛋白,芋头球蛋白占可溶性蛋白的80%左右,且文献[2]中报道的酶抑制活性与球蛋白有关,因此可初步认为本研究提取纯化所得活性蛋白即为球蛋白。
α-淀粉酶和α-葡萄糖苷酶能催化水解淀粉和低聚糖,引起餐后血糖升高[9-10]。Kumari等[11]提取纯化芋头蛋白,发现其能非竞争性抑制α-淀粉酶,70 ℃仍然保留较高活性,最适pH6.9,有研究表明块茎植物中抑制α-淀粉酶抑制活性蛋白也能抑制α-葡萄糖苷酶[12],分子量一般为11~25 kDa之间[13],与芋头中球蛋白的分子量相近,因此猜测芋头球蛋白也有抑制活性,Sharma等[14]从芋头中提取纯化得到两种α-淀粉酶抑制活性蛋白,能抵抗蛋白酶的酶解,与Mcewan等[13]发现芋头蛋白一样对α-淀粉酶抑制作用为选择性抑制。
芋头功能和营养特性已经研究了半个世纪,芋头蛋白具有一定的生物活性[1],国内对蛋白类α-淀粉酶和α-葡萄糖苷酶抑制剂提取工艺研究较少,而国外研究了芋头蛋白对α-淀粉酶抑制活性却对提取工艺没有对比与优化。因此,本文采用磷酸缓冲液提取芋头球蛋白,优化提取工艺,经DEAE-52离子纤维素柱层析纯化得到高活性组分,高效液相检测纯度,SDS-PAGE电泳测分子量,测等电点,研究其对α-淀粉酶和α-葡萄糖苷酶的抑制活性以评价其体外血糖调节活性,并通过酶抑制动力学初步研究作用机理,为进一步分析活性蛋白的结构和理化性质、研究其体内调节血糖活性奠定基础,有望指导功能食品的研发,提高芋头产品附加值。
1. 材料与方法
1.1 材料与仪器
新鲜广西荔浦芋头 于秋末采摘自南宁百货超市;猪胰腺α-淀粉酶(9 U/mg)、阿卡波糖(500 mg)A9281 北京索莱宝科技有限公司;酵母α-葡萄糖苷酶(50 U/mg) 南京都莱生物技术有限公司;可溶性淀粉 广州光华科技股份有限公司;对硝基苯-α-D-葡萄糖苷 上海麦克林生化科技有限公司;其他试剂 均为国产分析纯;实验用水 均为二级水。
Infinite M200 pro酶标仪 奥地利TECAN公司;KND系列凯氏定氮仪和消化炉 浙江托普云农科技股份有限公司。
1.2 实验方法
1.2.1 芋头蛋白的提取
1.2.1.1 芋头蛋白的提取工艺
提取工艺[15]:挑选完好、新鲜的芋头洗净去皮,切成1 cm3小块,按料液比1:15 mg/mL(干基)加入含0.3 mol/L氯化钠的0.1 mol/L磷酸缓冲液,于榨汁机中匀浆5 min,35 ℃恒温水浴提取2 h,4℃下5000 r/min离心15 min,上清液置于冰浴中,缓慢加入硫酸铵至80%饱和度,边加边轻轻搅拌,避免局部高浓度硫酸铵引起蛋白变性,离心得蛋白沉淀,溶于10倍体积的磷酸缓冲液,轻轻摇匀使溶解充分,所得蛋白液转入截留分子量3500 kDa的透析袋中,置于装有蒸馏水的大烧杯在4 ℃冰箱透析36 h,每6 h换一次水,冻干得粗蛋白粉。芋头总蛋白含量和粗蛋白中的总蛋白含量测定参照GB 5009.5-2016中凯氏定氮法,提取蛋白含量采取考马斯亮蓝法[16],以牛血清白蛋白为标准品制作标准曲线,蛋白质标曲为y=0.2019x+0.0037(R2=0.9995,其中x为吸光度,y为蛋白浓度)。蛋白质提取率、得率和纯度计算公式如下[17]:
1.2.1.2 芋头蛋白提取工艺单因素实验
设定基本条件为料液比1:15 g/mL,温度35 ℃,提取时间2 h,次数2次,改变其中一个条件,分别考察各因素对蛋白提取率的影响[18]:料液比取1:5、1:7.5、1:10、1:12.5、1:15、1:17.5、1:20 (g/mL),温度取25、30、35、40、50、60、70 ℃,提取时间取30、60、90、120、150、180 min,次数取1、2、3、4次。
1.2.1.3 响应面优化芋头蛋白提取工艺
选取料液比、提取温度和提取时间为因素,以蛋白质提取率为响应值,设计Box-Behnken试验[19],每组重复3次,因素及水平如表1。
表 1 响应面试验因素和水平Table 1. Independent variables and their coded levels used in response surface methodology因素 编码水平(Xi) −1 0 1 A 料液比(g/mL) 10 15 20 B 提取温度(℃) 30 40 50 C 提取时间(min) 90 120 150 1.2.2 芋头蛋白的纯化
采用DEAE-52纤维素离子交换层析柱[20]对芋头蛋白进行初步纯化。填料按照说明书中方法处理好,装入层析柱(2.6 cm×50 cm)自然沉降,关柱调节流速至0.3 mL/min平衡12 h,上样5.0 mL浓度40 mg/mL的芋头蛋白质溶液,待蛋白质溶液与填料上端平齐后,关柱,静置吸附1 h,以含氯化钠浓度0、0.1、0.2、0.3、0.4 mol/L的磷酸缓冲液洗脱,流速0.2 mL/min,15 min/管,40 管/组。分部收集器收集洗脱液,测OD280制作洗脱曲线,合并洗脱液,透析,冷冻干燥得纯化后的芋头球蛋白。
采用高效凝胶排阻色谱(GPC)[21]测蛋白质纯度,色谱条件:色谱柱SB-804HQ;流动相5%甲醇;检测波长280 nm;柱温度25 ℃;流速0.5 mL/min。
1.2.3 芋头球蛋白等电点和SDS-PAGE电泳分析
1.2.3.1 芋头蛋白等电点的测定
参考文献[22]将芋头球蛋白配成1.0 mg/mL溶液,用不同浓度醋酸溶液配成不同pH的溶液5.0 mL于15 mL离心管中,加入1.0 mL蛋白溶液,4℃静置1 h后5000 r/min离心15 min,测上清液蛋白质浓度,浓度最低说明沉淀量最大,即为等电点。
1.2.3.2 芋头蛋白SDS-PAGE电泳分析
配制1.0 mg/mL蛋白质溶液,加入4倍非还原上样缓冲液,混匀后1000 r/min离心5 min,参考文献[23]采用SDS-PAGE电泳法,配制5%浓缩胶、12%分离胶,蛋白上样量10 μL,80 V电泳至浓缩胶与分离胶的分界线处,改为120 V继续电泳至分离胶底部,考马斯亮蓝染色30 min,快速脱色液脱色,凝胶成像系统拍照、分析电泳条带。
1.2.4 芋头球蛋白对α-淀粉酶和α-葡萄糖苷酶的抑制动力学研究
1.2.4.1 芋头球蛋白对α-淀粉酶和α-葡萄糖苷酶抑制活性测定
确定最佳反应时间和α-淀粉酶浓度,使酶反应的速率在0.03~0.25 ΔA/min之间[24]。α-淀粉酶抑制活性采用3,5-二硝基水杨酸比色法[25],将0.25 mL的α-淀粉酶移入25 mL具塞试管,加入0.25 mL酶液,0.25 mL的蛋白质溶液,阳性对照以同体积1.0 mg/mL阿卡波糖代替,37 ℃预热10 min,加入10 mg/mL的可溶性淀粉3.25 mL,水浴振荡反应10 min后立即加入1.5 mL DNS终止反应,沸水浴5 min,流水冷却,蒸馏水定容至25 mL,空白组及对照组以同体积PBS代替,酶标仪测540 nm处吸光度。α-葡萄糖苷酶抑制活性采用4-硝基酚-α-D-吡喃葡萄糖苷(pNPG)比色法[26],反应体系采用96孔板法,加入120 L PBS,20 μL样品溶液,阳性对照以同体积1.0 mg/mL阿卡波糖代替,20 μL 0.3 U/mL的α-葡萄糖苷酶,37 ℃预热10 min,加20 μL 2.5 mmol/L pNPG反应30 min,加1.0 mol/L碳酸钠终止反应,测410 nm处吸光度,抑制率公式如下。
1.2.4.2 α-淀粉酶活性抑制动力学研究
参考文献[27]方法稍有改动,不同酶浓度(3.0、4.0、5.0、6.0、7.0 mg/mL)下测定球蛋白作用下的反应速率,绘制反应动力学曲线。固定酶浓度为0.5 mg/mL,测定不同底物浓度2.0、4.0、6.0、8.0、10.0 mg/mL时芋头球蛋白作用下的反应速率,作双倒数曲线判断抑制类型,求抑制常数Ki。
1.2.4.3 α-葡萄糖苷酶活性抑制动力学研究
参考文献[28]方法稍有改动,不同酶浓度(0.2、0.3、0.4、0.5、0.6 U/mL)下测球蛋白作用下的反应速率,绘制反应动力学曲线。测不同pNPG浓度为0.5、1.0、1.5、2.0、2.5、3.0 mmol/L时的反应速率,作双倒数曲线判断抑制类型,求抑制常数Ki。
1.3 数据处理
所有实验均进行3次平行实验,数据采用平均值±标准差的形式,采用Design-Expert8.0.6软件、SPSS17.0、Excel2010和Origin8.0软件分析处理数据。
2. 结果与分析
2.1 芋头蛋白的提取
2.1.1 单因素实验
如图1,随着料液比的提高,蛋白质提取率先增加后趋于稳定,因为料液比的提高可以增加原料与提取溶剂的接触面积,促进蛋白质溶出,但料液比超过1:15 g/mL后,不仅会增加杂质溶出,溶液中盐离子增多可能使蛋白变性,且导致蛋白浓度过低不利于后续的盐析,因此选取1:15 g/mL为宜。如图2,温度对蛋白质的提取率影响较大,低于25 ℃不利于蛋白质溶出,高于60 ℃可能引起淀粉糊化而包裹住蛋白质阻碍其溶出,40 ℃之前提取率随温度急剧变化,之后趋于稳定,70 ℃时提取率降低,可能是因为淀粉糊化包裹蛋白在离心时除去,为保证活性和提取率选取40 ℃作为提取温度。如图3,蛋白质提取率随提取时间先增加后降低,蛋白质的提取率与时间密切相关,时间少于60 min时蛋白质没有充分溶出,导致提取不够充分,而时间超过150 min蛋白质可能会变性沉淀而在离心中除去,因此,选取120 min作为提取时间。如图4,提取2次以后,蛋白质提取率增加变缓慢,表明大部分蛋白质已充分提取,因此,选取2次作为提取次数。
2.1.2 响应面优化芋头蛋白提取工艺
根据Box-Benhnken设计试验,结果见表2。使用Design Expert 8.0.6分析和拟合后得芋头蛋白的提取率(Y)对料液比(A)、提取温度(B)和提取时间(C)的二次多项式回归模型:
表 2 响应面试验设计与结果Table 2. Design and results of response urface methodology实验号 因素 响应值 料液比(mL/g) 温度(℃) 时间(min) 蛋白质提取率(%) 1 10 30 120 31.81±0.83 2 20 30 120 34.53±1.16 3 10 50 120 32.94±0.95 4 20 50 120 34.96±0.66 5 10 40 90 30.25±0.79 6 20 40 90 33.39±0.98 7 10 40 150 32.97±0.58 8 20 40 150 34.67±0.85 9 15 30 90 33.45±1.07 10 15 50 90 35.11±0.84 11 15 30 150 35.62±0.72 12 15 50 150 36.48±0.86 13 15 40 120 36.56±0.59 14 15 40 120 36.51±0.62 15 15 40 120 36.59±0.74 16 15 40 120 36.68±0.84 17 15 40 120 36.74±0.69 Y(%)=36.62+1.20A+0.51B+0.94C−0.18AB−0.36AC−0.20BC−2.70A2−0.36B2−1.10C2
如表3进行显著性分析,模型回归P<0.0001,失拟项0.0662>0.05,表明残差由随机误差引起,模型复决定系数R2=0.9971,所以模型可解释99.71%的响应值变化,模型校正决定系数R2Adj=0.9933,与R2接近,表明模型具有充分性和准确性。由表中F值可知三因素对提取率的影响:A>C>B,即料液比>提取时间>提取温度,一次项A、B、C,交互项AC和二次项A2、B2、C2极显著(P<0.01);交互项BC显著(P<0.05);其他均不显著。
表 3 回归模型方差分析表Table 3. Analysis of variance of regression model来源 平方和 自由度 均方 F值 P值 显著性 模型 59.99229 9 6.66581 262.9955 < 0.0001 ** A-料液比 11.47205 1 11.47205 452.6229 < 0.0001 ** B-提取温度 2.0808 1 2.0808 82.09672 < 0.0001 ** C-提取时间 7.10645 1 7.10645 280.3807 < 0.0001 ** AB 0.1225 1 0.1225 4.833164 0.0639 AC 0.5184 1 0.5184 20.45316 0.0027 ** BC 0.16 1 0.16 6.312704 0.0402 * A2 30.70611 1 30.70611 1211.491 < 0.0001 ** B2 0.532127 1 0.532127 20.99477 0.0025 ** C2 5.053138 1 5.053138 199.3685 < 0.0001 ** 残差 0.17742 7 0.025346 失拟项 0.1429 3 0.047633 5.519506 0.0662 净误差 0.03452 4 0.00863 总离差 60.16971 16 注: *:差异显著(P<0.05),**:差异极显著(P<0.01)。 由图5反映的是第三个因素处于零水平判断另外两个因素的交互作用,随料液比和温度的增加,提取率先提高后降低,提取率随温度的变化幅度小于料液比,交互作用不显著;随料液比和提取时间的增加,提取率先提高后降低,在几何中心点达到最大,交互作用显著,随提取时间和提取温度,提取率在温度提高时变化不大,随提取时间增加提取率快速提高后趋于平缓,两者的交互作用较显著,这与表3中AC的交互作用最显著一致,即料液比和时间对提取率的交互影响最大。最优提取条件的确定及验证:将回归方程对A、B、C分别取一阶偏导数等于零,得到最佳条件为料液比15.67:1 mL/g、温度41.33 ℃、时间124 min,此时的提取率为36.88%±0.25%,考虑实际操作将其修正为料液比16:1 mL/g、温度41 ℃、时间124 min,为验证响应面试验的准确性,重复实验3次,得提取率为36.75%±0.31%,和预测值吻合良好,表明此模型可用。童晶晶[15]采用盐提法提取香芋蛋白,提取率为55.68%,常银子等[29]采用酶法提取芋艿分离蛋白的提取率为10.20%,芋头蛋白的提取率与芋头品种和提取方法有关,本研究蛋白提取率相对较高,可用于活性蛋白的提取。
2.2 芋头蛋白的纯化
由图6和表4可知,芋头粗蛋白经DEAE-52纤维素层析柱后得四个洗脱组分,其中0.1 mol/L氯化钠洗脱组分蛋白含量最高,由含量可求出得率为0.20%±0.01%,且活性最高,可作为活性蛋白进一步研究。
表 4 DEAE-52纤维素柱层析不同盐浓度洗脱组分的蛋白质含量和酶抑制活性Table 4. Protein content and enzyme inhibitory activity of elution components with different salt concentrations on DEAE-52 cellulose column chromatographyNaCl浓度
(mol/L)蛋白质含量
(mg)1.0mg/mL蛋白质
对α-淀粉酶的
抑制率(%)1.0mg/mL蛋白质
对α-葡萄糖苷酶
的抑制率(%)0 13.84±0.15 7.62±0.16 5.32±0.38 0.1 65.58±0.41 58.62±0.45 35.92±0.87 0.2 53.24±0.47 12.32±0.23 9.05±0.59 0.3 15.24±0.28 8.43±0.26 5.86±0.27 0.4 3.49±0.52 4.72±0.45 2.12±0.33 由图7和表5可知,芋头蛋白纯化洗脱曲线中共有4个吸收峰,在20.078 min处有一主峰,经计算得该峰对应蛋白的纯度为93.27%,表明蛋白纯化效果较好。
表 5 芋头蛋白提取率和纯度Table 5. Extraction rate and purity of taro protein样品 蛋白质提取率(%) 蛋白质得率(%) 蛋白质纯度(%) 粗蛋白 36.75±0.31a 0.70±0.04a 85.72±0.47a 球蛋白 10.47±0.07b 0.20±0.01b 93.27±0.29b 注:同列不同字母代表差异显著(P<0.05)。 2.3 芋头蛋白等电点和SDS-PAGE电泳分析
2.3.1 芋头蛋白等电点的测定
如图8,pH=5.6时上清液蛋白浓度最低,说明此时蛋白沉淀量最大,即为芋头球蛋白等电点,在Damares等测得的芋头球蛋白G1等电点(pI)为5.5~9.5内[30]。
2.3.2 芋头蛋白SDS-PAGE电泳分析
如图9所示,芋头粗蛋白分子量为12、22、40、55和63 kDa,纯化后得到电泳纯的球蛋白,分子量为22 kDa左右,与文献[2]中具有蛋白酶抑制活性的芋头球蛋白的分子量一致。Sharma 等[14]提取纯化得到的两种具有α-淀粉酶抑制活性的蛋白的分子量为14.3和12.5 kDa,文献[30]中报道的一种芋头球蛋白也由12.5 kDa的同型亚基组成,其与很多活性有关。童晶晶[15]比较了不同提取溶剂的分子量,发现Tris提取物所含条带最多,胰蛋白酶抑制活性最强,表明一定浓度的缓冲液能促进蛋白溶出且蛋白种类保留率高,本文采用的磷酸缓冲液提取的蛋白条带也较多,说明可用于活性蛋白的提取。
2.4 芋头球蛋白对α-淀粉酶和α-葡萄糖苷酶的抑制动力学研究
2.4.1 α-淀粉酶和α-葡萄糖苷酶抑制活性的测定
由图10、图11可知,随着芋头球蛋白浓度增加,其对两种酶的抑制活性均增强,且呈良好的量效关系。利用SPSS软件求出芋头球蛋白对α-淀粉酶的IC50为(0.75±0.10) mg/mL,对α-葡萄糖苷酶的IC50为(2.09±0.19) mg/mL,阿卡波糖对α-淀粉酶的IC50为(0.61±0.13) mg/mL,对α-葡萄糖苷酶的IC50为(0.69±0.16) mg/mL。芋头球蛋白对α-淀粉酶的抑制活性与阿卡波糖相当,而对α-葡萄糖苷酶抑制活性低于阿卡波糖。
2.4.2 芋头球蛋白对α-淀粉酶和α-葡萄糖苷酶的抑制动力学研究
参照文献[27,31]能够确定芋头球蛋白对α-淀粉酶的抑制作用类型,由抑制动力学曲线图12、图13可知,加入不同浓度蛋白时所得的直线交于原点,且随蛋白浓度增加斜率减少,说明芋头球蛋白对α-淀粉酶和α-葡萄糖苷酶均为可逆抑制,且图14、图15的Lineweaver-Burk双倒数曲线符合非竞争性抑制的特点,因此推测芋头球蛋白对α-淀粉酶和α-葡萄糖苷酶为非竞争性抑制,蛋白与酶通过形成复合物来抑制酶,该复合物阻断活性位点或改变酶的构象,最终导致其催化活性降低,与文献一致[11]。由表6的双倒数曲线方程可以求得芋头球蛋白对α-淀粉酶抑制的Ki=(0.61±0.05) mg/mL,对α-葡萄糖苷酶抑制的Ki=(0.26±0.02) mmol/L,说明芋头球蛋白对两种酶的抑制活性均较高。
表 6 芋头球蛋白与α-淀粉酶和α-葡萄糖苷酶反应的Lineweaver-Burk双倒数曲线方程Table 6. Lineweaver-Burk plots equation of the reactions of α-amylase and α-glucosidase with taro globulin球蛋白浓度(mg/mL) α-淀粉酶反应的双倒数曲线方程 α-葡萄糖苷酶反应的双倒数曲线方程 0 y=25.385x+11.77,R2=0.997 y=23.689x+12.706,R2=0.9934 1.0 y=59.583x+30.255,R2=0.9974 y=33.67x+18.526,R2=0.9948 2.0 y=119.7x+62.758,R2=0.996 y=39.143x+22.322,R2=0.9967 3. 结论
芋头不仅提供营养物质,还是天然活性物质的主要来源。本研究从芋头中提取纯化得到一种球蛋白,发现其对α-淀粉酶和α-葡萄糖苷酶均具有较高的抑制活性,存在量效关系,且纯化后活性明显提高,抑制类型均为可逆的非竞争性抑制,表明芋头球蛋白具有一定的体外调节血糖活性,但还需进一步对球蛋白进行鉴定、研究构效关系和体内作用机制。另外,可进一步对其体内消化进行研究;或者酶解蛋白得到活性肽,对生物活性肽片段进行后续分离、纯化和测序研究,应用于保健食品、食品配料或其他类型的食品。
-
表 1 响应面试验因素和水平
Table 1 Independent variables and their coded levels used in response surface methodology
因素 编码水平(Xi) −1 0 1 A 料液比(g/mL) 10 15 20 B 提取温度(℃) 30 40 50 C 提取时间(min) 90 120 150 表 2 响应面试验设计与结果
Table 2 Design and results of response urface methodology
实验号 因素 响应值 料液比(mL/g) 温度(℃) 时间(min) 蛋白质提取率(%) 1 10 30 120 31.81±0.83 2 20 30 120 34.53±1.16 3 10 50 120 32.94±0.95 4 20 50 120 34.96±0.66 5 10 40 90 30.25±0.79 6 20 40 90 33.39±0.98 7 10 40 150 32.97±0.58 8 20 40 150 34.67±0.85 9 15 30 90 33.45±1.07 10 15 50 90 35.11±0.84 11 15 30 150 35.62±0.72 12 15 50 150 36.48±0.86 13 15 40 120 36.56±0.59 14 15 40 120 36.51±0.62 15 15 40 120 36.59±0.74 16 15 40 120 36.68±0.84 17 15 40 120 36.74±0.69 表 3 回归模型方差分析表
Table 3 Analysis of variance of regression model
来源 平方和 自由度 均方 F值 P值 显著性 模型 59.99229 9 6.66581 262.9955 < 0.0001 ** A-料液比 11.47205 1 11.47205 452.6229 < 0.0001 ** B-提取温度 2.0808 1 2.0808 82.09672 < 0.0001 ** C-提取时间 7.10645 1 7.10645 280.3807 < 0.0001 ** AB 0.1225 1 0.1225 4.833164 0.0639 AC 0.5184 1 0.5184 20.45316 0.0027 ** BC 0.16 1 0.16 6.312704 0.0402 * A2 30.70611 1 30.70611 1211.491 < 0.0001 ** B2 0.532127 1 0.532127 20.99477 0.0025 ** C2 5.053138 1 5.053138 199.3685 < 0.0001 ** 残差 0.17742 7 0.025346 失拟项 0.1429 3 0.047633 5.519506 0.0662 净误差 0.03452 4 0.00863 总离差 60.16971 16 注: *:差异显著(P<0.05),**:差异极显著(P<0.01)。 表 4 DEAE-52纤维素柱层析不同盐浓度洗脱组分的蛋白质含量和酶抑制活性
Table 4 Protein content and enzyme inhibitory activity of elution components with different salt concentrations on DEAE-52 cellulose column chromatography
NaCl浓度
(mol/L)蛋白质含量
(mg)1.0mg/mL蛋白质
对α-淀粉酶的
抑制率(%)1.0mg/mL蛋白质
对α-葡萄糖苷酶
的抑制率(%)0 13.84±0.15 7.62±0.16 5.32±0.38 0.1 65.58±0.41 58.62±0.45 35.92±0.87 0.2 53.24±0.47 12.32±0.23 9.05±0.59 0.3 15.24±0.28 8.43±0.26 5.86±0.27 0.4 3.49±0.52 4.72±0.45 2.12±0.33 表 5 芋头蛋白提取率和纯度
Table 5 Extraction rate and purity of taro protein
样品 蛋白质提取率(%) 蛋白质得率(%) 蛋白质纯度(%) 粗蛋白 36.75±0.31a 0.70±0.04a 85.72±0.47a 球蛋白 10.47±0.07b 0.20±0.01b 93.27±0.29b 注:同列不同字母代表差异显著(P<0.05)。 表 6 芋头球蛋白与α-淀粉酶和α-葡萄糖苷酶反应的Lineweaver-Burk双倒数曲线方程
Table 6 Lineweaver-Burk plots equation of the reactions of α-amylase and α-glucosidase with taro globulin
球蛋白浓度(mg/mL) α-淀粉酶反应的双倒数曲线方程 α-葡萄糖苷酶反应的双倒数曲线方程 0 y=25.385x+11.77,R2=0.997 y=23.689x+12.706,R2=0.9934 1.0 y=59.583x+30.255,R2=0.9974 y=33.67x+18.526,R2=0.9948 2.0 y=119.7x+62.758,R2=0.996 y=39.143x+22.322,R2=0.9967 -
[1] 童晶晶, 赖富饶, 吴晖, 等. 加工因素对张溪香芋全粉品质影响[J]. 粮食与油脂,2014,27(8):20−24. doi: 10.3969/j.issn.1008-9578.2014.08.006 [2] Pereira P R, Silva J T, Verícimo M A, et al. Crude extract from taro (Colocasia esculenta) as a natural source of bioactive proteins able to stimulate haematopoietic cells in two murine models[J]. Journal of Functional Foods,2015,18:333−343. doi: 10.1016/j.jff.2015.07.014
[3] Wu C, Lin K. The Antioxidative Characteristics of taro and sweet potato protein hydrolysates and their inhibitory capability on angiotensin converting enzyme[J]. Food Science and Technology Research,2017,23(6):845−853. doi: 10.3136/fstr.23.845
[4] Pereira P R, Corrêa A C N T, Vericimo M A, et al. Tarin, a potential immunomodulator and cox-inhibitor lectin found in taro (Colocasia esculenta)[J]. Comprehensive Reviews in Food Science and Food Safety,2018,17(4):878−891. doi: 10.1111/1541-4337.12358
[5] Yu J, Liu P, Duan J, et al. Itches-stimulating compounds from Colocasia esculenta (taro): Bioactive-guided screening and LC-MS/MS identification[J]. Bioorganic & Medicinal Chemistry Letters,2015,25(20):4382−4386.
[6] Ribeiro P P, Mere D A E, Afonso V M, et al. Purification and characterization of the lectin from taro (Colocasia esculenta) and its effect on mouse splenocyte proliferation in vitro and in vivo[J]. The Protein Journal, 2014, 33(1): 92-99. [7] 童晶晶, 张晓元, 赖富饶, 等. 不同溶剂对香芋蛋白提取及活性的影响[J]. 现代食品科技,2016,32(1):194−202. [8] 黄友如, 王教飞, 李昕蓓, 等. 芋艿分离蛋白的制备及工艺条件优化[J]. 常熟理工学院学报,2017,31(2):97−103. doi: 10.3969/j.issn.1008-2794.2017.02.021 [9] 罗丽平, 李冰晶, 赵景芳, 等. 三种食用菌提取物体外抗氧化与降血糖活性研究[J]. 食品工业科技,2020,41(20):324−329. [10] 李波, 包怡红, 高锋, 等. 红松松球鳞片多酚对α-淀粉酶和α-葡萄糖苷酶的抑制作用[J]. 食品工业科技,2015,36(1):63−65. [11] Kumari B, Sharma P, Nath A K. α-Amylase inhibitor in local Himalyan collections of Colocasia: Isolation, purification, characterization and selectivity towards α-amylases from various sources[J]. Pesticide Biochemistry and Physiology,2012,103(1):49−55. doi: 10.1016/j.pestbp.2012.03.003
[12] Tiengburanatam N, Boonmee A, Sangvanich P, et al. A novel alpha-glucosidase inhibitor protein from the rhizomes of Zingiber ottensii Valeton[J]. Appl Biochem Biotechnol,2010,162(7):1938−1951. doi: 10.1007/s12010-010-8971-7
[13] Mcewan R , Madivha R P , Djarova T , et al. Alpha-amylase inhibitor of amadumbe (Colocasia esculenta): Isolation, purification and selectivity toward alpha-amylases from various sources[J]. African Journal of Biochemistry Research,2010,4(9):220−224.
[14] Sharma K K, Pattabiraman T N. Natural plant enzyme inhibitors. Isolation and characterisation of two α-amylase inhibitors from Colocasia antiquorum tubers[J]. Journal of the Science of Food and Agriculture,1980,31(10):981−991. doi: 10.1002/jsfa.2740311003
[15] 童晶晶. 香芋蛋白的提取及其胰蛋白酶抑制剂的研究[D]. 广州: 华南理工大学, 2016. [16] 杨静华. 考马斯亮蓝法测定苦荞麦中可溶性蛋白的含量[J]. 山西医药杂志,2018,47(2):206−207. doi: 10.3969/j.issn.0253-9926.2018.02.035 [17] 石玮婷, 李荣, 姜子涛. 紫苏籽蛋白的提取及纯化研究[J]. 中国食品添加剂,2013(4):68−74. doi: 10.3969/j.issn.1006-2513.2013.04.003 [18] 黄文. 白果活性蛋白的分离、纯化、结构及其生物活性研究[D]. 武汉: 华中农业大学, 2002. [19] 阙淼琳, 蒋玉蓉, 曹美丽, 等. 响应面试验优化藜麦种子多酚提取工艺及其品种差异[J]. 食品科学,2016,37(4):7−12. doi: 10.7506/spkx1002-6630-201604002 [20] 周晓薇, 王静, 段浩, 等. 铁棍山药蛋白质的分离纯化及体外抗氧化活性[J]. 食品科学,2011,32(9):31−35. [21] 李雨哲. 马氏珍珠贝糖蛋白提取纯化及其抗氧化活性的研究[D]. 广州: 华南理工大学, 2011. [22] 崔竹梅, 王红玲, 张占琴, 等. 鹰嘴豆籽粒清蛋白和球蛋白等电点、相对分子量的测定[J]. 干旱地区农业研究,2007(6):89−95. [23] 周仲驹等夏其昌张祥明. 蛋白质电泳技术指南[M]. 北京: 化学工业出版社, 2007: 23−30. [24] 刘睿, 潘思轶, 刘亮, 等. 高粱原花青素对α-淀粉酶活力抑制动力学的研究[J]. 食品科学,2005(9):171−174. [25] 秦樱瑞, 黄先智, 曾艺涛, 等. 干燥方法对苦瓜降糖成分含量的影响[J]. 食品科学,2015,36(15):56−61. doi: 10.7506/spkx1002-6630-201515012 [26] Wu Y, Zhou Q, Chen X, et al. Comparison and screening of bioactive phenolic compounds in different blueberry cultivars: Evaluation of anti-oxidation and α-glucosidase inhibition effect[J]. Food Research International,2017,100:312−324. doi: 10.1016/j.foodres.2017.07.004
[27] 张永军, 黄惠华. 茶多酚对胰α-淀粉酶的抑制动力学研究[J]. 食品工业,2010,31(1):7−9. [28] 马庆一, 陈丽华, 杨海延, 等. 山茱萸中α-葡萄糖苷酶抑制活性因子的筛选(Ⅰ)[J]. 食品科学,2007(1):167−170. doi: 10.3321/j.issn:1002-6630.2007.01.039 [29] 常银子, 王丽霞, 仲山民, 等. 酶法提取芋艿蛋白质工艺[J]. 食品研究与开发,2011,32(3):19−22. doi: 10.3969/j.issn.1005-6521.2011.03.006 [30] Damares C. Monte-Neshich T L R R. Characterization and spatial localization of the major globulin families of taro (Colocasia esculenta L. Schott) tubers[J]. Plant Science, 1995, 112: 149-159.
[31] 伍城颖, 吴启南, 王红, 等. 芡种皮多酚提取物体外抑制α-葡萄糖苷酶和α-淀粉酶活性研究[J]. 食品工业科技,2015,36(16):91−94.





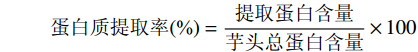
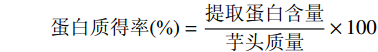
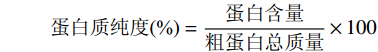
 下载:
下载:
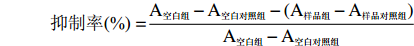















 下载:
下载:
