Research Progress on Preparation Process and Biological Activity of Marine Oligosaccharides
-
摘要: 随着海洋多糖研究的日益广泛,人们对海洋寡糖的研究也越来越受到重视。海洋寡糖是由海洋生物多糖经不同方法降解得到的小分子聚合物,具有来源广泛、分子量小、结构独特等特点。经降解后的海洋寡糖较多糖表现出更强的生物活性,具有抗氧化活性、抗肿瘤活性、免疫调节活性、抗炎活性、调节肠道微生物及许多其他生物活性,被广泛应用于食品、保健品、医学等领域。目前,海洋寡糖的制备方法主要有化学降解法、物理降解法和酶降解法。为了让更多人了解海洋寡糖的最新研究进展,促进海洋寡糖的研究与开发,本文重点对海洋寡糖的制备方法及生物活性进行了综述,以期为海洋寡糖的深入研究与开发提供一定的参考。Abstract: With the increasing research of marine polysaccharides, people are attaching importance to the research of marine oligosaccharides. Marine oligosaccharides are prepared by the degradation from marine polysaccharides with different methods. They have the characteristics of abundant sources, small molecular weight and unique structure. The degraded marine oligosaccharides have stronger biological activities than marine polysaccharides, such as anti-oxidation, anti-tumor, immunomodulation, anti-inflammatory, regulating intestinal microorganisms, etc. Therefore, they are widely used in food, health products, medicine and other fields. At present, the methods of marine oligosaccharides preparation include: Chemical degradation, physical degradation and enzyme degradation. In order to understand the research progress, promote the application and development of marine oligosaccharides, in this paper, the preparation methods and physiological activities of marine oligosaccharides are reviewed, which is expected to provide references for the further research and development of marine oligosaccharides.
-
海洋植物、海洋动物和海洋微生物是海洋多糖的主要来源,可大量制备结构新颖的糖类化合物,如海洋藻类来源的海藻酸盐、卡拉胶和琼胶,海洋动物来源的甲壳素、岩藻聚糖等,在食品、医药、农业、保健品及日化等诸多领域应用广泛[1-3]。海洋生物因其生存环境特殊,长期生活在高盐、低温缺氧、光照不足的环境中,使得海洋多糖往往具有比陆生多糖更为独特的生物活性[4-5]。但由于多糖类物质具有粘度大、分子量大、结构复杂、溶解性差、不利于人体吸收利用等缺点,所以其应用范围变得很狭窄[6]。因此,通过化学法、物理法或酶法破坏多糖糖苷键制备寡糖或低聚糖,研究分子量较低的寡糖或低聚糖的制备方法、结构及生物活性具有重要意义。
海洋寡糖是由海洋动物多糖和藻类多糖经过降解得到的小分子糖链,并且不同的降解方法会产生结构类型和生理活性不同的海洋寡糖[7-9]。与多糖相比,海洋寡糖具有生物活性强、相对分子量低、溶解性好、易于被人体吸收等特点,一直是糖化学、糖生物学及糖药物学的研究热点[10]。本综述主要对近几年海洋寡糖的制备和生理活性进行了回顾,以期为海洋寡糖的进一步研究与开发提供理论依据。
1. 海洋寡糖的制备
1.1 化学法降解
通过化学法降解制备海洋寡糖是最传统的降解方法,也是研究最广泛的降解方法,即在反应体系中加入各种化学试剂使多糖糖苷键发生断裂,从而使相对分子量降低形成寡糖的降解方法。降解产物分子量受反应中试剂浓度、时间和温度的影响[11-13]。目前,化学法降解制备海洋寡糖的主要方法为酸降解和氧化降解。
酸法降解是化学法降解中常用的降解方法,指的是通过向反应体系中加入酸性试剂使多糖糖苷键发生断裂,并控制反应温度、反应时间从而获得低分子量寡糖的降解方法,其常用的酸性试剂有盐酸、硝酸、浓硫酸、甲酸、乙酸、草酸等[14-16]。最早使用此方法降解海洋多糖的是Haug等[17],在100 ℃条件下,以海藻酸钠为原料,用1 mol/L草酸对其进行水解,结果表明,海藻酸钠的水解率约为30%,酸沉淀(pH2.85)后分离得到可溶和不可溶的两个组分,进一步水解研究发现,两个组分海藻酸钠的不同溶解性与其糖醛酸种类有关,可溶组分80%~90%为甘露糖醛酸;不可溶组分80%~90%为古罗糖醛酸。孙冲等[18]使用固相酸(活化后的732#阳离子交换树脂)对鲍鱼脏器多糖进行降解,通过响应面法对其降解工艺进行优化,确定最佳水解条件为:树脂用量40 g,水解时间3 h,水解温度70 ℃,此条件下多糖降解率为80.69%,红外光谱分析表明,鲍鱼脏器寡糖含有吡喃环,为α-型糖。秦玲等[19]分别采用不同浓度的三氯乙酸(TFA)和盐酸(HCl)对绿藻多糖CH1-1进行降解,选取盐酸浓度为0.1 mol/L,在80 ℃下降解3 h,并通过Bio-Gel P4凝胶色谱柱对寡糖混合物进行分离纯化,制备得到聚合度为1~8的硫酸阿拉伯寡糖。酸法降解成本低,技术成熟,但反应过程剧烈,易对降解产物活性造成影响[20]。
相比于酸法降解,氧化法降解是一种更温和的多糖降解方法,同时,氧化法降解产生的副产物和污染物较少,但也存在降解工艺复杂、降解反应不稳定及重复性差的问题。常用的氧化剂有过氧化氢、次氯酸钠等,其原理是利用氧化剂在反应体系中生成游离羟基自由基使多糖糖苷键发生断裂[21-22]。其中过氧化氢水解多糖是氧化水解中最主要的方法,具有成本低、产率高、绿色环保、易于工业化生产等优点。Wu等[23]利用过氧化氢制备水溶性牡蛎寡糖,通过对多糖降解条件优化,确定最佳降解条件为:过氧化氢浓度25%、反应时间3 h和温度85 ℃,寡糖的最大产量为10.61%,相比多糖具有更强的抗氧化活性。王灵昭等[24]研究利用过氧化氢降解水不溶性条斑点紫菜多糖,结果表明,在过氧化氢质量分数1.8%,温度60 ℃,时间6 h时,多糖降解效果最佳,通过液相色谱分析发现降解产物中包括3种寡糖组分,含有蛋白质2.12%、总糖93.66%。类Fenton反应降解多糖也是氧化降解多糖的一种方法,Li等[25]利用改良Fenton体系对海参岩藻糖基化硫酸软骨素进行降解,研究过氧化氢和Cu2+浓度、反应时间、反应温度和反应体系pH对多糖降解产物分子量的影响,通过实验选择过氧化氢浓度200 mmol/L、Cu2+浓度0.2 mmol/L、反应温度55 ℃和体系pH6为最佳多糖降解条件,并通过控制反应时间(1、3、5 h)得到三组降解产物,分子量分别为7.4、5.2和4.3 kDa。过氧化氢法降解的产物活性高,是一种环境友好型的多糖降解方法。
1.2 物理法降解
物理法降解是一种绿色降解海洋多糖的方法。目前,用于海洋寡糖制备的物理降解法主要有超声降解法和微波降解法,相比于其他方法,物理降解法具有操作简单、化学试剂用量少、污染少等特点,但是降解产物的得率低,所以一般不单独使用,常与化学法降解联合使用[26-27]。段科等[28]研究微波辅助盐酸和过氧化氢降解浒苔多糖,确定最佳降解条件为:盐酸浓度1 mol/L,过氧化氢浓度5%,降解时间10 min、降解温度50 ℃、微波功率900 W,在此条件下浒苔多糖降解率为77.88%,平均分子质量由84.02 ku下降到了53.59 ku,其抗氧化活性明显高于未降解浒苔多糖,对羟基自由基的清除率为61.51%。凌绍梅等[29]使用超声辅助过氧化氢法降解岩藻聚糖,通过利用50 ku超滤膜将降解产物分为>50 ku和<50 ku 2个组分,并研究其抗菌生物活性,研究表明,分子量相同情况下,降解2 h得到的低分子量岩藻聚糖抑菌效果好于降解4 h。降解相同时间的情况下,分子量大于50 ku的抑菌效果好于分子量小于50 ku的,分子量大于50 ku的降解产物表现出了更好的抑菌活性。此外,Li等[30]利用超声辅助非金属Fenton体系(过氧化氢/抗坏血酸)快速制备低分子量海参糖胺聚糖,研究了反应温度、抗坏血酸浓度及超声强度对降解片段分子量的影响,并通过傅里叶红外光谱、核磁共振谱分析确定其化学组成。结果表明,超声的机械作用会使多糖聚合物暴露更多的活性位点,这就导致了其更易与羟基自由基发生反应,从而可以更高效地降解硫酸化多糖,进一步的结构分析表明,硫酸化多糖的基本结构在解聚过程中几乎没有变化,羟基自由基优先裂解多糖骨架中的GlcA。
物理降解法具有操作简单、无污染等优势,但单独使用多糖的降解效率低,因此常将物理降解法与酸降解法、过氧化氢降解法等其他方法进行联合使用,以显著提升其降解效率及产物活性,大大增加物理降解法工业化生产的潜力[31]。
1.3 酶法降解
酶法降解是制备海洋寡糖的有效方法,目前,酶法降解可以分为特异性酶法降解和非特异性酶法降解,其中特异性酶不易获得、成本高,而非特异性酶易于获得、成本低,但需要大量研究进行筛选[32]。Boucelkha等[33]利用F. multivorum褐藻胶裂解酶对褐藻中的海藻酸钠进行部分酶解,结果表明,F. multivorum褐藻胶裂解酶是一种古罗糖醛酸裂解酶,它只作用于古罗糖醛酸片段,通过HPAEC测定后发现,降解后的海藻酸钠寡糖具有较高的刚性和粘度。邓宇峰等[34]利用酶法对龙须菜琼胶寡糖的制备工艺进行研究,通过纤维素酶和琼胶酶直接对龙须菜进行酶解,简化了寡糖制备工艺,并通过正交试验优化酶解条件,最佳酶解工艺为:底物浓度0.5%、酶解温度45 ℃、pH6.5、琼胶酶加酶量10 U/mL、纤维素酶加酶量6.5 U/mL、颗粒大小为过40~60目筛、酶解时间5 h,此条件下水解度为56.6%,还原糖含量为4.652 mg/mL。此外,Yu等[35]用海洋黄杆菌CZ1127岩藻聚糖酶制备海参岩藻低聚糖,通过液相色谱-质谱联用技术测定酶解产物的寡糖组成,并对酶解产物进行分离纯化,最后通过ESI-CID-MS/MS技术确定酶解产物结构组成。结果表明,酶解产物中主要含有四种低聚糖,且四种寡糖的结构非常相似,为酶法制备海参岩藻低聚糖的研究提供理论基础和实验参考。
相比于化学法和物理法,酶法降解具有降解条件温和,降解过程绿色环保,降解产物得率高、活性高、均一性好等特点,但适合多糖降解的酶种不易获得,存在酶活性低、稳定性差等缺点,达不到工业化生产的要求[36]。因此,深入研究和开发高活性的多糖降解酶尤为重要。以上各种海洋寡糖制备方法的优缺点见表1。
2. 海洋寡糖生理活性
2.1 抗氧化活性
研究发现,周围环境及人体自我新陈代谢会产生自由基,自由基活性强易与人体内生物大分子发生反应,造成健康细胞和组织的损伤。Falkeborg等[37]利用海藻酸裂解酶制备海藻酸钠寡糖并研究其抗氧化活性,研究发现在铁诱导的乳化亚油酸氧化过程中,海藻酸钠寡糖具有良好的抗氧化活性,并能完全抑制TBARS的形成,且海藻酸钠寡糖的抗氧化活性高于抗坏血酸,抑制率可达89%。进一步的自由基清除活性分析表明,海藻酸钠寡糖可以清除稳定的ABTS自由基(ABTS+·)以及羟自由基(·OH)和超氧阴离子自由基(
⋅O−2 ),且分子量低于1000 kDa的海藻酸钠寡糖具有较好的自由基清除能力,对ABTS+·、·OH和⋅O−2 清除率分别高达99.5%、90%和87%。Ramos等[38]研究发现,具有较低G/M比(α-L-聚古罗糖醛酸/β-D-聚甘露糖醛酸)的海藻酸钠寡糖表现出更好的DPPH·清除活性,表明分子量和G/M比例是控制海藻酸钠寡糖抗氧化性能的重要因素。此外,不同的制备方法也会影响海藻酸盐寡糖抗氧化活性[39]。卡拉胶寡糖具有显著的体外抗氧化活性,不同降解方法会产生不同的卡拉胶寡糖,并会导致聚合度(DP)、还原糖和硫酸根含量及末端结构发生改变,从而影响其抗氧化活性,其中,通过氧化水解的卡拉胶寡糖具有更强的抗氧化活性[40]。Zhang等[41]通过琼胶酶水解江蓠琼胶,研究不同聚合度(DP)水解产物对ABTS自由基、DPPH自由基、羟基自由基、超氧阴离子自由基和Fe3+的清除能力,结果发现DP3的琼胶寡糖对ABTS自由基和超氧阴离子自由基的抗氧化效果最好,DP5的琼胶寡糖对Fe3+、DPPH自由基和羟基自由基的清除率最高,DP8的琼胶寡糖抗氧化能力最差。Liu等[42]利用酸法从绿藻Ulva lactuca和Enteromorpha prolifera中提取硫酸寡糖ULO和EPO,研究ULO和EPO对SAMP8小鼠的抗衰老作用及其潜在机制,研究发现经过降解后的寡糖能够有效减少SAMP8小鼠细胞的氧化损伤,保护脑神经元,起着重要的抗衰老作用。进一步研究发现,ULO和EPO的单糖组成、硫酸根含量以及分子量大小影响了其预防衰老的效果,其中高硫酸根含量的ULO具有很好的预防细胞凋亡的作用。相比于大分子量的海洋多糖,低分子量的海洋寡糖具有更高的抗氧化能力,并且海洋寡糖的抗氧化能力还与其制备方法及结构组成有关,因此,抗氧化活性更强的海洋寡糖可作为抗氧化剂应用于保健、医学、化妆品等领域中,具有广阔的的应用前景。
2.2 抗肿瘤活性
恶性肿瘤又称癌症,现已成为当前危害生命健康的重大疾病之一,大量国内外研究表明海洋寡糖具有抗肿瘤作用。Chen等[43]利用酶法降解海藻酸钠,研究不同聚合度(DP)海藻酸钠寡糖对骨肉瘤(OS)术后患者的抗肿瘤作用,研究发现DP5海藻酸钠寡糖在体外对骨肉瘤的生长具有明显的抑制作用,并且可以通过增加血清中SOD和GSH提高骨肉瘤患者的抗氧化能力,通过降低血清中IL-1β和IL-6改善骨肉瘤患者的抗炎能力,从而进一步抑制患者骨肉瘤病情恶化。此外,藻酸盐寡糖还可通过抑制miR-29b的表达水平,影响Toll样受体(TLR)信号传导发挥其抗肿瘤活性[44]。壳寡糖对癌细胞有一定的抑制效果,Zou等[45]研究壳寡糖对原位肝肿瘤的抑制作用和免疫调节作用,研究发现壳寡糖可抑制HepG2细胞的生长、侵袭和转移,并且诱导S噬菌体阻滞,促进细胞凋亡。进一步研究发现壳寡糖通过调节NF-κB信号通路抑制肝癌,并且该信号通路与PI3K/Akt、p53及p38 MAPK信号通路相互作用。一方面,壳寡糖激活巨噬细胞中的NF-κB信号通路活性,并增强免疫功能;另一方面,壳寡糖通过使HepG2细胞中的NF-κB信号通路失活来抑制肝肿瘤,从而抑制p38 MAPK、PI3K/Akt信号通路活化并促进p53信号通路活化。此外,海参来源的岩藻糖化硫酸软骨素具有不同的侧链岩藻糖基化修饰,表现出较强的生物活性。Li等[30]发现从美国肉参中提取岩藻糖化硫酸软骨素及其降解产物具有抗肿瘤活性,对天然多糖和降解片段进行MTT和细胞迁移实验分析表明,低分子量岩藻糖化硫酸软骨素对A549细胞表现出更高的抗肿瘤活性。综上所述,海洋寡糖具有良好的抗肿瘤活性,可通过增强机体免疫能力及抗氧化能力,提高其抗肿瘤活性,并且海洋寡糖的抗肿瘤活性强弱也与其结构组成有关。因此,海洋寡糖可作为潜在的抗肿瘤药物,具有可观的发展前景。
2.3 免疫调节活性
免疫调节功能不足会导致人体更易产生疾病,并且多数癌症的发生都与免疫调节功能不足有关[46]。海洋寡糖具有结构类型多样、机体内靶点多等特点,故增强机体免疫调节能力一直是海洋寡糖活性研究热点之一[6]。Yuan等[47]采用不同浓度(50、100和200 mg/g)卡拉胶寡糖对S180荷瘤小鼠灌胃,研究卡拉胶寡糖对S180荷瘤小鼠免疫系统的影响,研究发现卡拉胶寡糖可以提高小鼠巨噬细胞吞噬作用,加快脾细胞分泌抗体,加速脾淋巴细胞增殖以及提高小鼠NK细胞活性并呈剂量依赖性,结构表明卡拉胶寡糖具有免疫增强功能。Yao等[48]利用酶法从红藻制备卡拉胶寡糖并制备其脱硫酸盐衍生物(DSK),研究两者对小胶质细胞免疫调节活性的影响,结构表明卡拉胶寡糖和DSK均能抑制脂多糖(LPS)激活小胶质细胞,降低小胶质细胞的细胞活力,促进精氨酸酶和肿瘤坏死因子(TNF-α)的释放,且呈浓度依赖性,但DSK的免疫促进效果弱于卡拉胶寡糖,进一步可以说明卡拉胶寡糖对免疫系统的调节功能与其硫酸基团含量有关。此外,已有研究表明卡拉胶寡糖的免疫调节活性与其硫酸基团含量呈正相关,硫酸基团含量越高,其免疫活性越强[49]。海洋硫酸化寡糖可以刺激巨噬细胞大量产生细胞因子,具有一定的免疫调节作用,Kidgell等[50]通过检测脂多糖(LPS)活化后的RAW264.7鼠巨噬细胞释放炎症介质信号分子的水平,量化绿藻Ulva硫酸寡糖的体外免疫调节作用,研究发现绿藻Ulva硫酸寡糖可以提高巨噬细胞中抗炎因子IL-10和前列腺素E2(PGE2)的含量水平,并具有剂量依赖性,表明绿藻Ulva硫酸寡糖具有一定的体外免疫促进作用。另外,Xu等[51]发现不同多糖降解方式得到的海藻酸钠寡糖在免疫调节活性上有着显著差异,其中酶法降解得到的海藻酸钠寡糖免疫调节效果最优,因其可以激活NF-κB和MAPK信号传导通路,从而能显着提高RAW264.7鼠巨噬细胞中一氧化氮(NO)、活性氧(ROS)和肿瘤坏死因子(TNF-α)的表达,进一步对其结构分析发现,海藻酸钠寡糖的不饱和末端结构、分子大小和M/G比对巨噬细胞的活化起到了重要影响作用。综上所述,海洋寡糖可以调节免疫相关信号通路,提高巨噬细胞的吞噬能力,从而增强机体免疫功能,且其增强作用具有一定的剂量依赖性。因此,海洋寡糖可作为一种天然免疫调节剂用于保健食品行业、医药等领域中,具有重要的研究意义。
2.4 抗炎活性
炎症俗称“发炎”,是机体与促炎因子作用后产生的一种适应性反应,被认为是癌症和其他各种慢性病发病的主要危险因素[52]。Shi等[53]研究发现壳寡糖可以抑制由脂多糖(LPS)诱导IPEC-J2细胞炎症介质的产生,且抑制效果与壳寡糖浓度有关,采用壳寡糖200 μg/mL处理IPEC-J2细胞可以有效抑制炎症细胞因子IL-6和IL-8的分泌和表达,研究其反应机理发现壳寡糖可以有效激活IPEC-J2细胞TLR4表达(TLR4是一种模式识别受体,在炎症反应中起到重要作用)。壳寡糖的抗炎作用还受其分子量大小的影响,Vo等[54]研究两种分子量范围(低于1和1~3 kDa)壳寡糖对脂多糖(LPS)诱导的BV-2小鼠小胶质细胞炎症反应的保护作用,结果发现壳寡糖通过抑制小胶质细胞内核因子κB活化和丝裂原活化蛋白激酶(MAPK)磷酸化,从而抑制细胞内促炎介质的产生,具有抗炎作用,且分子量1~3 kDa的壳寡糖抗炎效果较强。Chung等[55]采用酶法制备低分子量壳寡糖,研究其对过敏性哮喘模型小鼠肺部炎症的保护作用,研究表明低分子量壳寡糖可以显著抑制Th2细胞因子(IL-4、IL-5和IL-13)和促炎性细胞因子的产生。此外,Guo等[56]发现K-卡拉胶寡糖可以显著抑制脂多糖(LPS)诱导的RAW264.7巨噬细胞炎症细胞因子(NO、TNF-α、IL-β、IL-8)及相关炎症基因(mTNF-α、mIL-β、mIL-8)的表达。蛋白质组学分析表明,K-卡拉胶寡糖通过抑制细胞表面LPS的受体CD14,削弱Rel/NF-κB信号通路的传导,保护RAW264.7巨噬细胞免受LPS的感染。另外,已有研究发现,藻酸盐寡糖可抑制RAW264.7巨噬细胞内炎症介质的合成和促炎细胞因子的分泌,表明藻酸盐寡糖也可通过影响巨噬细胞发挥其抗炎作用[57]。综上所述,海洋寡糖可抑制致细胞内炎因子及炎症介质的合成和表达,具有优良的抗炎活性。因此,继续深入研究海洋寡糖的抗炎效果,得到抗炎活性更强的海洋寡糖,有望大大提升其在食品、医药等领域的应用。
2.5 调节肠道微生物
肠道菌群被称为人类的“第二基因组”,越来越受到研究者的关注,但生活中的不良习惯例如滥用抗生素、过度摄入酒精和不良饮食习惯等会导致肠道微生物失调进而引起肥胖症、炎症性肠病、慢性疲劳综合征和癌症等疾病的发生[58-59]。研究发现,壳寡糖可调节肠道中的抗肥胖菌群(Coprobacillus cateniformis和Clostridium leptum),提升高脂饮食小鼠血清中瘦素的水平,抑制小鼠体重的增加,缓解高脂饮食引起的慢性炎症,这表明壳寡糖益生元功效的发挥与肠道微生物密切相关[60]。Li等[61]发现从海参(Isostichopus badionotus和Pearsonothuria graeffffei)中提取的岩藻寡糖(Dfuc-Ib和Dfuc-Pg)可抑制由高脂饮食引起的高脂血症、肥胖症和炎症,并且可以调节小鼠盲肠菌群和结肠菌群改善营养不良。进一步研究发现,不同的磺基化修饰使两种寡糖在生物活性上产生了一定的差异,Dfuc-Pg糖链结构中含4-O-磺基较多,可以作为治疗高脂饮食小鼠代谢综合征和调节肠道菌群的药物,Dfuc-Ib糖链结构中含2-O-磺基较多,可缓解小鼠代谢综合征和肠道菌群失调。Sun等[62]通过模拟人体肠道对K-卡拉胶寡糖(KO3和KO6)的消化,研究其体外发酵特性和其发酵上清液的致炎作用,研究发现K-卡拉胶寡糖非常容易降解,并对短链脂肪酸(SCFA)的产生和肠道菌群的组成表现出显著影响,KO3和KO6均能显著促进促炎细菌Prevotella和抑制消炎细菌Bacteroides和Parabacteroides,其中KO3改善了短链脂肪酸的产生并显著促进了肠道中双歧杆菌(Bifidobacterium)和乳酸杆菌(Lactobacillius)的生长,KO6则降低短链脂肪酸的生成并显著提升黏蛋白降解菌Prevotellaceae的丰度,从肠道微生物的角度解释了K-卡拉胶寡糖的致炎作用。此外,Zhang等[63]利用人体粪便研究了江蓠硫酸多糖(GLP)及其琼胶寡糖(GLO)的体外发酵特性,在体外发酵过程中,GLP和GLO都增加了体系中短链脂肪酸的浓度,并调节了粪便微生物的组成和多样性,但GLP增加了拟杆菌门(Bacteroidetes)的丰度,降低了厚壁菌门(Firmicutes)的丰度,而GLO增加了厚壁菌门(Firmicutes)和酸杆菌门(Actinobacteria)的丰度,这为琼胶寡糖作为功能食品中益生元提供了理论依据。
大量的体内、体外实验表明,海洋寡糖对肠道微生物的组成有着显著影响,海洋寡糖能够改善肠道菌群结构和丰度,促进有益菌的生长,降低致病菌的相对丰度。因此,深入研究海洋寡糖对肠道菌群的影响作用及机制,能够为海洋寡糖相关保健品的开发提高理论依据。
2.6 其他活性
除了上述生物活性外,海洋寡糖还具有许多其他的生理功能,例如细胞保护作用、调节动植物生长作用及降血脂作用等。阿霉素(DOX)是一种高效的化学治疗剂,但阿霉素具有剂量依赖性的心脏毒性,其使用剂量受到限制,Guo等[64]研究发现海藻酸钠寡糖可抑制DOX的急性心脏毒性,经海藻酸钠寡糖处理后的被DOX损伤小鼠存活率明显增加,海藻酸钠寡糖可改善DOX引起的心脏功能障碍,并减弱DOX引起的心肌细胞凋亡。此外,海藻酸钠寡糖可通过阻碍p38MAPK/NF-κB信号通路,抑制pp38MAPK蛋白的表达,预防和治疗肺动脉高压(PH)[65]。另外,海藻酸钠寡糖还可以增强普通小麦对干旱环境的耐受性并促进其根部生长[66]。非甾体类抗炎药(NSAIDs)通常在临床医学中使用,会引起胃肠道糜烂、溃疡和出血,Higashimura等[67]发现琼胶寡糖可促进巨噬细胞血红素加氧酶(HO)的表达,口服琼胶寡糖可预防由NSAID引起的肠道损伤和炎症。在水产养殖中,琼胶寡糖被用作饲料添加剂,可以提高鱼虾等水产的免疫力,郭娜等[68]通过酶法从海带中提取琼胶寡糖并将其添加到海参饲料中,发现饲喂添加琼胶寡糖的饲料可促进海参体内碱性磷酸酶(AKP)和酸性磷酸酶(ACP)的生成,表明琼胶寡糖可作为水产养殖中的免疫增强剂。Shu等[69]发现低分子量岩藻聚糖可抑制由IL-1β刺激的类风湿关节炎成纤维样滑膜细胞的活性并可诱导其凋亡,提示低分子量岩藻聚糖对类风湿关节炎的潜在治疗作用。此外,岩藻寡糖还具有降血脂活性,Li等[70]研究发现岩藻寡糖可促进脂肪组织过氧化物酶体增殖物激活受体γ(PPARγ)mRNA的表达,并同时抑制瘦素、aP2和F4/80的mRNA表达,研究表明岩藻寡糖可通过减少脂质合成和促进脂质分解调节血脂异常,表现出良好的降血脂活性。
3. 展望
海洋生物现已成为寡糖的重要来源之一。海洋寡糖可通过酸降解法、氧化降解法、物理降解法和酶降解法等方法制备,不同降解方法具有不同特点,其中化学法降解是制备海洋寡糖最传统的降解方法,具有成本低、技术成熟等优点,但易腐蚀设备,对环境有一定污染。物理降解法具有操作简单、试剂用量少等特点,但是单独使用降解效果差,常与化学降解法联合使用。酶法降解具有高效、特异性强等特点,但特异性酶成本高,不易获得,因此研究筛选非特异性多糖降解酶就显得尤为重要。
此外,海洋寡糖也因其独特结构和生理活性越来越受到研究者们的关注,虽然已有大量国内外研究表明海洋寡糖具有抗氧化、免疫调节、抗肿瘤、调节肠道菌群、抗炎等许多活性,但尚未阐明其生物活性作用机理的细节,有待进一步研究。因此,未来还需加强对其作用机理的研究,以期开发出海洋寡糖的新型海洋功能性食品,并在食品、农业和医学等领域发挥其重要作用。
-
[1] Zhu B W, Ni F, Xiong Q, et al. Marine oligosaccharides originated from seaweeds: Source, preparation, structure, physiological activity and applications[J]. Critical Reviews in Food Science and Nutrition,2021,61(1):60−74. doi: 10.1080/10408398.2020.1716207
[2] 张柯柯, 刘伟治, 律倩倩. 海洋微生物来源的岩藻多糖降解酶[J]. 微生物学通报,2018,45(9):2054−2062. [Zhang K K, Liu Z W, Lyu Q Q. Fucoidan-degrading enzymes from marine microorganisms[J]. Microbiology China,2018,45(9):2054−2062. [3] 张磊, 王锦旭, 杨贤庆, 等. 海洋动物多糖的研究进展[J]. 食品工业,2018,39(1):211−215. [Zhang L, Wang J X, Yang X Q, et al. Research progress of marine animal polysaccharides[J]. The Food Industry,2018,39(1):211−215. [4] Zhao J, Yang J F, Song S, et al. Anticoagulant activity and structural characterization of polysaccharide from abalone(Haliotis discus hannai Ino) gonad[J]. Molecules(Basel, Switzerland),2016,21(6):697−708. doi: 10.3390/molecules21060697
[5] 李俊慧, 李珊, 胡亚芹, 等. 食源性海洋硫酸多糖的神经保护构效机理研究进展[J]. 中国食品学报,2017,17(4):155−164. [Li J H, Li S, Hu Y Q, et al. Neuroprotection mechanism of sulfated polysaccharides from marine food: A review[J]. Journal of Chinese Institute of Food Science and Technology,2017,17(4):155−164. [6] 赵小亮, 王钰婷, 肖宁, 等. 海洋寡糖及其衍生物活性的研究进展[J]. 生物技术进展,2018,8(6):477−488. [Zhao X L, Wang Y T, Xiao N, et al. Progress on activities of marine oligosaccharides and their derivatives[J]. Current Biotechnology,2018,8(6):477−488. [7] Shen J J, Chang Y G, Dong S G, et al. Cloning, expression and characterization of a ι-carrageenase from marine bacterium Wenyingzhuangia fucanilytica: A biocatalyst for producing ι-carrageenan oligosaccharides[J]. Journal of Biotechnology,2017,259:103−109. doi: 10.1016/j.jbiotec.2017.07.034
[8] Shi D, Qi J, Zhang H, et al. Comparison of hydrothermal depolymerization and oligosaccharide profile of fucoidan and fucosylated chondroitin sulfate from Holothuria floridana[J]. International Journal of Biological Macromolecules,2019,132:738−747. doi: 10.1016/j.ijbiomac.2019.03.127
[9] 曹佳淋, 辛妍娇, 汤顺清. 琼脂寡糖的制备及其对免疫细胞的作用[J]. 材料科学与工程学报,2016,34(6):890−894. [Cao J L, Xin Y J, Tang S Q. Preparation of agaro-oligosaccharides and their effect on immune cells[J]. Journal of Materials Science and Engineering,2016,34(6):890−894. [10] 于广利, 谭仁祥. 海洋天然产物与药物研究开发[M]. 北京: 科学出版社, 2016: 222−228. Yu G L, Tan R X. Marine natural products research and drug development[M]. Beijing: Science Press, 2016: 222−228.
[11] Ouyang J M, Wang M, Lu P, et al. Degradation of sulfated polysaccharide extracted from algal Laminaria japonica, and its modulation on calcium oxalate crystallization[J]. Materials Science & Engineering C,2010,30(7):1022−1029.
[12] Kalitnik A A, Marcov P A, Anastyuk S D, et al. Gelling polysaccharide from Chondrus armatus and its oligosaccharides: The structural peculiarities and anti-inflammatory activity[J]. Carbohydrate Polymers,2015(115):768−775.
[13] Liu X, Hao J J, Zhang L J, et al. Activated AMPK explains hypolipidemic effects of sulfated low molecular weight guluronate on HepG2cells[J]. European Journal of Medicinal Chemistry,2014,85(15):304−310.
[14] 刘雪, 王姝垚, 曹素健, 等. 海洋硫酸鼠李寡糖的制备研究[J]. 中国海洋药物,2017,36(6):18−22. [Liu X, Wang S Y, Cao S J, et al. Research on the preparation of marine sulfated rhamno-oligosaccharides[J]. Chinese Journal of Marine Drugs,2017,36(6):18−22. [15] Tommeraas K, Varum K M, Christensen B E. Preparation and characterisation of oligosaccharides produced by nitrous acid depolymerisation of chitosans[J]. Carbohydrate Research,2001,333:137−144. doi: 10.1016/S0008-6215(01)00130-6
[16] 王浩贤. 聚甘露糖醛酸和聚古罗糖醛酸纯化及降解产物活性研究[D]. 青岛: 中国海洋大学, 2012: 10−12. Wang H X. The purification of polymannuronic acids and polyguluronic acids as well as the research on the activity of the oligosaccharides of algin series[D]. Qingdao: Ocean University of China, 2012: 10−12.
[17] Haug A, Bjørn Larsen. A study on the constitution of alginic acid by partial acid hydrolysis[J]. Acta Chemica Scandinavica,1966,5:271−277.
[18] 孙冲, 杜阿珠, 姚昱锟, 等. 响应面法优化固相酸水解鲍鱼脏器多糖工艺优化[J]. 食品工业科技,2020,41(11):171−177. [Sun C, Du A Z, Yao Y K, et al. Optimization of solid phase acid hydrolysis of polysaccharide from abalone viscera by response surface methodology[J]. Science and Technology of Food Industry,2020,41(11):171−177. [19] 秦玲, 孙辉, 刘志纯, 等. 绿藻多糖CH1-1的可控降解及其寡糖的制备研究[J]. 中国海洋药物,2019,38(1):23−27. [Qin L, Sun H, Liu Z C, el al. Research on the controlled degradation of the green alga polysaccharide CH1-1 and preparation of the oligosaccharides[J]. Chinese Journal of Marine Drugs,2019,38(1):23−27. [20] 邰宏博, 唐丽薇, 陈带娣, 等. 褐藻胶寡糖制备的研究进展[J]. 生命科学研究,2015,19(1):75−79. [Tai H B, Tang L W, Chen D D, et al. Progresses on preparation of alginate oligosaccharide[J]. Life Science Research,2015,19(1):75−79. [21] Courtois J. Oligosaccharides from land plants and algae: Production and applications in therapeutics and biotechnology[J]. Current Opinion in Microbiology,2009,12(3):261−273. doi: 10.1016/j.mib.2009.04.007
[22] Kim K J, Lee O H, Lee B Y. Low-molecular-weight fucoidan regulates myogenic differentiation through the mitogen-activated protein kinase pathway in C2C12 cells[J]. British Journal of Nutrition,2011,106(12):1836−1844. doi: 10.1017/S0007114511002534
[23] Wu S, Huang X. Preparation and antioxidant activities of oligosaccharides from Crassostrea gigas[J]. Food Chemistry,2017,216:243−246. doi: 10.1016/j.foodchem.2016.08.043
[24] 王灵昭, 史辰娟, 汪维喜, 等. 过氧化氢降解水不溶性条斑紫菜多糖[J]. 食品与发酵工业,2018,44(3):204−208. [Wang L Z, Shi C J, Wang W X, et al. Degradation of water-insoluble polysaccharide from Porphyra yezoensis by hydrogen peroxide[J]. Food and Fermentation Industries,2018,44(3):204−208. [25] Li J H, Li S, Zhi Z J, et al. Depolymerization of fucosylated chondroitin sulfate with a modified fenton-system and anticoagulant activity of the resulting fragments[J]. Marine Drugs,2016,14(9):170−183. doi: 10.3390/md14090170
[26] Li B, Liu S, Xing R, et al. Degradation of sulfated polysaccharides from Enteromorpha prolifera and their antioxidant activities[J]. Carbohydrate Polymers,2013,92(2):1991−1996. doi: 10.1016/j.carbpol.2012.11.088
[27] Jo B W, Choi S K. Degradation of fucoidans from Sargassum fulvellum and their biological activities[J]. Carbohydrate Polymers,2014,111:822−829. doi: 10.1016/j.carbpol.2014.05.049
[28] 段科, 单虎, 林英庭, 等. 微波辅助盐酸/过氧化氢降解浒苔多糖及其抗氧化活性[J]. 食品科技,2015,40(12):142−147. [Duan K, Shan H, Lin Y T, et al. Degradation of polysaccharide from Enteromorpha prolifera with hydrochloric acid and hydrogen peroxide assisted by microwave and its antioxidant activity[J]. Food Science and Technology,2015,40(12):142−147. [29] 凌绍梅, 吴永沛, 刘翼翔, 等. 低分子量岩藻聚糖制备工艺及其抗菌活性的研究[J]. 食品科技,2014,39(7):184−189. [Ling S M, Wu Y P, Liu Y X, et al. Preparation technology of low-molecular-weight fucoidans and their antibacterial activity[J]. Food Science and Technology,2014,39(7):184−189. [30] Li J H, Li S, Wu L M, et al. Ultrasound-assisted fast preparation of low molecular weight fucosylated chondroitin sulfate with antitumor activity[J]. Carbohydrate Polymers,2019,209:82−91. doi: 10.1016/j.carbpol.2018.12.061
[31] Huber G W, Iborra S, Corma A. Synthesis of transportation fuels from biomass: Chemistry, catalysts, and engineering[J]. Chemical Reviews,2006,106(9):4060−4066.
[32] Belik A A, Silchenko A S, Kusaykin M I, et al. Alginate lyases: Substrates, structure, properties, and prospects of application[J]. Russian Journal of Bioorganic Chemistry,2018,44(4):386−396. doi: 10.1134/S1068162018040040
[33] Boucelkha A, Petit E, Elboutachfaiti R, et al. Production of guluronate oligosaccharide of alginate from brown algae Stypocaulon scoparium using an alginate lyase[J]. Journal of Applied Phycology,2016,29(1):1−11.
[34] 邓宇峰, 林娟, 叶秀云, 等. 龙须菜酶解制备琼胶寡糖的工艺优化[J]. 食品工业,2019,40(5):110−115. [Deng Y F, Lin J, Ye X Y, et al. Process optimization of preparation of agarose oligosaccharides by enzymatic hydrolysis of Gracilaria lemaneiformis[J]. The Food Industry,2019,40(5):110−115. [35] Yu L, Xu X, Xue C, et al. Enzymatic preparation and structural determination of oligosaccharides derived from sea cucumber(Acaudina molpadioides) fucoidan[J]. Food Chemistry,2013,139(1−4):702−709. doi: 10.1016/j.foodchem.2013.01.055
[36] Zhao X M, She X P, Liang X M, et al. Induction of antiviral resistance and stimulary effect by oligochitosan in tobacco[J]. Pestic Biochem Physiol,2006(87):78−84.
[37] Falkeborg M, Cheong L Z, Gianfico C, et al. Alginate oligosaccharides: Enzymatic preparation and antioxidant property evaluation[J]. Food Chemistry,2014,164:185−194. doi: 10.1016/j.foodchem.2014.05.053
[38] Ramos P E, Silva P, Alario M M, et al. Effect of alginate molecular weight and M/G ratio in beads properties foreseeing the protection of probiotics[J]. Food Hydrocolloids,2018,77:8−16. doi: 10.1016/j.foodhyd.2017.08.031
[39] 蒋越, 姚子昂, 陈丰嘉, 等. 藻酸盐寡糖制备工艺及生物活性研究进展[J]. 中国酿造,2018,37(8):19−23. [Jiang Y, Yao Z A, Chen F J, et al. Preparation of alginate oligosaccharides and their biological activities[J]. China Brewing,2018,37(8):19−23. doi: 10.11882/j.issn.0254-5071.2018.08.005 [40] Sun Y J, Yang B Y, Wu Y M, et al. Structural characterization and antioxidant activities of κ-carrageenan oligosaccharides degraded by different method[J]. Food Chemistry,2015,178:311−318. doi: 10.1016/j.foodchem.2015.01.105
[41] Zhang Y H, Song X N, Lin Y, et al. Antioxidant capacity and prebiotic effects of Gracilaria neoagaro oligosaccharides prepared by agarase hydrolysis[J]. International Journal of Biological Macromolecules,2019,137:177−186. doi: 10.1016/j.ijbiomac.2019.06.207
[42] Liu X Y, Liu D, Lin G P, et al. Anti-ageing and antioxidant effects of sulfate oligosaccharides from green algae Ulva lactuca and Enteromorpha prolifera in SAMP8 mice[J]. International Journal of Biological Macromolecules,2019,139:342−351. doi: 10.1016/j.ijbiomac.2019.07.195
[43] Chen J Y, Hu Y, Zhang L R, et al. Alginate oligosaccharide DP5 exhibits antitumor effects in osteosarcoma patients following surgery[J]. Frontiers in Pharmacology,2017,8:623. doi: 10.3389/fphar.2017.00623
[44] Yang Y, Ma Z, Yang G, et a. Alginate oligosaccharide indirectly affects toll-like receptor signaling via the inhibition of microRNA-29b in aneurysm patients after endovascular aortic repair[J]. Drug Design Development & Therapy,2017,11:2565−2579.
[45] Zou P, Yuan S, Yang X, et al. Structural characterization and antitumor effects of chitosan oligosaccharides against orthotopic liver tumor via NF-κB signaling pathway[J]. Journal of Functional Foods,2019,57:157−165. doi: 10.1016/j.jff.2019.04.002
[46] 张胜霞, 吴海歌, 姚子昂, 等. 两种海洋寡糖对S180荷瘤小鼠抗肿瘤及免疫调节作用的研究[J]. 现代免疫学,2012,32(1):5−8. [Zhang S X, Wu H G, Yao Z A, et al. Anti-tumor effect and immunoregulatory activity of two marine oligosaccharides on S180 sarcoma in mice[J]. Current Immunology,2012,32(1):5−8. [47] Yuan H, Song J, Li X, et al. Immunomodulation and antitumor activity of κ-carrageenan oligosaccharides[J]. Cancer Letters,2006,243(2):228−234. doi: 10.1016/j.canlet.2005.11.032
[48] Yao Z A, Xu L, Wu H G. Immunomodulatory function of κ-carrageenan oligosaccharides acting on LPS-activated microglial cells[J]. Neurochemical Research,2014,39(2):333−343. doi: 10.1007/s11064-013-1228-4
[49] Xu L, Yao Z, Wu H, et al. The immune regulation ofκ-car- rageenan oligosaccharide and its desulfated derivatives on LPS- activated microglial cells[J]. Neurochemistry International,2012,61(5):689−696. doi: 10.1016/j.neuint.2012.06.019
[50] Kidgell J T, Glasson C, Magnusson M, et al. The molecular weight of ulvan affects thein vitro inflammatory response of a murine macrophage[J]. International Journal of Biological Macromolecules,2020,150:839−848. doi: 10.1016/j.ijbiomac.2020.02.071
[51] Xu X, Wu X T, Wang Q Q, et al. Immunomodulatory effects of alginate oligosaccharides on murine macrophage RAW264.7 cells and their structure-activity relationships[J]. Journal of Agricultural and Food Chemistry,2014,62(14):3168−3176. doi: 10.1021/jf405633n
[52] 吴哲, 任丹丹, 梁馨元, 等. 褐藻胶寡糖的制备分离及生物活性[J]. 食品安全质量检测学报,2020,11(1):1−7. [Wu Z, Ren D D, Liang X Y, et al. Preparation, separation and biological activities of alginate oligosaccharides[J]. Journal of Food Safety and Quality,2020,11(1):1−7. [53] Shi L, Fang B, Yong Y H, et al. Chitosan oligosaccharide-mediated attenuation of LPS-induced inflammation in IPEC-J2 cells is related to the TLR4/NF-κB signaling pathway[J]. Carbohydrate Polymers,2019,219:269−279. doi: 10.1016/j.carbpol.2019.05.036
[54] Vo T S, Ngo D H, Ta Q V, et al. Protective effect of chitin oligosaccharides against lipopolysaccharide-induced inflammatory response in BV-2 microglia[J]. Cellular Immunology,2012,277(1-2):14−21. doi: 10.1016/j.cellimm.2012.06.005
[55] Chung M J, Park J K, Park Y I. Anti-inflammatory effects of low-molecular weight chitosan oligosaccharides in IgE-antigen complex-stimulated RBL-2H3 cells and asthma model mice[J]. International Immunopharmacology,2012,12(2):453−459. doi: 10.1016/j.intimp.2011.12.027
[56] Guo J, Han S, Lu X, et al. κ-Carrageenan hexamer have significant anti-inflammatory activity and protect RAW264.7 macrophages by inhibiting CD14[J]. Journal of Functional Foods,2019,57:335−344. doi: 10.1016/j.jff.2019.04.029
[57] 史旭阳. 褐藻胶寡糖的抗炎活性机制研究[D]. 深圳: 深圳大学, 2015: 10−14. Shi X Y. Investigation of the anti-inflammatory activity of alginate-derived oligosaccharides[D]. Shenzhen: Shenzhen University, 2015: 10−14.
[58] Shang Q, Jiang H, Cai C, et al. Gut microbiota fermentation of marine polysaccharides and its effects on intestinal ecology: An overview[J]. Carbohydrate Polymers,2018,179:173−185. doi: 10.1016/j.carbpol.2017.09.059
[59] Marchesi J R, Adams D H, Fava F, et al. The gut microbiota and host health: A new clinical frontier[J]. Gut,2016,65(2):330−339. doi: 10.1136/gutjnl-2015-309990
[60] Tang D, Wang Y H, Kang W Y, et al. Chitosan attenuates obesity by modifying the intestinal microbiota and increasing serum leptin levels in mice[J]. Journal of Functional Foods,2020,64:1−10.
[61] Li S, Li J, Mao G, et al. Effect of the sulfation pattern of sea cucumber-derived fucoidan oligosaccharides on modulating metabolic syndromes and gut microbiota dysbiosis caused by HFD in mice[J]. Journal of Functional Foods,2019,55:193−210. doi: 10.1016/j.jff.2019.02.001
[62] Sun Y J, Cui X Y, Duan M M, et al. In vitro fermentation of κ-carrageenan oligosaccharides by human gut microbiota and its inflammatory effect on HT29 cells[J]. Journal of Functional Foods,2019,59:80−91. doi: 10.1016/j.jff.2019.05.036
[63] Zhang X, Aweya J J, Huang Z X, et al. In vitro fermentation of Gracilaria lemaneiformis sulfated polysaccharides and its agaro-oligosaccharides by human fecal inocula and its impact on microbiota[J]. Carbohydrate Polymers,2020,234:115894. doi: 10.1016/j.carbpol.2020.115894
[64] Guo J J, Ma L L, Shi H T, et al. Alginate oligosaccharide prevents acute doxorubicin cardiotoxicity by suppressing oxidative stress and endoplasmic reticulum-mediated apoptosis[J]. Marine Drugs,2016,14(12):231−243. doi: 10.3390/md14120231
[65] Hu Y, Feng Z, Feng W J, et al. AOS ameliorates monocrotaline-induced pulmonary hypertension by restraining the activation of P-selectin/p38MAPK/NF-κB pathway in rats[J]. Biomedecine & Pharmacotherapie,2019,109:1319−1326.
[66] Zhang Y H, Liu H, Yin H, et al. Nitric oxide mediates alginate oligosaccharides-induced root development in wheat (Triticum aestivum L.)[J]. Plant Physiology & Biochemistry,2013,71:49−56.
[67] Higashimura Y, Naito Y, Takagi T, et al. Preventive effect of agaro-oligosaccharides on non-steroidal anti-inflammatory drug-induced small intestinal injury in mice[J]. Journal of Gastroenterology & Hepatology,2014,29(2):310−317.
[68] 郭娜, 姚子昂, 于国友, 等. 海带酶解产物对海参生长及其免疫相关因子的影响[J]. 中国酿造,2019,38(4):160−164. [Guo N, Yao Z A, Yu G Y, et al. Effects of enzymatic hydrolysate of Laminaria japonica on growth and immune-related factors of sea cucumber[J]. China Brewing,2019,38(4):160−164. doi: 10.11882/j.issn.0254-5071.2019.04.031 [69] Shu Z H, Shi X Z, Nie D Q, et al. Low-molecular-weight fucoidan inhibits the viability and invasiveness and triggers apoptosis in IL-1β-treated human rheumatoid arthritis fibroblast synoviocytes[J]. Inflammation,2015,38(5):1777−1786. doi: 10.1007/s10753-015-0155-8
[70] Li S, Li J, Mao G, et al. Fucosylated chondroitin sulfate oligosaccharides from Isostichopus badionotus regulates lipid disorder in C57BL/6 mice fed a high-fat diet[J]. Carbohydrate Polymers,2018,201:634−642. doi: 10.1016/j.carbpol.2018.08.020
计量
- 文章访问数:
- HTML全文浏览量:
- PDF下载量:





 下载:
下载:
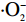
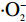
 下载:
下载: 