Screening of Uric Acid-lowering Food and Medicinal Materials Based on Inhibiting Xanthine Oxidase Activity and Zebrafish Hyperuricemia Model
-
摘要: 结合体外(黄嘌呤氧化酶活性抑制)和体内(斑马鱼高尿酸血症模型)方法,对15种食药材乙醇粗提物的降尿酸活性进行筛选。体外实验设置空白组、酶反应组、抑制剂组、对照组,酶标仪295 nm测定吸光度,计算15种食药材对黄嘌呤氧化酶(XOD)活性的抑制率;体内实验随机选取受精后第5 d(5dpf)的斑马鱼,设置空白组、模型组(200 μmol/L PO+10 μmol/L XSS)、食药材给药组(200 μmol/L PO+10 μmol/L XSS+不同浓度提取物)、阳性对照组(200 μmol/L PO+10 μmol/L XSS+APL 2 mmol/L),水溶浸泡,28.5 ℃培养箱中孵育24 h,测定尿酸含量,对具有良好XOD抑制活性的食药材做进一步降尿酸活性验证。体外试验结果表明,15种乙醇粗提物均具有XOD抑制活性,其中8种在400 μg/mL时抑制率达到50%以上,分别为:红景天、兔耳草、牡丹皮、败酱草、黄柏、绿萝花、决明子、雪菊。体内试验结果表明,8种处理组尿酸水平与模型组相比显著降低(P<0.05或P<0.01),均显示出降尿酸活性。
-
关键词:
- 降尿酸 /
- 黄嘌呤氧化酶 /
- 斑马鱼高尿酸血症模型 /
- 活性筛选 /
- 食药材
Abstract: Through the combination of in vitro (the xanthine oxidase inhibitory activity) and in vivo (a zebrafish hyperuricemia model) methods, the uric acid-lowering activity of 15 edible herbs crude ethanol extracts was screened. In vitro experiment set up blank group, enzyme reaction group, inhibitor group and control group. The absorbance at 295 nm with microplate reader was measured. In vivo experiment 5 days post fertilization zebrafish larvae with normal development were randomly divided into blank group, model group (200 μmol/L PO+10 μmol/L XSS), edible herbs group (200 μmol/L PO+10 μmol/L XSS+extracts of different concentrations) and positive control group (200 μmol/L PO+10 μmol/L XSS+APL 2 mmol/L). All groups were cultivated at 28.5 ℃ for 24 h to determine the uric acid contents and further verify the uric acid-lowering activity. In vitro experiment showed that 15 ethanol extracts were inhibitory, with 8 having greater than 50% inhibitory rate at 400 μm/mL. The most active one was the ethanol extracts of the Rhodiola crenulate, which was followed closely by Lagotis brevituba, Poeania suffruticosa, Patrinia scabiosaefolia, Phellodendron chinense, Scindapsus aureus, Cassia tora and Coreopsis tinctorial. In vivo experiment showed that the uric acid level of all these eight extract groups were significantly lower than the model group (P<0.05 or P<0.01). -
高尿酸血症(Hyperuricemia,HUA)与血液中尿酸水平升高有关,是常见的代谢性疾病之一。由于体液中尿酸含量超标,尿酸单钠晶体(MSU)会在关节内以及关节周围形成和沉积[1]。HUA不仅是痛风、急性关节炎、高血压、尿酸性肾病和高脂血症、糖尿病等的重要生化基础,而且还与中风、冠心病和心力衰竭等多种心血管疾病密切相关[2]。近年来,随着生活水平的提高和高蛋白饮食的增加,人们的尿酸水平呈上升趋势[3]。流行病学证据表明,HUA的普遍化已经成为一种亟待解决的公共卫生问题[4]。
尽管当前用于治疗高尿酸血症的化学药物可以快速有效缓解患者的症状,但这些化学药物具有潜在的副作用[5],其中还包括许多不良反应,可导致不同程度的肝损害,神经系统不良反应和其它副作用,因此,有必要寻找更有效,更安全的药物来治疗高尿酸血症和痛风[6]。由于食药材具有安全性高、来源广、种类多、综合疗效好、不良反应少等特点[7],已成为研究降尿酸活性成分的新热点。在本研究中,结合文献调研[8],以中医理论为指导,选取了在传统应用中具有清热利湿,活血化瘀,利尿补虚功效的15种常见的食药材。
常用于筛选降尿酸活性成分的方法分为两种:体外和体内筛选法。常用的体外筛选方法主要是筛选黄嘌呤氧化酶(XOD)抑制剂,而体内筛选方法是通过建立高尿酸血症动物模型进行筛选[9]。因此,首先根据XOD活性抑制,对15种食药材是否具有降尿酸功效进行了体外筛选,然后通过斑马鱼高尿酸血症模型进一步对其降尿酸活性进行验证,为揭示这些食药材降尿酸功效以及进一步开发利用提供科学依据,同时为未来降尿酸活性成分的快速筛选提供新的思路。
1. 材料与方法
1.1 材料与仪器
AB品系野生型斑马鱼 饲养条件:pH7.0~7.6,水温27.5~29 ℃,昼夜光照控制为14 h:10 h,每天喂食丰年虾两次,斑马鱼胚胎孵育在28.5 ℃的恒温培养箱中;本试验使用食药材见表1 来自西藏和北京同仁堂中药店;氧嗪酸钾(PO)、黄嘌呤、黄嘌呤钠盐(XSS)、黄嘌呤氧化酶(X1875)、别嘌呤醇(APL) 美国Sigma公司;Amplex® Red尿酸/尿酸酶检测试剂盒 英潍捷基(上海)贸易有限公司;其余试剂 均为分析纯。
表 1 15种食药材信息Table 1. List of edible herbs used in this study序号 药材名 拉丁名 科名 传统功效 参考文献 1 苍术 Atractylodes lancea (Thunb.)DC. Compositae 抗炎、肝脏保护、抗肿瘤等 [10] 2 决明子 Cassia tora L. Leguminosae 降压、免疫、降血脂等 [11] 3 野菊花 Chrysanthemum indicum L. Compositae 抗炎、抗肿瘤、抑菌等 [12] 4 陆额 Corydalis wuzhengyiana Z. Y. Su et Liden Papaveraceae 抑制黄嘌呤氧化酶活性 [13] 5 雪菊 Coreopsis tinctoria Nutt. Compositae 抗炎、降压、降血脂等 [14] 6 芡实 Euryale ferox Salisb. Nymphaeaceae 抗氧化剂、降血糖、抑菌等 [15] 7 洛神花 Hibiscus sabdariffa Linn. Malvaceae 利尿、抗炎、降压等 [16] 8 兔耳草 Lagotis brevituba Maxim. Scrophulariaceae 抗痛风、抗炎、抗氧化等 [17] 9 百合 Lilium brownii F. E. Brown var. viridulum Baker Liliaceae 抗癌、抗缺氧、抗疲劳等 [18] 10 败酱草 Patrinia scabiosaefolia Fisch. Valerianaceae 抗炎、抗肿瘤、镇静等 [19] 11 黄柏 Phellodendron chinense Schneid. Rutaceae 抗痛风、消炎、退烧等 [20] 12 牡丹皮 Poeania suffruticosa Andr. Ranunculaceae 抗炎、免疫、肝保护等 [21] 13 红景天 Rhodiola crenulate (Hook. f. et Thoms.) H. Ohba Crassulaceae 保护肾脏、抗缺氧、抗疲劳等 [22] 14 雪莲 Saussurea involucrata (Kar. et Kir.) Sch.-Bip. Compositae 抗炎、抗氧化、保护心血管系统等 [23] 15 绿萝花 Scindapsus aureus (Linden ex Andre) Engl. Thymelaeaceae 抗炎、降糖、抗氧化等 [24] 循环水养殖系统 上海海圣生物实验设备有限公司;Multiskan GO型全波长酶标仪 Thermo Fisher公司;S-18KS型手持微量电动组织匀浆器 莱普特科学仪器(北京)有限公司;KQ-600DV数控超声波清洗器 昆山舒美公司。
1.2 实验方法
1.2.1 食药材提取物的制备
各种食药材粉碎成粗粉,称取5.0 g,10倍量75%乙醇,超声提取两次(40 ℃,40 min,480 W,40 kHz),抽滤,合并两次滤液,旋转蒸发浓缩(40 ℃),氮气挥干,分别得到各种食药材提取物。每种提取物分别用乙醇和水复溶,得到乙醇提取物醇溶液和水溶液。
1.2.2 基于XOD活性抑制的体外降尿酸食药材筛选
以黄嘌呤为底物,通过酶标仪检测15种食药材XOD抑制活性。反应设置:空白组、酶反应组、抑制剂组、对照组,每组总体积为200 μL。分组及剂量见表2。将提取物醇溶液和50 μL黄嘌呤共孵育5 min后,加入50 μL XOD引发反应(XOD需要在37 ℃下预孵30 min以稳定酶活),混合均匀,37 ℃,295 nm测定吸光度,所有测定均重复三次。本试验以APL作为阳性对照。
表 2 分组及剂量Table 2. Grouping and dosage组别 2 mmol/L黄嘌呤(μL) XOD
(μL)提取物醇溶液(μL) 磷酸盐缓冲液(μL) 空白组 50 − − 150 酶反应组 50 50 − 100 抑制剂组 50 50 100 − 对照组 50 − 100 50 抑制率(%)=(1−A3−A4A1−A2)×100 式中:A1、A2、A3、A4分别代表酶反应组、空白组、抑制剂组和对照组在295 nm处的吸光度。
1.2.3 基于斑马鱼HUA模型的体内降尿酸食药材筛选
1.2.3.1 构建斑马鱼HUA模型给药剂量的选择
斑马鱼HUA模型构建方法参考文献[25],简述如下:通过PO+XSS水溶给药浸泡5dpf (5days post fertilization,即受精后5 d斑马鱼,28.5 ℃孵育24 h后检测斑马鱼尿酸水平变化,以模型组与空白组相比尿酸含量显著升高作为建模成功的指标。
随机选取5dpf斑马鱼于4个6孔板中,分成8组,每组三个复孔(40尾/孔),每孔容量4 L。空白组:给予等量斑马鱼培养用水;模型组PX2:200 μmol/L PO+10 μmol/L XSS;模型组PX4:400 μmol/L PO+20 μmol/L XSS;模型组PX6:600 μmol/L PO+30 μmol/L XSS;模型组PX8:800 μmol/L PO+40 μmol/L XSS;模型组PX10:1 mmol/L PO+50 μmol/L XSS;模型组PX20:2 mmol/L PO+100 μmol/L XSS;模型组PX40:4 mmol/L PO+200 μmol/L XSS。每组水溶给药浸泡斑马鱼24 h后,测定斑马鱼尿酸水平变化,选择与空白组相比尿酸水平显著升高的浓度作为构建斑马鱼HUA模型给药剂量。
1.2.3.2 每种食药材给药剂量的选择
随机选取5dpf斑马鱼于2个6孔板中,分成6组,每组三个复孔(60尾/孔),每孔容量4 mL。6组:1000、500、100、50、20、10 μg/mL提取物水溶给药浸泡斑马鱼,28.5 ℃培养箱中孵育24 h后,记录各组死亡率。
1.2.3.3 基于斑马鱼高尿酸模型的体内降尿酸食药材筛选
构建斑马鱼HUA模型,对具有良好XOD抑制活性的食药材做进一步降尿酸活性验证。随机选取5dpf斑马鱼于6孔板中,每组三个复孔(40尾/孔),每孔容量4 mL。空白组:等量斑马鱼培养用水;模型组:200 μmol/L PO+10 μmol/L XSS;食药材给药组:200 μmol/L PO+10 μmol/L XSS+不同浓度提取物(每种食药材的给药剂量根据1.2.2.1的结果确定);阳性对照组:200 μmol/L PO+10 μmol/L XSS+APL 2 mmol/L。除空白组外,其余组先用PO和XSS处理斑马鱼,然后加入相应剂量的APL和食药材提取物,每组均为水溶给药浸泡斑马鱼,28.5 ℃培养箱中孵育24 h后,测定尿酸水平。
1.2.3.4 斑马鱼尿酸含量测定
28.5 ℃培养箱中孵育24 h后,收集斑马鱼于1.5 mL EP管中,吸净EP管中的液体,加入40 μL PBS,使用手持匀浆器将收集到的斑马鱼匀浆破碎,直至无明显组织碎块,15000×g,4 ℃,离心15 min;使用Amplex® Red尿酸/尿酸酶检测试剂盒测定斑马鱼尿酸含量。
1.3 数据处理
应用SPSS 24.0统计软件进行统计学分析,以均数±标准偏差(͞x±sd)表示。采用方差分析和t检验来确定其统计学意义(P<0.05,P<0.01)。
2. 结果与分析
2.1 乙醇粗提物对XOD活性的体外抑制
XOD是催化嘌呤代谢最后两个步骤的关键酶,该酶会增加血液中尿酸的积累,抑制XOD活性可以阻断次黄嘌呤向黄嘌呤和黄嘌呤向尿酸的转化,从而有效降低血清尿酸水平,达到预防和治疗高尿酸血症的目的[26],在长期的研究中,XOD已成为治疗HUA的重要靶标。新型XOD抑制剂的开发在HUA治疗领域具有广阔的前景,因此,本研究以XOD为体外筛选的靶标,对15种食药材的降尿酸活性进行了体外初步筛选。
如表3所示,15种食药材的乙醇粗提物均具有XOD抑制活性,其中有8种在浓度400 μg/mL时抑制率达到50%以上,这8种食药材分别是红景天、兔耳草、牡丹皮、败酱草、黄柏、绿萝花、决明子和雪菊,其中红景天XOD抑制活性最强,其IC50值为(140.96±2.76)μg/mL。在测定条件下,阳性药物APL的IC50值为6.769 μg/mL。
表 3 15种食药材XOD抑制率及IC50值Table 3. Percentage of XOD inhibition and IC50 value of 15 edible herbs名称 XOD抑制率(%) IC50(μg/mL) 50(μg/mL) 100(μg/mL) 200(μg/mL) 300(μg/mL) 400(μg/mL) 红景天 10.84±0.25 43.84±1.35 62.53±2.86 94.53±1.00 97.68±0.62 140.96±2.76 兔耳草 14.54±0.47 26.77±0.48 51.04±1.10 69.27±3.06 86.76±1.28 204.93±2.40 牡丹皮 11.12±0.36 29.65±0.58 37.89±2.14 64.53±1.75 77.49±2.52 241.63±6.84 败酱草 11.09±0.59 19.04±0.96 40.20±0.74 50.20±1.30 67.14±0.29 291.57±1.34 黄柏 1.79±0.26 2.50±0.60 18.69±1.86 55.25±5.20 82.13±4.28 294.48±1.10 绿萝花 6.88±0.46 10.40±0.44 25.73±1.07 46.57±6.28 75.45±6.73 302.49±4.88 决明子 11.53±1.12 33.59±0.60 34.91±1.29 48.56±0.88 57.56±0.44 319.68±3.66 雪菊 16.97±0.29 25.94±0.70 29.22±1.98 48.62±1.67 55.49±1.08 343.51±9.47 百合 9.11±0.41 10.31±0.35 22.86±1.05 37.58±0.76 49.52±1.49 − 陆额 7.89±0.22 10.08±0.53 14.72±1.41 26.56±0.50 33.68±1.17 − 野菊花 − 5.97±0.63 13.47±1.69 19.15±0.94 20.51±0.38 − 芡实 − 8.35±0.68 14.99±0.92 14.52±1.18 13.06±0.91 − 洛神花 − 2.95±0.39 12.77±2.52 18.16±0.52 17.09±0.41 − 苍术 − 1.93±0.59 10.29±0.90 11.07±0.69 8.85±0.33 − 雪莲 − 5.64±0.79 11.09±2.14 11.38±0.69 31.43±5.84 − 2.2 构建斑马鱼HUA模型给药剂量的选择
如图1所示,水溶给药PO+XSS浸泡斑马鱼24 h后,测定斑马鱼尿酸水平变化,以模型组与空白组相比尿酸含量出现显著升高作为建模成功的指标。结果显示PX2、PX4和PX6处理组尿酸水平显著高于空白组(P<0.001或P<0.01),其中,PX2处理组尿酸含量最高,斑马鱼存活率100%,此浓度下能够成功构建斑马鱼HUA模型,因此,本实验选择200 μmol/L PO+10 μmol/L XSS作为构建斑马鱼HUA模型给药剂量。
斑马鱼基于其独特的生物学特性,不仅被应用于遗传学和发育生物学研究,而且已经扩展到疾病模型和活性物质筛选领域。通过化学诱导,遗传学和其他方法,研究人员创建了一系列可用于活性物质筛选的斑马鱼人类疾病模型[27]。通过构建斑马鱼高通量活性成分筛选平台,斑马鱼已被广泛用于食药材活性成分和天然化合物的筛选[28]。在之前的工作中,已经成功地构建了斑马鱼高尿酸血症模型[25],该模型可以进行高通量的食药材筛选,基于此使用斑马鱼高尿酸血症模型来筛选具有降尿酸功效的食药材。与现有的动物高尿酸血症模型相比,筛选时间大大缩短,筛选效率提高。
2.3 每种食药材给药剂量的选择
表4统计了8种食药材不同浓度乙醇提取物水溶液浸泡给药24 h后,斑马鱼幼鱼的死亡率。以此作为体内筛选时给药剂量的选择依据。红景天选择一个浓度剂量组:10 μg/mL;牡丹皮选择两个浓度剂量组:10、20 μg/mL;绿萝花选择三个浓度剂量组:10、20、50 μg/mL;决明子选择三个浓度剂量组:20、50、100 μg/mL;雪菊、兔耳草、败酱草、黄柏三个浓度剂量组:50、100、500 μg/mL。
表 4 不同浓度给药组斑马鱼幼鱼死亡率(%)Table 4. Mortalities of zebrafish larvae at different concentrations (%)名称 给药浓度 1000
(μg/mL)500
(μg/mL)100
(μg/mL)50
(μg/mL)20
(μg/mL)10
(μg/mL)雪菊 0 0 0 0 0 0 兔耳草 0 0 0 0 0 0 败酱草 100 0 0 0 0 0 黄柏 0 0 0 0 0 0 决明子 100 100 0 0 0 0 绿萝花 100 100 100 0 0 0 牡丹皮 100 100 100 39.45±2.55 0 0 红景天 100 100 100 100 47.78±2.55 0 2.4 乙醇粗提物对HUA模型斑马鱼尿酸水平的影响
在对15种食药材体外XOD抑制活性验证的基础上,对8种体外抑制效果明显的食药材乙醇粗提物的降尿酸活性做进一步验证。空白组、模型组、食药材给药组、阳性对照组水溶给药浸泡斑马鱼,28.5 ℃培养箱中孵育24 h后,对各处理组的尿酸水平进行测定,结果如图2所示。药物处理24 h后,模型组尿酸水平与空白组相比显著升高(P<0.01),表明模型建立成功。除空白组外,红景天组,兔耳草低中高剂量组,牡丹皮高剂量组,败酱草低中剂量组,黄柏中高剂量组,绿萝花低中高剂量组,决明子低中高剂量组,雪菊低中高剂量组和APL组尿酸水平均显著低于模型组(P<0.05)。除败酱草和决明子以外,其他6种提取物对尿酸水平的影响与浓度呈正相关,与体外XOD活性抑制的实验结果一致。
关于红景天、绿萝花、败酱草和雪菊的XOD抑制活性和降尿酸活性研究很少。其中,红景天和绿萝花降尿酸效果与阳性对照组APL非常接近,表明其降尿酸能力更具有明显的优势。这四种是典型的传统藏药,历史悠久,具有扎实的应用基础,对多种顽固性疾病有良好的疗效。现代医学研究发现这四种中药具有抗炎、抗菌和抗肿瘤作用,并且对代谢疾病(例如糖尿病、高血压和高脂血症)的治疗也具有一定的作用。这四种中药在降尿酸药物的研究中将具有很大的开发价值,其具有降尿酸功效的关键活性化合物也有待进一步分离和提取。
3. 结论
通过体外体内相结合的方法对15种食药材是否具有降尿酸活性进行了筛选,为揭示这些食药材降尿酸功效以及进一步开发利用提供科学依据,随着相关研究的不断深入和完善,斑马鱼高尿酸血症模型在筛选新的降尿酸活性物质方面将具有广阔的实际应用前景。此外,随着关键活性成分的逐渐分离和提取,红景天、绿萝花、败酱草和雪菊在未来降尿酸产品的研发中将具有极好的开发价值。
-
表 1 15种食药材信息
Table 1 List of edible herbs used in this study
序号 药材名 拉丁名 科名 传统功效 参考文献 1 苍术 Atractylodes lancea (Thunb.)DC. Compositae 抗炎、肝脏保护、抗肿瘤等 [10] 2 决明子 Cassia tora L. Leguminosae 降压、免疫、降血脂等 [11] 3 野菊花 Chrysanthemum indicum L. Compositae 抗炎、抗肿瘤、抑菌等 [12] 4 陆额 Corydalis wuzhengyiana Z. Y. Su et Liden Papaveraceae 抑制黄嘌呤氧化酶活性 [13] 5 雪菊 Coreopsis tinctoria Nutt. Compositae 抗炎、降压、降血脂等 [14] 6 芡实 Euryale ferox Salisb. Nymphaeaceae 抗氧化剂、降血糖、抑菌等 [15] 7 洛神花 Hibiscus sabdariffa Linn. Malvaceae 利尿、抗炎、降压等 [16] 8 兔耳草 Lagotis brevituba Maxim. Scrophulariaceae 抗痛风、抗炎、抗氧化等 [17] 9 百合 Lilium brownii F. E. Brown var. viridulum Baker Liliaceae 抗癌、抗缺氧、抗疲劳等 [18] 10 败酱草 Patrinia scabiosaefolia Fisch. Valerianaceae 抗炎、抗肿瘤、镇静等 [19] 11 黄柏 Phellodendron chinense Schneid. Rutaceae 抗痛风、消炎、退烧等 [20] 12 牡丹皮 Poeania suffruticosa Andr. Ranunculaceae 抗炎、免疫、肝保护等 [21] 13 红景天 Rhodiola crenulate (Hook. f. et Thoms.) H. Ohba Crassulaceae 保护肾脏、抗缺氧、抗疲劳等 [22] 14 雪莲 Saussurea involucrata (Kar. et Kir.) Sch.-Bip. Compositae 抗炎、抗氧化、保护心血管系统等 [23] 15 绿萝花 Scindapsus aureus (Linden ex Andre) Engl. Thymelaeaceae 抗炎、降糖、抗氧化等 [24] 表 2 分组及剂量
Table 2 Grouping and dosage
组别 2 mmol/L黄嘌呤(μL) XOD
(μL)提取物醇溶液(μL) 磷酸盐缓冲液(μL) 空白组 50 − − 150 酶反应组 50 50 − 100 抑制剂组 50 50 100 − 对照组 50 − 100 50 表 3 15种食药材XOD抑制率及IC50值
Table 3 Percentage of XOD inhibition and IC50 value of 15 edible herbs
名称 XOD抑制率(%) IC50(μg/mL) 50(μg/mL) 100(μg/mL) 200(μg/mL) 300(μg/mL) 400(μg/mL) 红景天 10.84±0.25 43.84±1.35 62.53±2.86 94.53±1.00 97.68±0.62 140.96±2.76 兔耳草 14.54±0.47 26.77±0.48 51.04±1.10 69.27±3.06 86.76±1.28 204.93±2.40 牡丹皮 11.12±0.36 29.65±0.58 37.89±2.14 64.53±1.75 77.49±2.52 241.63±6.84 败酱草 11.09±0.59 19.04±0.96 40.20±0.74 50.20±1.30 67.14±0.29 291.57±1.34 黄柏 1.79±0.26 2.50±0.60 18.69±1.86 55.25±5.20 82.13±4.28 294.48±1.10 绿萝花 6.88±0.46 10.40±0.44 25.73±1.07 46.57±6.28 75.45±6.73 302.49±4.88 决明子 11.53±1.12 33.59±0.60 34.91±1.29 48.56±0.88 57.56±0.44 319.68±3.66 雪菊 16.97±0.29 25.94±0.70 29.22±1.98 48.62±1.67 55.49±1.08 343.51±9.47 百合 9.11±0.41 10.31±0.35 22.86±1.05 37.58±0.76 49.52±1.49 − 陆额 7.89±0.22 10.08±0.53 14.72±1.41 26.56±0.50 33.68±1.17 − 野菊花 − 5.97±0.63 13.47±1.69 19.15±0.94 20.51±0.38 − 芡实 − 8.35±0.68 14.99±0.92 14.52±1.18 13.06±0.91 − 洛神花 − 2.95±0.39 12.77±2.52 18.16±0.52 17.09±0.41 − 苍术 − 1.93±0.59 10.29±0.90 11.07±0.69 8.85±0.33 − 雪莲 − 5.64±0.79 11.09±2.14 11.38±0.69 31.43±5.84 − 表 4 不同浓度给药组斑马鱼幼鱼死亡率(%)
Table 4 Mortalities of zebrafish larvae at different concentrations (%)
名称 给药浓度 1000
(μg/mL)500
(μg/mL)100
(μg/mL)50
(μg/mL)20
(μg/mL)10
(μg/mL)雪菊 0 0 0 0 0 0 兔耳草 0 0 0 0 0 0 败酱草 100 0 0 0 0 0 黄柏 0 0 0 0 0 0 决明子 100 100 0 0 0 0 绿萝花 100 100 100 0 0 0 牡丹皮 100 100 100 39.45±2.55 0 0 红景天 100 100 100 100 47.78±2.55 0 -
[1] Maiuolo J, Oppedisano F, Gratteri S, et al. Regulation of uric acid metabolism and excretion[J]. International Journal of Cardiology,2016,213:8−14. doi: 10.1016/j.ijcard.2015.08.109
[2] 田青, 王昱, 李哲, 等. 体检人群中尿酸与心血管病危险因素的相关性研究[J]. 中国继续医学教育,2019,11(1):62−65. [3] Liu R, Han C, Wu D, et al. Prevalence of Hyperuricemia and gout in mainland China from 2000 to 2014: A systematic review and meta-analysis[J]. BioMed Research International,2015,2015:762820.
[4] Dehlin M, Jacobsson L, Roddy E. Global epidemiology of gout: prevalence, incidence, treatment patterns and risk factors[J]. Nature Reviews Rheumatology,2020,16(7):1−11.
[5] Gliozzi M, Malara N, Muscoli S, et al. The treatment of hyperuricemia[J]. International Journal of Cardiology,2016,213(1):23−27.
[6] Mttomo S, Hirota M, Fujita T. New xanthine oxidase inhibitors from the fruiting bodies of Tyromyces fissilis[J]. Bioscience Biotechnology and Biochemistry,2019,83(5):1−11.
[7] 张雪, 俸婷婷, 黄俊飞, 等. 降尿酸药物筛选方法学研究进展[J]. 亚太传统医药,2015,11(6):48−50. [8] 许洪波, 周瑞, 谢培, 等. 27种中草药的黄嘌呤氧化酶抑制活性筛选[J]. 时珍国医国药,2017(3):41−42. [9] 子正, 徐琳, 高建东. 高尿酸血症动物模型研究进展[J]. 医学综述,2020,26(8):1462−1466. [10] 李曼玲, 范莉, 冯伟红, 等. 苍术的化学药理研究进展[J]. 中国中医药信息杂志,2002,9(11):79−82. [11] 春晓, 王月明, 韦东来, 等. 决明子的主要化学成分和药理作用研究进展[J]. 现代农业研究,2018(6):47−50. [12] 袁慧杰, 赖志辉, 管艳艳, 等. 野菊花主要活性成分的药理作用研究进展[J]. 中华中医药学刊,2018,36(3):651−653. [13] 卓玛东智, 孙杰, 袁瑞瑛, 等. 罗堆多吉颗粒及组方成分陆额对黄嘌呤氧化酶活性的影响研究[J]. 西藏大学学报(自然科学版),2015,30(1):58−62. [14] 曾晓漫, 贺晓云. 昆仑雪菊的化学成分与功效研究进展[J]. 食品工业科技,2019,40(13):335−339. [15] 杨晓曦, 张庆林. 中药芡实的研究进展[J]. 国际药学研究杂志,2015,42(2):160−164. [16] 顾关云, 蒋昱. 玫瑰茄的药理作用与临床应用[J]. 现代药物与临床,2010,25(3):165−172. [17] 朱继孝, 张红阳, 钟国跃, 等. 藏族药兔耳草属药用植物化学成分与药理作用研究进展[J]. 中国实验方剂学杂志,2017,23(12):214−222. [18] 罗林明, 裴刚, 覃丽, 等. 中药百合化学成分及药理作用研究进展[J]. 中药新药与临床药理,2017,28(6):824−837. [19] 陈淑玲, 韩亮. 败酱草的现代研究进展[J]. 广东药科大学学报,2017,33(6):816−821. [20] 高妍, 周海芳, 刘朵, 等. 黄柏化学成分分析及其药理作用研究进展[J]. 亚太传统医药,2019,15(4):207−209. [21] 李方军. 牡丹皮化学成分及药理作用研究进展[J]. 安徽医药,2004,8(1):9−10. [22] 季宇彬, 耿欣, 汲晨锋. 红景天研究进展[J]. 天津中医药,2007,24(1):81−85. [23] 达娃卓玛. 西藏产雪莲花的化学和药理研究进展[J]. 中国民族民间医药,2015,24(12):25−31. [24] 张晓英, 张致英. 藏药绿萝花药理作用研究进展[J]. 中国民族医药杂志,2017,23(2):51−53. [25] Zhang Y Y, Li Q, Wang F Z et al. A zebrafish (Danio rerio) model for high-throughput screening food and drugs with uric acid-lowering activity[J]. Biochemical and Biophysical Research Communications,2019,508(2):494−498. doi: 10.1016/j.bbrc.2018.11.050
[26] Borges F, Fernandes E, Roleira F. Progress towards the discovery of xanthine oxidase inhibitors[J]. Current Medicinal Chemistry,2002,9(2):195−217. doi: 10.2174/0929867023371229
[27] Delvecchio C, Tiefenbach J, Krause H M. The zebrafish: A powerful platform for in vivo, HTS drug discovery[J]. Assay and Drug Development Technologies,2011,9(4):354−361. doi: 10.1089/adt.2010.0346
[28] 王佑华, 黎晌, 杨彬睿, 等. 斑马鱼模型在中医药研究中的应用现状[J]. 中西医结合学报,2012,10(11):1189−1197.





 下载:
下载:
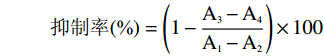


 下载:
下载:
