Study on Anti-hyperuricemia Effect of Ampelopsis grossedentata Extracts
-
摘要: 目的:研究藤茶提取物对高尿酸血症小鼠的降尿酸效果和对肝肾的保护作用。方法:腹腔注射氧嗪酸钾诱导建立高尿酸血症小鼠模型,以藤茶提取物低、中、高剂量(100、200、400 mg/kg)和别嘌呤醇(10 mg/kg)连续灌胃14 d,检测小鼠血清尿酸(Uric acid, UA)、尿素氮(Blood urea nitrogen, BUN)、肌酐(Creatinine, CRE)、天门冬氨酸氨基转氨酶(Aspartate aminotransferase, AST)、谷氨酸氨基转氨酶(Alanine aminotransferase, ALT)和肝脏黄嘌呤氧化酶(Xanthine oxidase, XOD)水平;计算肝肾系数后切片染色,观察肝肾组织的病理学特征。结果:与模型组相比,200和400 mg/kg藤茶提取物组小鼠血清尿酸值分别降低22.65%(P<0.05)和29.15%(P<0.01),显著降低血清肌酐和尿素氮水平(P<0.05), 下调天门冬氨酸氨基转氨酶、谷氨酸氨基转氨酶和肝脏黄嘌呤氧化酶水平(P<0.05),降低肝肾系数;病理组织形态学检查结果发现藤茶提取物对高尿酸血症小鼠肝组织和肾组织有明显改善作用。结论:200、400 mg/kg藤茶提取物对高尿酸血症小鼠有良好的降尿酸效果和肝肾保护作用。Abstract: Objective: To study the effect of Ampelopsis grossedentata extracts on lowering uric acid and protection of liver and kidney in hyperuricemia mice. Methods: Hyperuricemia mice model was induced with potassium oxazinate. Different doses of Ampelopsis grossedentata extracts (100, 200, 400 mg/kg) and allopurinol (10 mg/kg) were intragastricly administered to mice for consecutive 14 days. Levels of uric acid (UA), urea nitrogen (BUN), creatinine (CRE), aspartate aminotransferase (AST), alanine aminotransferase (ALT) in serum, and xanthine oxidase (XOD) level in liver were detected. The liver and kidney coefficients were calculated and the pathological changes of the liver-kidney tissues by HE staining were observed. Results: Compared with the model group, the serum uric acid contents in the doses of 200 and 400 mg/kg decreased by 22.65% (P<0.05) and 29.15% (P<0.01), while CRE and BUN contents were significantly reduced (P<0.05). Meanwhile, the serum AST, ALT and XOD in liver contents decreased (P<0.05) and the liver and kidney coefficients were reduced. The pathological sections showed that Ampelopsis grossedentata extracts could improve the liver and kidney morphology. Conclusion: Ampelopsis grossedentata extracts (200 and 400 mg/kg) could reduce the level of serum uric acid and showed the protective effects on the liver and kidney.
-
Keywords:
- Ampelopsis grossedentata extract /
- hyperuricemia /
- uric acid
-
高尿酸血症(Hyperuricemia,HUA)是体内尿酸生成增加或尿酸排泄减少而导致尿酸水平高于正常值的一种代谢性疾病[1]。高尿酸血症不仅是引发痛风[2]的关键生化指标,还与糖尿病[3]、高血压[4]、慢性肾病[5]、冠心病[6]等疾病密切相关。尿酸是黄嘌呤和次黄嘌呤在黄嘌呤氧化酶(XOD)的参与下代谢的最终产物,而在尿酸的排泄过程中,超过70%的尿酸会通过肾脏排泄[7],黄嘌呤氧化酶异常上调导致嘌呤代谢受阻和尿酸生成增多[8]。目前临床西药治疗高尿酸血症药物主要有抑制尿酸生成药、促进尿酸排泄药和促进尿酸溶解药三类[9],其中一线治疗药物别嘌呤醇为黄嘌呤氧化酶抑制剂,通过抑制尿酸生成而达到降尿酸的目的,但临床上只有不到一半患者可以控制其尿酸水平,且别嘌呤醇的不良反应与HLA-B*5801等位基因阳性率有相关性,有国际组织报道华人对HLA-B*5801的携带率较高[10],因而限制了别嘌呤醇的使用;促进尿酸排泄药物苯溴马隆是通过抑制肾小管对尿酸的重吸收,从而降低血中尿酸浓度,临床用药发现苯溴马隆长期服用会造成肝肾损伤[11],因而寻找到一种副作用小且可安全使用的天然药物具有重大意义。
藤茶为显齿蛇葡萄(Ampelopsis grossedentata(Hand-Mazz)W.T.Wang)的嫩茎叶,始载于《茶经》,是葡萄科蛇葡萄属多年生木质藤本植物[12],主要分布于我国湖南、湖北、云南、贵州、广东、广西、福建等长江以南各省[13]。藤茶即可入药也可食用,民间用其嫩茎叶入茶已有数百年的历史。据《中草药汇编》等文献记载,藤茶入药有清热解毒的功效,可治疗感冒风热、咽喉肿痛等[14]。现代研究表明,藤茶及其提取物具有抗炎[15]、抗菌[16]、抗氧化[17]、降血糖[18]、降血脂[19]、降压[20]等多种药理活性。本实验使用藤茶提取物灌胃氧嗪酸钾诱导的高尿酸血症小鼠模型,对藤茶提取物降尿酸作用进行研究,评价藤茶提取物的降尿酸水平及对肝脏和肾脏组织的影响,为开发藤茶降尿酸作用提供实验依据。
1. 材料与方法
1.1 材料与仪器
SPF级雄性ICR小鼠 体质量(18~22 g),斯贝福(北京)生物技术有限公司,实验动物许可证号:SCXK(京)2019-0010;藤茶提取物(50%的二氢杨梅素和5%的槲皮素) 无锡市世纪生物工程有限公司;别嘌呤醇(批号:20180305) 世贸天阶制药(江苏)有限责任公司;氧嗪酸钾(批号:O0164) 武汉远成共创科技有限公司;羧甲基纤维素钠(CMC-Na) 国药集团化学试剂有限公司;尿酸(UA)、尿素氮(BUN)、肌酐(CRE)、天门冬氨酸氨基转氨酶(AST)、谷氨酸氨基转氨酶(ALT)、黄嘌呤氧化酶(XOD)试剂盒 南京建成生物工程研究所。
Enspire酶标仪 美国PerkinElmer;FC5515R高速冷冻离心机 美国OHAUS;EL-104 分析天平 瑞士梅特勒-托利多;HH-2电热恒温水浴锅 上海皓庄仪器;Eclipse Ci荧光显微镜 日本尼康公司。
1.2 实验方法
1.2.1 高尿酸血症小鼠模型建立
12只ICR雄性小鼠适应性喂养7 d后,随机分为正常组(NC)和模型组(MC),每组6只。第8 d上午,模型组腹腔注射给药氧嗪酸钾(用0.5%羧甲基纤维素钠配制成12 mg/mL乳悬液)进行造模,注射体积为10 g/0.1 mL,连续7 d以制备高尿酸血症模型。造模7 d后,给药1 h后,对小鼠进行眼内眦静脉采血,4 ℃下静置1 h,3500 r/min离心15 min分离血清,待用。
1.2.2 给药方法
以建立的HUA小鼠模型为基础,将48只ICR雄性小鼠随机分为正常对照组(NC)、模型对照组(MC)、别嘌呤醇组(ALLO)、藤茶提取物低(L)、中(M)、高(H)剂量组,共6组,每组8只。确定别嘌呤醇给药剂量为10 mg/kg/d,藤茶提取物低、中、高剂量组对应浓度分别为100、200、400 mg/kg/d。第8~14 d期间,正常组注射生理盐水,其余组注射等体积(300 mg/kg)氧嗪酸钾造模。第15~28 d期间,在正常组与其余各组分别注射生理盐水和氧嗪酸钾1 h后,别嘌呤醇组和藤茶提取物给药组分别灌胃相应剂量别嘌呤醇和藤茶提取物,其中正常组和模型组灌胃等体积(10 g/0.1 mL)生理盐水。
1.2.3 小鼠体重相对变化率
每天观察小鼠的一般情况并在给药前对小鼠进行称重,计算每只小鼠的体重相对变化率(%)=(每日称量体重/实验开始前体重)×100
1.2.4 小鼠肝肾系数
小鼠颈脱臼处死后取其肝脏和肾脏进行称量,计算各组小鼠的肝肾系数,肝肾系数(mg/g)=小鼠脏器(mg)/小鼠体重(g)。
1.2.5 相关指标检测
末次给药1 h后,对小鼠进行摘眼球取血,取血0.5 mL,低温静置1 h后,3500 r/min离心15 min分离血清;取肾脏和肝脏,4%多聚甲醛溶液固定,石蜡包埋,HE染色,病理组织学检测;准确称取肝脏,按试剂盒说明书制备肝脏匀浆。按照试剂盒检测说明书操作测定各组小鼠血清中尿酸(UA)、尿素氮(BUN)、肌酐(CRE)、天门冬氨酸氨基转氨酶(AST)、谷氨酸氨基转氨酶(ALT)和肝脏黄嘌呤氧化酶(XOD)含量。
1.3 数据分析
采用 SPSS 23.0 统计软件对数据进行统计学处理,实验数据以平均值±标准差(
2. 结果与分析
2.1 小鼠体质量相对变化率情况
图1显示,各组小鼠在实验期间,体重相对变化率情况总体呈增长趋势,但与正常组相比,各组间均无统计学差异(P>0.05),说明别嘌呤醇和藤茶提取物对小鼠生长无明显影响。
2.2 小鼠肝肾系数
藤茶提取物对高尿酸血症小鼠脏器系数的影响见表1。与正常组比较,模型组小鼠的肝脏、肾脏系数均有所上升,肝脏系数和肾脏系数具有显著水平(P<0.05)。与模型组相比,别嘌呤醇组肝脏系数和肾脏系数显著降低(P<0.05),藤茶提取物组肝脏、肾脏系数均有所降低,其中200和400 mg/kg藤茶提取物组肾脏指数有显著性差异(P<0.05)。说明藤茶提取物有降低高尿酸血症小鼠肝脏、肾脏指数的作用。
表 1 藤茶提取物对高尿酸血症小鼠脏器系数的影响Table 1. Effects of Ampelopsis grossedentata extract on organ coefficient of HUA mice组别 肝脏系数(%) 肾脏系数(%) NC 7.5907±0.85 2.0237±0.19 MC 7.9295±0.88* 2.4987±0.27* AGEL 7.9078±0.76 2.3199±0.14 AGEM 7.837±0.59 2.1427±0.36# AGEH 7.6305±0.98 2.1287±0.11# ALLO 7.4616±0.63# 2.0291±0.25# 注:与正常组比较,*:P<0.05,**:P<0.01;与模型组比较,#:P<0.05,##:P<0.01。 2.3 对高尿酸血症小鼠血清尿酸(UA)的影响
与正常组相比,模型组组血清尿酸值极显著增加40.3%(P<0.01);与模型组相比,灌胃200和400 mg/kg藤茶提取物后,小鼠血清尿酸值分别降低22.65%(P<0.05)和29.15%(P<0.01),别嘌呤醇组血清尿酸水平显著降低69.15%(P<0.01),灌胃100 mg/kg藤茶提取物有降低小鼠血清尿酸值但无统计学差异,可能是因为100 mg/kg藤茶提取物的血药浓度达不到降低血尿酸的作用,见图2。综上,灌胃不同剂量藤茶提取物对高尿酸血症小鼠的降尿酸作用明显差异,200和400 mg/kg藤茶提取物有良好降尿酸效果。
2.4 对高尿酸血症小鼠血清肌酐(CRE)和尿素氮(BUN)的影响
血清肌酐和尿素氮均通过肾脏进行代谢,临床上常用来评估肾脏损伤程度[21]。藤茶提取物对高尿酸血症小鼠血清肌酐和尿素氮含量的影响见图3。与正常组相比,模型组肌酐和尿素氮水平显著升高(P<0.01);与模型组相比,灌胃100和200 mg/kg藤茶提取物降低肌酐水平(P<0.05),200 mg/kg藤茶提取物显著降低尿素氮水平(P<0.01),400 mg/kg藤茶提取物显著降低肌酐和尿素氮水平(P<0.01);与模型组相比,别嘌呤醇组显著降低尿素氮水平(P<0.01),肌酐水平有降低,但无显著差别。
2.5 对高尿酸血症小鼠血清谷草转氨酶(AST)和谷丙转氨酶(ALT)含量的影响
AST和ALT为临床上诊断肝脏受损程度指标,肝细胞膜通透性增加或肝细胞坏死均可导致ALT和AST水平升高[22]。藤茶提取物对高尿酸血症小鼠血清 AST 和 AST含量的影响见图4。与正常组相比,模型组小鼠血清AST、ALT含量极显著升高(P<0.01);与模型组相比,灌胃100和200 mg/kg藤茶提取物可显著降低AST含量(P<0.05),400 mg/kg藤茶提取物可极显著降低AST含量(P<0.01);灌胃100 mg/kg藤茶提取物可显著降低ALT含量(P<0.05),200和400 mg/kg藤茶提取物可极显著降低ALT含量(P<0.01);别嘌呤醇组可降低AST、ALT含量(P<0.05)。说明藤茶提取物可降低AST、ALT含量,且具有剂量依赖性。
2.6 对小鼠肝脏组织XOD活性的影响
图5表明,与正常组相比,模型组小鼠肝脏组织中XOD活性极显著升高(P<0.01);与模型组相比,别嘌呤醇给药组小鼠肝脏XOD活性极显著降低(P<0.01);灌胃200 mg/kg藤茶提取物可显著降低高尿酸血症小鼠肝脏组织XOD活性(P<0.05),灌胃400 mg/kg藤茶提取物可极显著降低高尿酸血症小鼠肝脏组织XOD活性(P<0.01)。说明藤茶提取物可以降低高尿酸血症小鼠肝脏组织XOD活性。
2.7 小鼠肾组织病理变化
如图6可见,正常组小鼠肾小管细胞整体排列紧密,形态正常且饱满,肾小球结构清楚;模型组小鼠肾小球数量未见明显差异,肾小管上皮细胞空泡变形,轻度炎症浸润;与模型组相比,别嘌呤醇组小鼠肾小管官腔扩张明显,肾小球萎缩变形,炎症细胞浸润;藤茶提取物各剂量组小鼠肾小管形态与模型组相比轻微改善。
![]() 图 6 AGE对氧嗪酸钾诱导的高尿酸血症小鼠肾脏的影响(200×)注:正常组(A);模型组(B);别嘌醇组(C);高剂量组(D);中剂量组(E);低剂量组(F)。图7同。Figure 6. Effects of AGE on the influence of kidney in hyperuricemia mice induced by potassium oxonate(200×)
图 6 AGE对氧嗪酸钾诱导的高尿酸血症小鼠肾脏的影响(200×)注:正常组(A);模型组(B);别嘌醇组(C);高剂量组(D);中剂量组(E);低剂量组(F)。图7同。Figure 6. Effects of AGE on the influence of kidney in hyperuricemia mice induced by potassium oxonate(200×)2.8 小鼠肝组织病理变化
由图7所示,各组肝细胞形态正常,与空白组相比,模型组小鼠肝细胞伴随轻度水肿;与模型组相比,别嘌呤醇组小鼠肝细胞伴随轻度水肿和轻微炎症细胞浸润;藤茶提取物各剂量组小鼠肝细胞无坏死且正常。
3. 讨论与结论
近年来,由于生活方式和饮食结构的改变,高尿酸血症已成为威胁现代人健康的常见疾病[23]。有研究表明高尿酸血症患者的患病率逐年升高,而长期的血尿酸水平过高,不仅引起痛风、肾脏病变和代谢性疾病,患者的AST、ALT等指标水平也高于正常人,其原因可能是尿酸水平通过引起胰岛素抵抗而致代谢性疾病[24]。黄嘌呤氧化酶广泛存在于哺乳动物肝脏中,是嘌呤代谢过程中的关键酶,在尿酸调控过程中发挥重要作用,尿酸是由黄嘌呤氧化酶氧化次黄嘌呤所产生的,再经由肾小管排出体外[25-28]。氧嗪酸钾为一种尿酸酶抑制剂,可特异性阻止尿酸降解,从而升高血清尿酸水平[29]。本实验选用氧嗪酸钾诱导高尿酸血症小鼠模型[30],模型组血尿酸值与正常组相比升高40.3%,表明造模成功。
实验结果显示,与模型相比,藤茶提取物各剂量组对高尿酸血症小鼠的血尿酸含量有明显的降低作用,且不同浓度藤茶提取物的降尿酸效果表现为:400>200>100 mg/kg藤茶提取物。血清肌酐和尿素氮用来反映肾功能情况,谷丙转氨酶和谷草转氨酶则可反映肝功能情况,与正常组相比,模型组血清CRE、BUN、AST、ALT和肝脏XOD含量极显著升高(P<0.01),肝肾系数上升,说明持续的高尿酸水平可能对肾功能和肝功能产生损伤;与模型组相比,藤茶提取物能明显降低血清CRE、BUN、AST、ALT和肝脏XOD水平,同时肝肾系数下降,表明藤茶提取物对肝脏和肾脏有保护作用。藤茶提取物给药组能够降低血清尿酸水平可能是通过降低XOD含量,从而减少尿酸生成或促进尿酸排泄,进而达到降尿酸的效果。病理组织学形态检查发现,别嘌呤醇组的肾组织细胞有明显空泡变化,肝脏细胞有轻微水肿和炎症浸润,而藤茶提取物给药组对肝肾组织损伤明显小于别嘌呤醇,说明藤茶提取物给药组能够有效改善因高尿酸血症而导致的肝肾功能损伤。
综上,藤茶提取物能够明显降低氧嗪酸钾诱导的高尿酸血症小鼠血尿酸水平,且作用与剂量有正相关趋势。其机制可能是通过降低小鼠肝脏XOD活性,从而降低血清尿酸水平,同时对肝肾组织有明显保护作用,但其具体作用机制还需要进一步研究探索,为开发藤茶降尿酸作用提供实验依据。
-
图 6 AGE对氧嗪酸钾诱导的高尿酸血症小鼠肾脏的影响(200×)
注:正常组(A);模型组(B);别嘌醇组(C);高剂量组(D);中剂量组(E);低剂量组(F)。图7同。
Figure 6. Effects of AGE on the influence of kidney in hyperuricemia mice induced by potassium oxonate(200×)
表 1 藤茶提取物对高尿酸血症小鼠脏器系数的影响
Table 1 Effects of Ampelopsis grossedentata extract on organ coefficient of HUA mice
组别 肝脏系数(%) 肾脏系数(%) NC 7.5907±0.85 2.0237±0.19 MC 7.9295±0.88* 2.4987±0.27* AGEL 7.9078±0.76 2.3199±0.14 AGEM 7.837±0.59 2.1427±0.36# AGEH 7.6305±0.98 2.1287±0.11# ALLO 7.4616±0.63# 2.0291±0.25# 注:与正常组比较,*:P<0.05,**:P<0.01;与模型组比较,#:P<0.05,##:P<0.01。 -
[1] 倪青, 孟祥. 高尿酸血症和痛风中医认识与治疗[J]. 北京中医药,2016,35(6):529−535. [Ni Qing, Meng Xiang. TCM understanding and treatment of hyperuricemia and gout[J]. Beijing Journal of Traditional Chinese Medicine,2016,35(6):529−535. [2] Harris M D, Siegel L B, Alloway J A. Gout and hyperuricemia[J]. Am Fam Physician,1999, 59(4):925−934.
[3] Mahbub M H, Yamaguchi N, Takahashi H, et al. Association of plasma free amino acids with hyperuricemia in relation to diabetes mellitus, dyslipidemia, hypertension and metabolic syndrome[J]. Sci Rep,2017,7(1):17616. doi: 10.1038/s41598-017-17710-6
[4] Wang J, Qin T, Chen J, et al. Hyperuricemia and risk of incident hypertension: A systematic review and meta-analysis of observational studies[J]. PLoS One,2014,9(12):e114259. doi: 10.1371/journal.pone.0114259
[5] Chang H Y, Tung C W, Lee P H, et al. Hyperuricemia as an independent risk factor of chronic kidney disease in middle-aged and elderly population[J]. Am J Med Sci,2010,339(6):509−515. doi: 10.1097/MAJ.0b013e3181db6e16
[6] Huang H, Huang B, Li Y, et al. Uric acid and risk of heart failure: A systematic review and meta-analysis[J]. Eur J Heart Fail,2014,16(1):15−24. doi: 10.1093/eurjhf/hft132
[7] Lipkowitz M S. Regulation of uric acid excretion by the kidney[J]. Curr Rheumatol Rep,2012,14(2):179−188. doi: 10.1007/s11926-012-0240-z
[8] Wang C H, Zhang C, Xing X H. Xanthine dehydrogenase: An old enzyme with new knowledge and prospects[J]. Bioengineered,2016,7(6):395−405. doi: 10.1080/21655979.2016.1206168
[9] 孙珊珊, 曲连悦, 杜荣蓉, 等. 高尿酸血症药物治疗研究进展[J]. 中国临床药理学与治疗学,2019,24(5):589−594. [Sun Shanshan, Qu Lianyue, Du Rongrong, et al. Research progress on drug therapy of hyperuricemia[J]. Chinese Journal of Clinical Pharmacology and Therapeutics,2019,24(5):589−594. doi: 10.12092/j.issn.1009-2501.2019.05.017 [10] 关灵, 刘碧波, 廖玉婷, 等. 别嘌醇所致严重皮疹与HLA-B*5801等位基因的相关性[J]. 中国现代药物应用,2016,10(5):7−8. [Guan Ling, Liu Bibo, Liao Yuting, et al. Correlation between allopurinol-induced severe rash and HLA-B*5801 allele[J]. Chinese Journal of Modern Drug Application,2016,10(5):7−8. [11] CFDA. 警惕苯溴马隆的肝损害风险[J]. 上海医药, 2015, 36(5): 39. CFDA. Be alert to the risk of liver damage of benzbromarone[J]. Shanghai Medical & Pharmaceutical Journal, 2015, 36(5): 39.
[12] 冉京燕, 方建国, 谢雪佳, 等. 藤茶的本草资源学研究概况[J]. 中草药,2016,47(20):3728−3735. [Ran Jingyan, Fang Jianguo, Xie Xuejia, et al. Scientific research on herbal resource of vine tea[J]. Chinese Traditional and Herbal Drugs,2016,47(20):3728−3735. doi: 10.7501/j.issn.0253-2670.2016.20.028 [13] 张红忠, 雷林, 罗正江, 等. 初探藤茶的文献研究[J]. 贵州农机化,2018(3):53−55, 61. [Zhang Hongzhong, Lei Lin, Luo Zhengjiang, et al. Preliminary study on the literature of Ampelopsis grossedentata[J]. Guizhou Agricultural Mechaniation,2018(3):53−55, 61. [14] 罗祖友, 付晓芳, 吴谋成. 藤茶的研究进展[J]. 食品科学,2005,26(8):513−517. [Luo Zuyou, Fu Xiaofang, Wu Moucheng. Progress on the study of Ampelopsis grossedentata[J]. Food Science,2005,26(8):513−517. doi: 10.3321/j.issn:1002-6630.2005.08.133 [15] Hou X L, Tong Q, Wang W Q, et al. Suppression of inflammatory responses by dihydromyricetin, a flavonoid from Ampelopsis grossedentata, via inhibiting the activation of NF-κB and MAPK signaling pathways[J]. J Nat Prod,2015,78(7):1689−1696. doi: 10.1021/acs.jnatprod.5b00275
[16] 周茜雅, 陈婧, 方建国, 等. 藤茶抗菌作用研究进展[J]. 中草药,2017,48(22):4819−4825. [Zhou Qianya, Chen Jing, Fang Jianguo, et al. Research progress on antibacterial effects of Ampelopsis grossedentata[J]. Chinese Traditional and Herbal Drugs,2017,48(22):4819−4825. doi: 10.7501/j.issn.0253-2670.2017.22.034 [17] 徐新, 李佳川, 王元, 等. 土家药食资源藤茶提取物体外抗氧化活性研究[J]. 西南民族大学学报(自然科学版),2018,44(2):171−175. [Xu Xin, Li Jiachuan, Wang Yuan, et al. In vitro antioxidant activity of vine tea extracts from medicinal resources in Tujia county[J]. Journal of Southwest Minzu University(Natural Science Edition),2018,44(2):171−175. [18] Le L, Jiang B, Wan W, et al. Metabolomics reveals the protective of dihydromyricetin on glucose homeostasis by enhancing insulin sensitivity[J]. Rep,2016,6:36184.
[19] 左雪媚, 刘倩, 廖芳帆, 等. 藤茶黄酮对高脂大鼠的降血脂作用研究[J]. 湖南农业科学,2019(6):18−22. [Zuo Xuemei, Liu Qian, Liao Fangfan, et al. Study on the effects of reducing blood lipid by flavonoids from Ampelopsis grossedentata on hyperlipidemia rats[J]. Agricultural Science & Technology,2019(6):18−22. [20] 赵喜兰. 显齿蛇葡萄叶总黄酮对原发性高血压大鼠的降血压研究[J]. 食品工业科技,2016,37(6):351−355. [Zhao Xilan. Effect of the flavonoid fraction of Ampelopsis grossedentata on spontaneously hypertensive rats[J]. Science and Technology of Food Industry,2016,37(6):351−355. [21] 白云凯, 刘惠, 肖桦, 等. 代谢综合征肾损伤观察[J]. 昆明医学院学报,2002,23(1):69−71. [Bai Yunkai, Liu Hui, Xiao Ye, et al. Observation on renal lesion due to metabolic syndrome[J]. Academic Journal of Kunming Medical College,2002,23(1):69−71. [22] 王灿, 苗志敏, 李长贵, 等. 人体血尿酸水平对血清谷丙转氨酶和谷草转氨酶水平的影响[J]. 山东医药,2010,50(29):1−3. [Wang Can, Miao Zhimin, Li Changgui, et al. Impact of uric acid on alanine amiotransferase and aspartate aminotransferase[J]. Shandong Medical Journal,2010,50(29):1−3. doi: 10.3969/j.issn.1002-266X.2010.29.001 [23] Lai S, Mariotti A, Coppola B, et al. Uricemia and homocysteinemia: Nontraditional risk factors in the early stages of chronic kidney disease-preliminary data[J]. Eur Rev Med Pharmacol Sci,2014,18(7):1010−1017.
[24] 张文, 李楠, 刘守东, 等. 海勤疗养员高尿酸血症对高血脂及肝功能的影响[J]. 中国疗养医学,2020,29(12):1259−1261. [Zhang Wen, Li Nan, Liu Shoudong, et al. Effects of hyperuricemia on hyperlipidemia and liver function in marine convalescents[J]. Chinese Journal of Convalescent Medicine,2020,29(12):1259−1261. [25] Qian X, Wang X, Luo J, et al. Hypouricemic and nephroprotective roles of anthocyanins in hyperuricemic mice[J]. Food Funct,2019,10(2):867−878. doi: 10.1039/C8FO02124D
[26] Zhang R, Zhan S, Li S, et al. Anti-hyperuricemic and nephroprotective effects of extracts from Chaenomeles sinensis (Thouin) Koehne in hyperuricemic mice[J]. Food Funct,2018,9(11):5778−5790. doi: 10.1039/C8FO01480A
[27] Chen Y, Li C, Duan S, et al. Curcumin attenuates potassium oxonate-induced hyperuricemia and kidney inflammation in mice[J]. Biomed Pharmacother,2019,118:109195. doi: 10.1016/j.biopha.2019.109195
[28] Yong T, Li D, Li M, et al. Anti-hyperuricemic effect of 2-hydroxy-4-methoxy-benzophenone-5-sulfonic acid in hyperuricemic mice through XOD[J]. Molecules,2018,23(10):2671. doi: 10.3390/molecules23102671
[29] 朱春霞. 虎桂药对有效组分配伍干预高尿酸血症及其肾保护作用机制研究[D]. 中山: 广东药科大学, 2018: 4−5. Zhu Chunxia. The mechanism study on effects of effective component compatibility of Polyonum cuspidatum and Ramulus cinnamomi on hyperuricemia and renal protection[D]. Zhongshan: Guangdong Pharmaceutical University, 2018: 4−5.
[30] 王陈芸, 李哲丽, 叶尤松, 等. 氧嗪酸钾致小鼠急性高尿酸血症动物模型的研究及评价[J]. 中药药理与临床,2019,35(1):176−180. [Wang Chenyun, Li Zheli, Ye Yousong. Study and evaluation of potassium oxonate-induced acute hyperuricemia animal mode[J]. Pharmacology and Clinics of Chinese Materia Medica,2019,35(1):176−180.





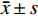

 下载:
下载:






 下载:
下载:
